Clear Sky Science · nl
De positieve feedbacklus UFL1-AKT bevordert de progressie van borstkanker door de lipidesynthese te versterken
Waarom kankercellen zo veel geven om vet
Borstkankercellen, zoals alle snelgroeiende cellen, hebben een constante aanvoer van bouwstenen nodig om nieuwe membranen en signaalmoleculen te maken. Vetten, of lipiden, vormen een kernonderdeel van die aanvoer. Deze studie onthult hoe een weinig bekend proteïnesysteem kankercellen in een "vetproductie‑overdrive" zet, waardoor tumoren groeien en behandelingen ontwijken. Inzicht in deze verborgen brandstoflijn kan nieuwe wegen openen om borstkanker te vertragen of uit te hongeren.
Een verborgen proteïnetag met grote gevolgen
Onze cellen passen voortdurend het gedrag van hun eiwitten aan met kleine chemische tags. Een van die tags, UFM1 genoemd, wordt aangebracht door een enzym dat UFL1 heet. UFM1‑tagging (UFMylatie) is in verband gebracht met DNA‑herstel en stressreacties, maar de rol ervan bij kanker was onduidelijk. De auteurs tonen aan dat UFL1 veel actiever is in menselijke borstkweken dan in normaal borstweefsel, in alle belangrijke subtypen. Patiënten met tumoren met hogere UFL1‑niveaus hebben doorgaans een slechtere overleving. Wanneer onderzoekers UFL1 in borstkankercellen of in muizen tumoren verminderden, vertraagde de kankergroei, daalde de celdeling en nam celdood toe, wat suggereert dat UFL1 zich als een kankerverwekkende factor gedraagt.
Hoe een signaalhub wordt omgeschakeld naar vetproductiemodus
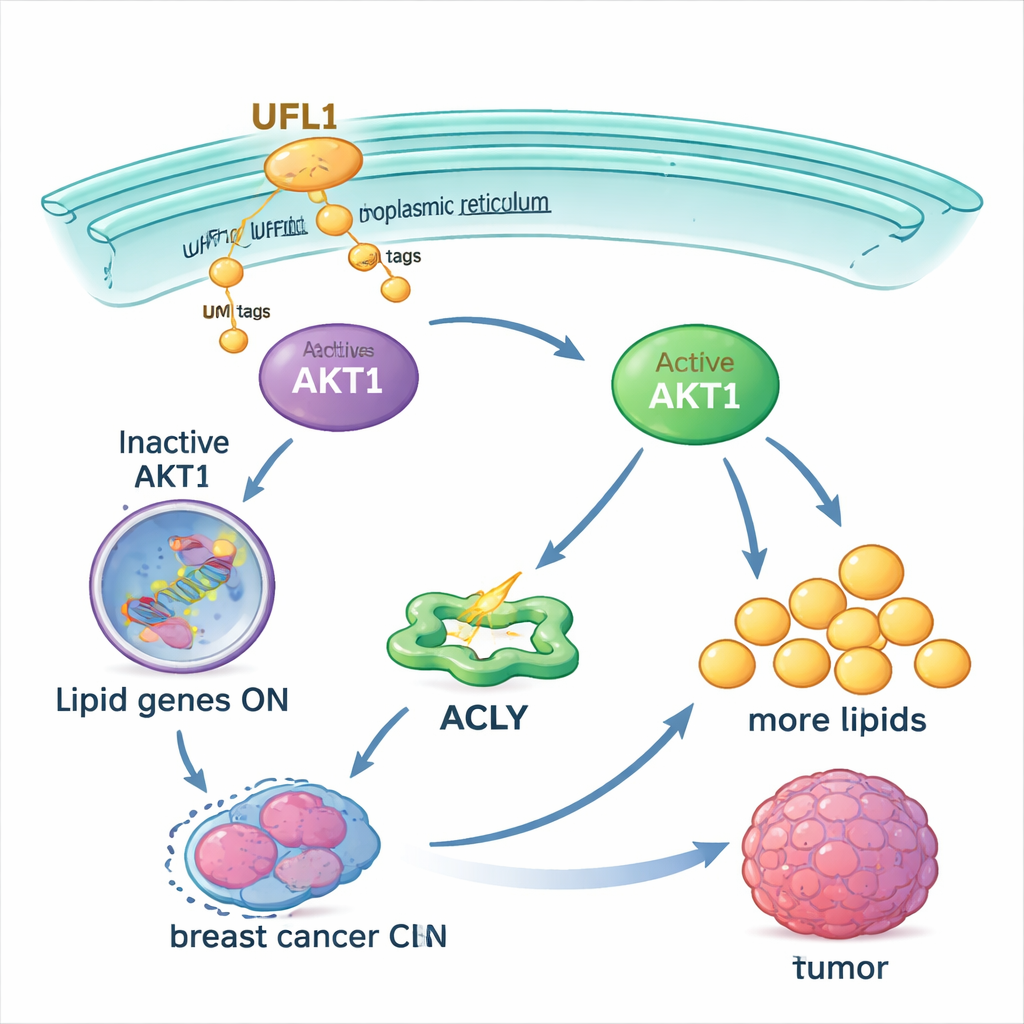
Om te begrijpen hoe UFL1 tumoren helpt, zocht het team naar moleculaire partners en vond een sleutelregulator van signalen genaamd AKT1. AKT1 is een centraal schakelaar die cellen aanzet tot groei en tot het maken van nieuwe lipiden. De studie laat zien dat UFL1 fysiek bindt aan AKT1 en het op meerdere specifieke plaatsen voorziet van UFM1‑tags. Deze tagging verandert de vorm van AKT1, waardoor een interne "rem" die het normaal stilhoudt, wordt versoepeld. Het helpt AKT1 ook verplaatsen naar een membraangebied binnen de cel, het endoplasmatisch reticulum, waar andere enzymen het volledig kunnen activeren door fosfaatgroepen toe te voegen. Zonder UFM1‑tags op die plaatsen is AKT1 veel moeilijker te activeren.
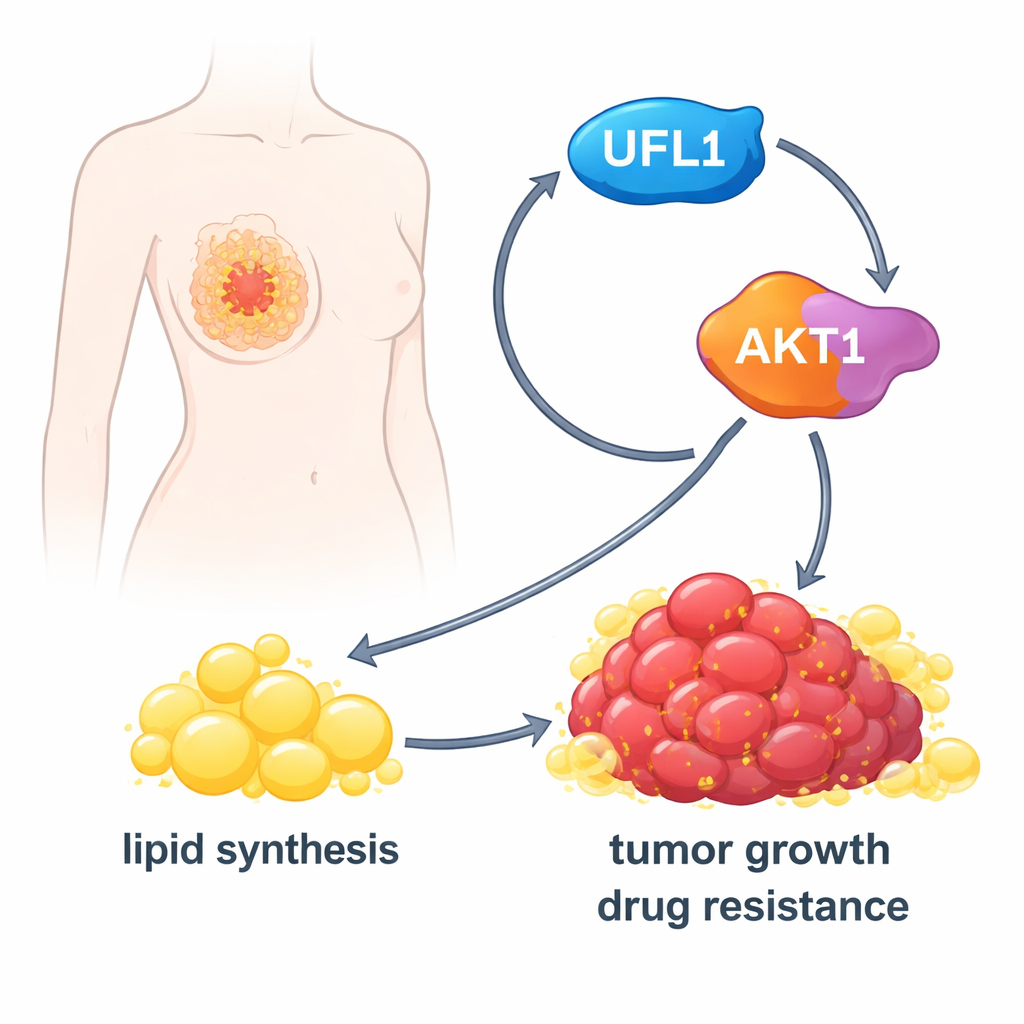
Het aanzetten van de kanker‑vetfabriek
Eens geactiveerd zet AKT1 cellen ertoe aan hun vetproductie op te voeren. Het verhoogt de activiteit van een belangrijk metabolisch enzym, ACLY, en verhoogt de niveaus van hoofdregulatoren zoals SREBP1 die vele vet‑producerende genen inschakelen. In in het laboratorium gekweekte borstkankercellen zorgde UFL1 ervoor dat cellen meer vetdruppels, vrije vetzuren en cholesterol ophoopten. Het verwijderen van UFL1 verminderde deze lipidevoorraden scherp, zowel in kweek als in in muizen gegroeide tumoren. Het van buitenaf toevoegen van extra vetzuren kon het groeiverlies van UFL1‑deficiënte kankercellen grotendeels herstellen, wat aangeeft dat het belangrijkste effect van UFL1 is het veiligstellen van voldoende lipiden om tumoruitbreiding te ondersteunen.
Een zelfversterkende lus die tumorgroei aandrijft
Verrassend genoeg loopt de relatie tussen UFL1 en AKT1 beide kanten op. De onderzoekers ontdekten dat zodra AKT1 actief is, het op zijn beurt een fosfaat‑tag aan UFL1 toevoegt op een specifieke plaats. Deze modificatie versterkt UFL1’s vermogen om AKT1 met UFM1 te taggen, waardoor een positieve feedbacklus ontstaat: UFL1 activeert AKT1, en AKT1 activeert UFL1. Het muteren van ofwel de UFM1‑taggingsites op AKT1 of de fosfaatsite op UFL1 doorbreekt deze lus. In muizen groeiden tumoren met deze gemuteerde versies slecht, bevatten ze minder lipiden en vertoonden ze meer stervende cellen. In monsters van patiënten met triple‑negatieve borstkanker verschenen hogere niveaus van geactiveerd UFL1 en geactiveerd AKT1 vaak samen, wat benadrukt dat deze lus ook in echte tumoren actief is.
De lus verzwakken om behandelingen effectiever te maken
Aangezien veel medicijnonderzoeken AKT al als doelwit hebben, testten de auteurs of het blokkeren van UFMylatie deze behandelingen effectiever kon maken. In borstkankercellen verlaagden zowel een kleine‑molecuulremmer van UFMylatie als een AKT‑remmer elk de AKT1‑activiteit en de lipideophoping, maar het combineren van beide werkte veel beter dan elk afzonderlijk. De combinatie vertraagde ook de tumorgroei en verminderde het vetgehalte in muizen tumoren zonder merkbaar gewichtsverlies bij de dieren. Het blokkeren van UFMylatie maakte kankercellen bovendien gevoeliger voor standaardchemotherapieën zoals cisplatine en etoposide, die vaak falen wanneer AKT sterk actief is.
Wat dit voor patiënten betekent
Voor een niet‑specialist laat de studie zien dat bepaalde borstkankers zichzelf bedraden met een zelfversterkende lus die zowel hun groei als hun vetaanvoer voedt. UFL1 en AKT1 werken samen als twee pedalen die tegelijk worden ingedrukt: de één tagt, de ander geeft signalen, en samen zetten ze de lipidenproductie en de tumorgroei in gang. Door geneesmiddelen te vinden die deze lus verstoren — hetzij door UFMylatie, AKT1 of hun interactie te blokkeren — kunnen toekomstige therapieën mogelijk de tumorgroei vertragen en bestaande behandelingen effectiever maken, vooral bij agressieve vormen van borstkanker.
Bronvermelding: Meng, F., Du, Y., Liang, J. et al. The UFL1-AKT positive feedback loop promotes breast cancer progression by enhancing lipid synthesis. Nat Commun 17, 614 (2026). https://doi.org/10.1038/s41467-026-68492-3
Trefwoorden: borstkanker, lipidenmetabolisme, AKT‑signaaltransductie, UFMylatie, gerichte therapie