Clear Sky Science · nl
Continu continu verstelbare multistabiliteit in DNA-replicatienetwerken
Van eenvoudige schakelaars naar vele mogelijke toestanden
Biologische systemen, van delende cellen tot zich ontwikkelende embryo’s, werken zelden als eenvoudige lichtschakelaars die alleen aan of uit kunnen staan. Vaak nemen ze eerder vele langdurige toestanden aan, zoals een dimmer die op talloze posities kan blijven hangen. Dit artikel beschrijft een chemisch netwerk op DNA‑basis dat eerder als die dimmer werkt: het kan stabiel niet slechts een paar onderscheiden toestanden handhaven, maar in wezen elke samenstelling langs een continu spectrum. Die mogelijkheid kan een krachtige basis vormen voor toekomstige slimme materialen, moleculaire geheugens en biochemische computers die analoge, en niet alleen digitale, informatie verwerken.
Waarom meerdere stabiele toestanden belangrijk zijn
Veel cellulaire beslissingen — of een stamcel rijpt, een cel zichzelf doet afsterven of een gennetwerk een eerder signaal onthoudt — hangen af van “multistabiliteit”, het vermogen om onder gelijke omstandigheden in meer dan één stabiel activiteitspatroon te rusten. Traditionele synthetische versies van zulke systemen zijn opgebouwd uit gencircuits, enzymen of DNA-strengen die elkaar aan- of uitzetten. Deze ontwerpen leveren doorgaans een handjevol discrete uitkomsten op, zoals klassieke bistabiele schakelaars met twee langdurige toestanden. Opschalen van dat idee is lastig: een N‑toestandsysteem kan ongeveer N×(N−1) zorgvuldig afgestemde remmende verbindingen vereisen, en het systeem blijft nog steeds alleen tussen een klein aantal vaste punten wisselen in plaats van een vloeiend continuüm van mogelijkheden te bieden.
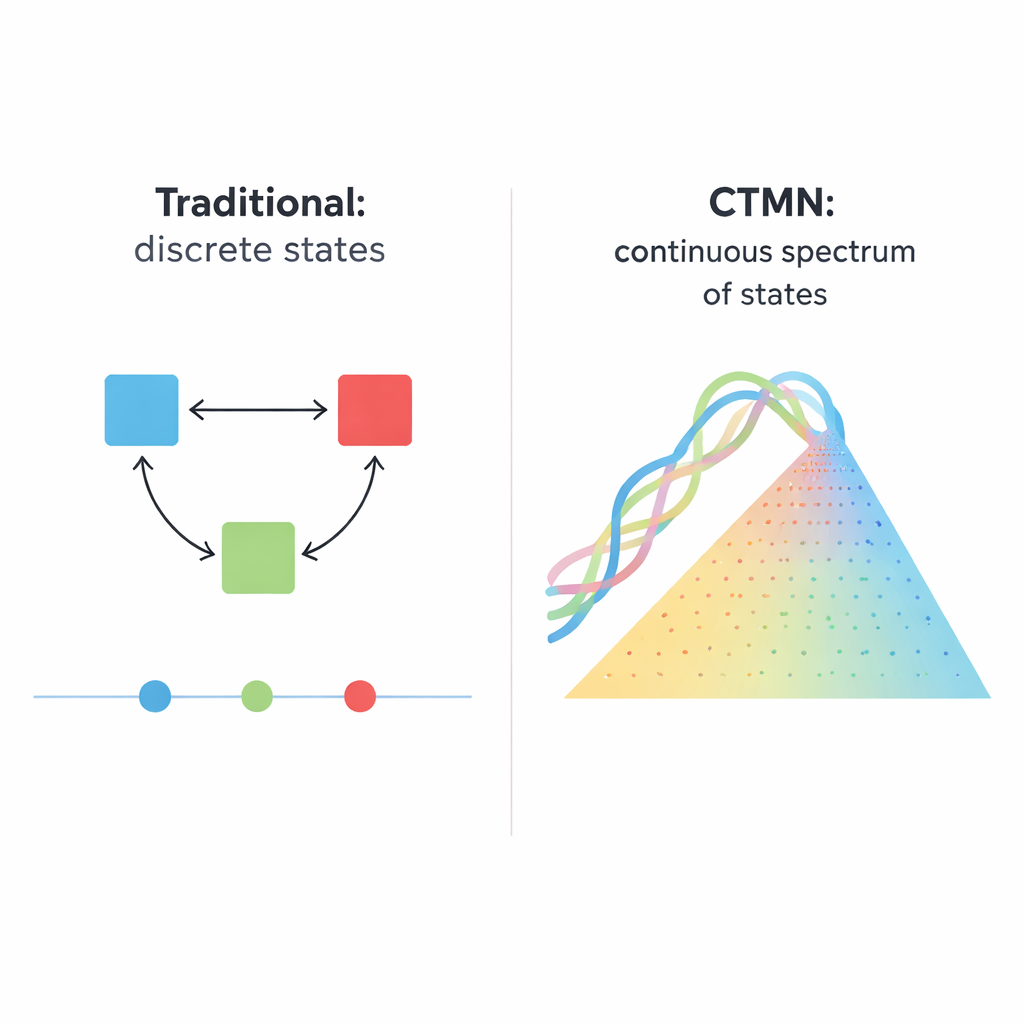
Een nieuw soort DNA-netwerk: continu verstelbaar
De auteurs introduceren een ander ontwerpprincipe, geïmplementeerd in wat zij continu verstelbare multistabiliteitsnetwerken (CTMN’s) noemen. In plaats van te vertrouwen op vele afzonderlijke remsignalen, gebruiken ze directe competitie tussen DNA-replicatiemodules die verbonden zijn door reversibele strand‑uitwisselingsreacties. Elke module bestaat uit ontworpen DNA-duplexen die zowel kunnen deelnemen aan strandverplaatsing als dienstdoen als sjabloon voor DNA‑polymerase, ondersteund door een nicking‑enzym dat sleutelsegmenten knipt en herstelt. De chemische brandstof — nucleotide bouwstenen genoemd dNTP’s — drijft voortdurende polymerisatie en nicking aan en houdt het systeem ver van evenwicht. Onder deze omstandigheden “bevriezen” de concurrerende modules effectief in welke relatieve verhoudingen ze ook begonnen, waardoor niet slechts twee of drie uitkomsten ontstaan maar een hele continue lijn (of, bij meer modules, een vlak) van langdurige toestanden.
Hoe de moleculaire machine het geheugen vergrendelt
In hun eenvoudigste netwerk met twee modules, CTMN‑1, tonen de onderzoekers experimenteel en met gedetailleerde kinetische modellering aan dat het systeem kan neerkomen op een familie van stabiele mengsels die bijna het volledige bereik bestrijken van “voornamelijk module A” tot “voornamelijk module B.” Polymerisatie zet actieve duplexen om in verlengde vormen die tijdelijk uit de stranduitwisselingscompetitie zijn verwijderd; nicking herstelt ze vervolgens, en sluit zo een autoregulerende lus. Wanneer beide modules deze lus delen, onderdrukken ze wederzijdse interconversie zo sterk dat het systeem gedurende vele uren dicht bij zijn beginsamenstelling blijft, mits brandstof beschikbaar is. Lineaire stabiliteitsanalyse van de onderliggende vergelijkingen onthult een gehele manifold — feitelijk een continuüm — van evenwichtstoestanden, in tegenstelling tot het enkele vaste punt dat wordt gezien wanneer enzymen of brandstof worden verwijderd.
Programmeerbare reacties en moleculair geheugen
Aangezien de toestand van het netwerk is opgeslagen in DNA‑samenstellingen, kan deze op programmeerbare manieren worden gestuurd en uitgelezen. De auteurs ontwerpen korte RNA “triggers” die tijdelijk aan specifieke DNA-strengen binden, de competitie bevoordelen en het netwerk naar een nieuwe samenstelling verschuiven. Zelfs nadat het RNA door een enzym is afgebroken, blijft de nieuwe toestand bestaan en functioneert ze als een vorm van moleculair geheugen. Herhaalde of sterkere stimuli verplaatsen het systeem vloeiend langs het continuüm van toestanden in plaats van het tussen simpele aan/uit‑posities te laten omslaan. Bovendien kunnen de DNA‑replicatieproducten zelf worden aangepast om als signalen voor downstreamprocessen te fungeren: in demonstraties activeren verschillende toestanden van CTMN‑1 selectief een van twee DNA‑gebaseerde katalysatoren of bevoordelen ze RNA‑transcriptie richting een van twee boodschapperstrengen, zonder de onderliggende multistabiliteit te verstoren.
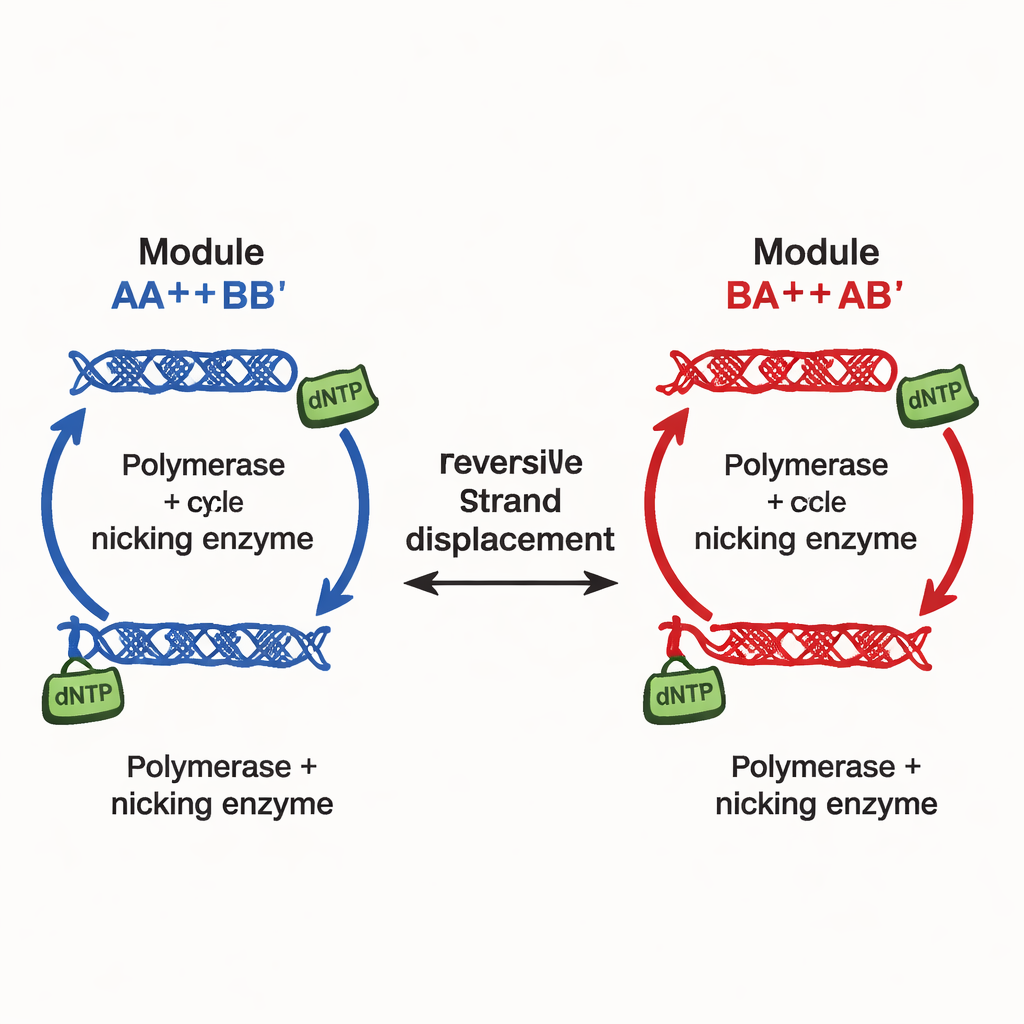
Opschalen naar complexe moleculaire “dimmers”
Om aan te tonen dat deze strategie schaalbaar is, bouwen de onderzoekers een netwerk met drie modules, CTMN‑2, door extra ontworpen DNA‑duplexen toe te voegen die een gemeenschappelijk uitwisselingsdomein delen maar verschillende replicatiesjablonen coderen. Nu vullen de mogelijke evenwichtstoestanden een tweedimensionale regio, zoals punten over een driehoekig fasediagram, in plaats van langs een eenvoudige lijn. Opnieuw bevestigen experimenten dat veel verschillende samenstellingen stabiel zijn zolang brandstof en enzymen aanwezig zijn, en dat ze allemaal naar een enkel evenwichtspunt inzakken wanneer de energievoorziening wordt verwijderd. Omdat het toevoegen van nieuwe modules alleen nieuwe DNA‑constructen vereist die op hetzelfde verplaatsingskader worden aangesloten, neemt de algehele bedrading niet explosief in complexiteit toe zoals bij traditionele ontwerpen.
Wat dit betekent voor toekomstige moleculaire technologieën
Voor niet‑specialisten is de kernboodschap dat de auteurs een DNA‑replicatienetwerk hebben omgevormd tot een hoogst flexibel, analoog geheugentoestel. In plaats van te kiezen uit een paar vooraf ingestelde opties, kan hun systeem betrouwbaar een van tientallen experimenteel te onderscheiden toestanden vasthouden, elk gedefinieerd door hoeveel van elke DNA‑module aanwezig is, en kan het voorbijgaande chemische pulsen omzetten in langdurige verschuivingen langs dit continuüm. Omdat de uitgaande DNA‑strengen programmeerbaar zijn en losstaan van het stabiliserende mechanisme, zou hetzelfde raamwerk in principe een breed scala aan downstream biochemische reacties of materiaaleigenschappen met fijne, graduele controle kunnen reguleren. Dit werk wijst daarmee in de richting van moleculaire apparaten die rekenen, onthouden en zich aanpassen meer als neurale of mechanische analoge systemen dan als eenvoudige digitale schakelaars.
Bronvermelding: Zhong, R., Fu, Y., Jiang, S. et al. Continuously tunable multistability in DNA replication networks. Nat Commun 17, 1782 (2026). https://doi.org/10.1038/s41467-026-68488-z
Trefwoorden: DNA-multistabiliteit, moleculair geheugen, synthetische biochemische netwerken, DNA-strandaustopping, analoog moleculair rekenen