Clear Sky Science · nl
Robuuste en interpreteerbare voorspelling van genmarkers en celt types uit ruimtelijke transcriptomics-gegevens
Routine weefselpreparaten omzetten in moleculaire kaarten
Wanneer een biopsie wordt afgenomen zien artsen doorgaans alleen wat de microscoop onthult: de vormen en patronen van cellen in roze-en-paarse kleuringen. Onder die kleuren ligt echter een verborgen wereld van genen die aan- of uitgaan en daarmee beïnvloeden hoe een kanker groeit en reageert op behandeling. Deze studie introduceert STimage, een nieuw kunstmatig-intelligentiesysteem dat probeert dat moleculaire script rechtstreeks uit standaard pathologiebeelden te lezen, en zo mogelijk sneller en goedkoper inzicht biedt zonder aanvullende laboratoriumtests.
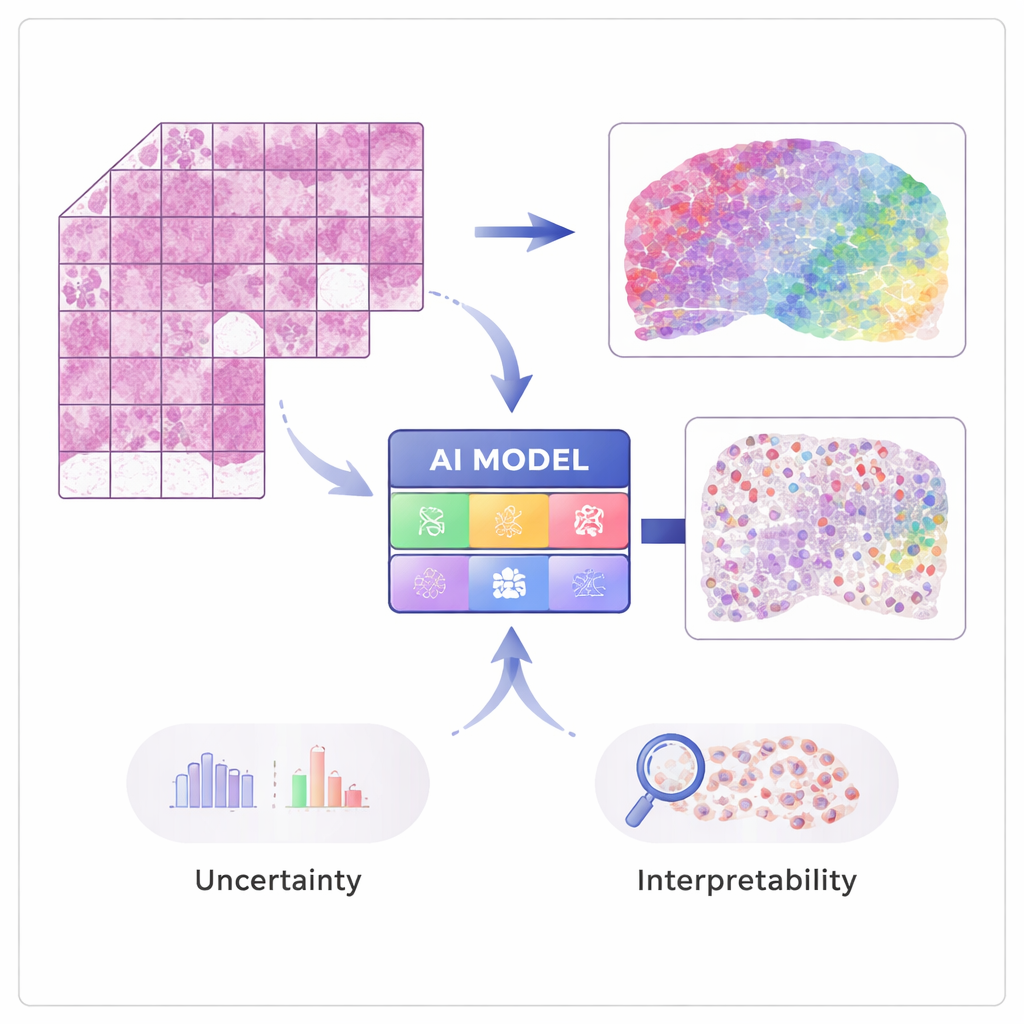
Van afbeelding naar genactiviteit
Moderne technieken in “ruimtelijke transcriptomics” kunnen de activiteit van tienduizenden genen meten terwijl wordt vastgehouden waar elk signaal in het weefsel vandaan kwam. Deze methoden zijn krachtig maar duur en nog niet routinematig in ziekenhuizen. STimage wordt getraind op een bescheiden aantal van zulke ruimtelijke datasets, waarbij elk weefselbeeld is gekoppeld aan gedetailleerde genmetingen op vele kleine plekjes. De AI leert lokale visuele patronen op de hematoxyline- en eosine (H&E)-kleuring—zoals hoe dicht opeengepakt of onregelmatig de kernen zijn—te matchen met de onderliggende genactiviteit, zodat ze later genexpressie en celtypen kan voorspellen op basis van gewone beelden alleen.
Een betrouwbaardere AI-patholoog bouwen
Een belangrijk doel van het werk is niet alleen nauwkeurigheid, maar ook betrouwbaarheid en verklaarbaarheid. In plaats van voor elk gen één enkel getal uit te geven, voorspelt STimage een volledige kansverdeling die een waarschijnlijke bandbreedte van genactiviteit op elke locatie beschrijft. Het scheidt ook twee soorten onzekerheid: één veroorzaakt door lawaaierige of variabele data, en een andere die de eigen onwetendheid van het model weerspiegelt. Door veel licht verschillenden versies van het model te trainen en die te middelen—een ensemble-benadering—verbeteren de onderzoekers zowel de prestatie als het inzicht in waar het systeem zeker is en waar niet, wat cruciaal is voor klinische besluitvorming.
Getest over kankers, technologieën en ziekenhuizen heen
Het team evalueerde STimage op uiteenlopende datasets van borstkanker, huidkanker en nierkanker, evenals een immuungerelateerde leverziekte. Het leerde belangrijke kanker- en immuunmarkers te voorspellen, vaak in overeenstemming met de echte ruimtelijke patronen die in onafhankelijke experimenten werden gezien. Het model bleef standhouden wanneer het werd uitgedaagd met data uit verschillende laboratoria, verschillende methoden voor samplevoorbereiding en zelfs verschillende onderliggende technologieën, waaronder platformen met enkelcelresolutie en oudere, lagere-resolutie systemen. In directe vergelijkingen met verschillende bestaande AI-tools kwamen STimage en zijn ensemblevarianties meestal als beste uit de bus, vooral bij het beoordelen hoe goed de voorspelde patronen overeenkwamen met de werkelijke verdeling van genactiviteit in het weefsel.
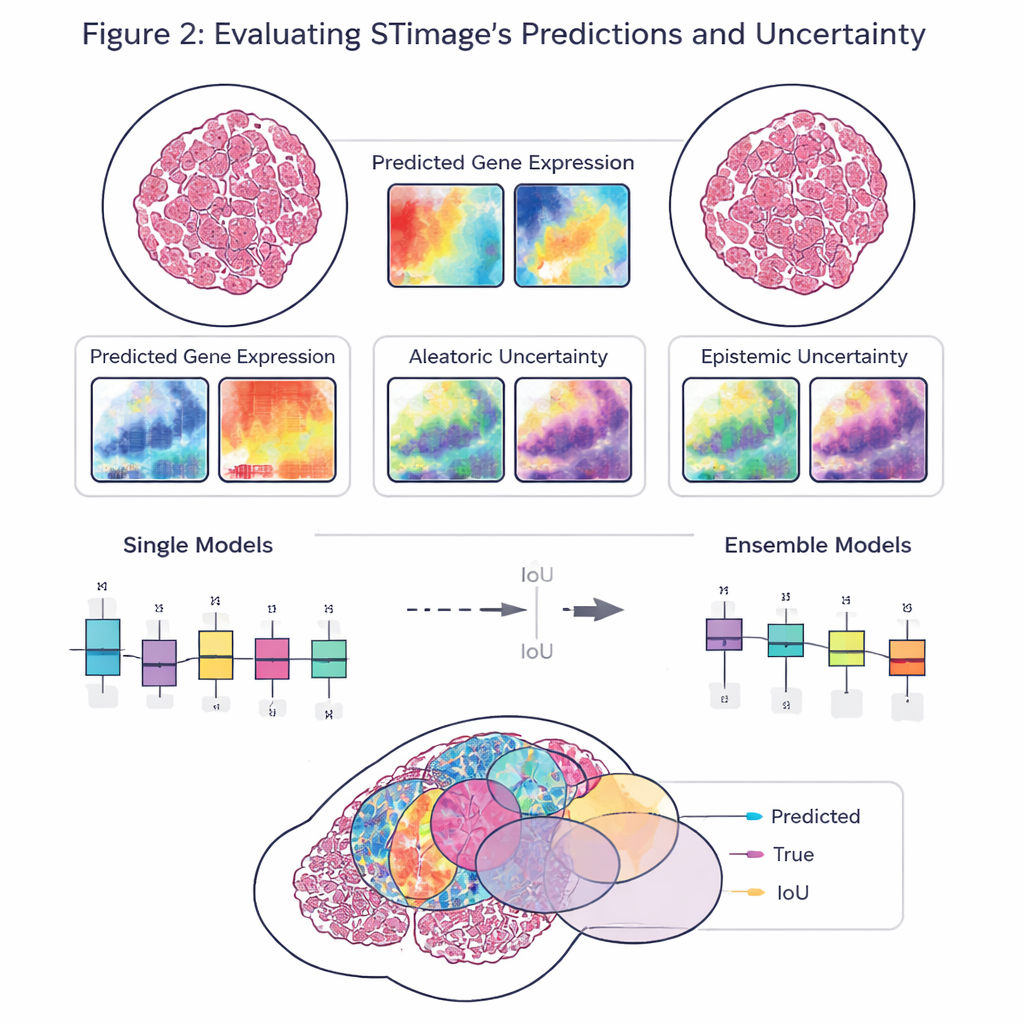
In tumoren kijken: cellen, overleving en medicijnrespons
STimage gaat verder dan genvoorspelling en leidt af welke celtypen elk gebied bezetten, met behulp van hoogresolutie-datasets waarin de identiteit van elke cel bekend is. Het model kon kankercellen onderscheiden van immuun- en ondersteunende cellen en hun rangschikking over een preparaat in kaart brengen. De auteurs pasten STimage vervolgens toe op grote verzamelingen routinematige kankerpictures uit The Cancer Genome Atlas. Zelfs zonder ruimtelijke metingen waren de door de AI voorspelde genprofielen nauw verwant aan echte bulk-gengegevens. Deze voorspellingen waren sterk genoeg om patiënten in hogere- en lagere-risicogroepen in te delen en te helpen onderscheiden welke patiënten waarschijnlijker volledig zouden reageren op bepaalde behandelingen voor borstkanker.
Waarom dit belangrijk is voor toekomstige patiënten
Voor patiënten en clinici is de belofte van STimage een soort “moleculair overlager” op het vertrouwde pathologiediapositief. In plaats van meerdere dure tests aan te vragen, zou één gescande afbeelding op een dag kunnen onthullen waar agressieve genprogramma’s actief zijn, hoe immuuncellen verdeeld zijn en welke markers wijzen op betere of slechtere uitkomsten of verschillende medicijnresponsen. Hoewel de methode nog wordt verfijnd en de correlatie met echte metingen niet perfect is, maakt het vermogen om ruimtelijke patronen vast te leggen, zijn eigen onzekerheid te schatten en te benadrukken welke cellen zijn voorspellingen aandrijven, het een praktische stap richting meer informatieve, transparante digitale pathologie.
Bronvermelding: Tan, X., Mulay, O., Xie, J. et al. Robust and interpretable prediction of gene markers and cell types from spatial transcriptomics data. Nat Commun 17, 1781 (2026). https://doi.org/10.1038/s41467-026-68487-0
Trefwoorden: digitale pathologie, ruimtelijke transcriptomics, kankerbiomarkers, deep learning, tumormicro-omgeving