Clear Sky Science · nl
PTRAMP, CSS en Ripr vormen een geconserveerd complex dat vereist is voor de invasie van merozoïeten van Plasmodium-soorten in erytrocyten
Waarom dit belangrijk is in de strijd tegen malaria
Malariaparasieten moeten onze rode bloedcellen binnendringen om ziekte te veroorzaken. Deze studie onthult een klein aantal eiwitten die samen een gedeelde "instapbrug" vormen die door meerdere belangrijke malariasoorten wordt gebruikt, inclusief die welke mensen infecteren. Door te laten zien hoe deze brug wordt opgebouwd en hoe antilichamen die soms kunnen blokkeren, wijst het werk op nieuwe manieren om vaccins te ontwerpen die mogelijk tegen meer dan één type malaria tegelijk bescherming bieden. 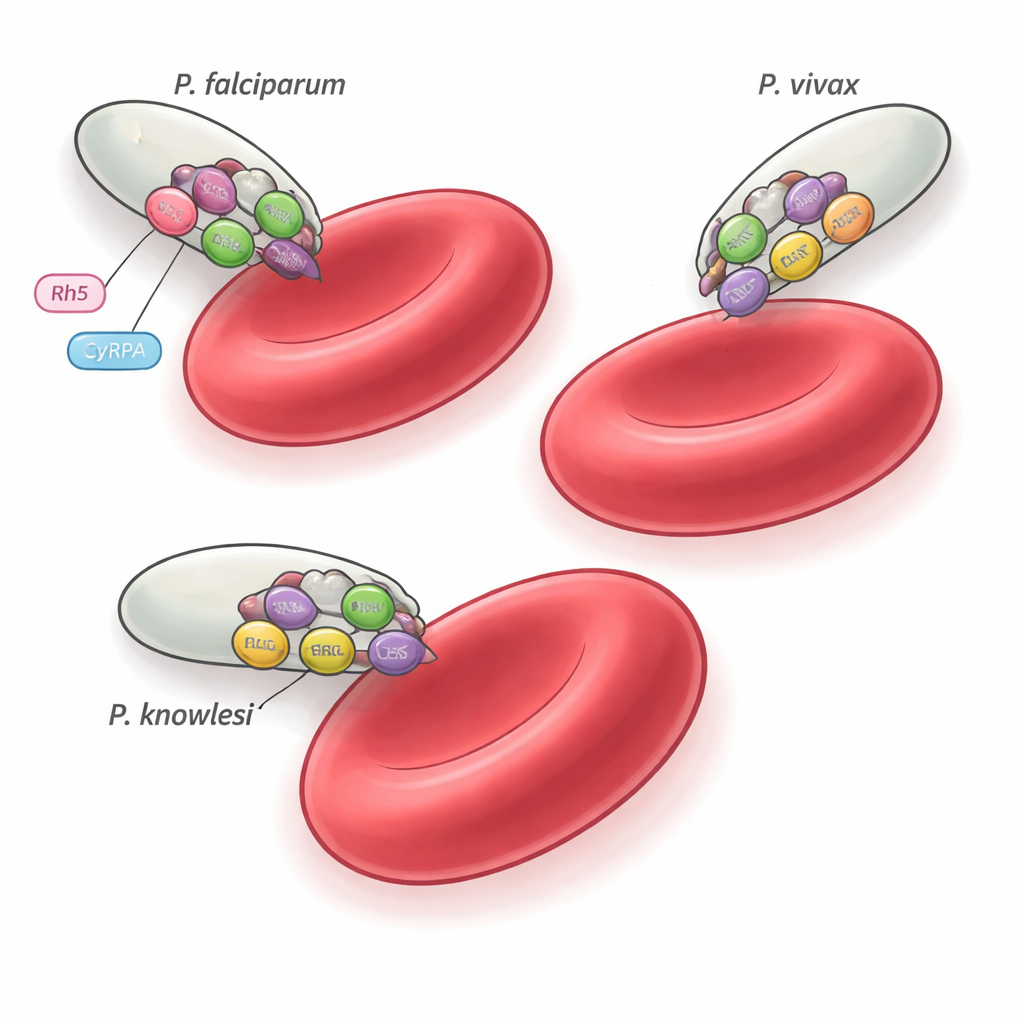
Een gemeenschappelijke gereedschapsset bij veel malariaparasieten
Er zijn meer dan 200 Plasmodium-soorten, maar slechts een handvol, zoals P. falciparum, P. vivax en P. knowlesi, infecteert mensen. Deze soorten staan op verschillende takken van de parasietenstamboom en geven de voorkeur aan verschillende typen rode bloedcellen, maar ze moeten allemaal erytrocyten met uiterste precisie binnendringen. Eerdere studies in P. falciparum identificeerden een vijfdelige assemblage, het PCRCR-complex, dat essentieel is voor invasie en zich vastklikt aan een humaan receptor op rode bloedcellen genaamd basigin. Eén onderdeel van dat complex, een eiwit genaamd Rh5, is uniek voor P. falciparum en zijn nauwe verwanten, wat een raadsel oproept: wat gebruiken andere malariasoorten in plaats daarvan? De huidige studie richt zich op drie begeleidende eiwitten — PTRAMP, CSS en Ripr — die in het hele geslacht geconserveerd zijn en test of ze een universele invasie‑machine vormen.
Het bouwen van een driedelige invasiebrug
Met sequentiezoeksels in vele parasietgenomen tonen de auteurs aan dat PTRAMP, CSS en Ripr aanwezig zijn in alle belangrijke Plasmodium-lijnen, in tegenstelling tot Rh5 dat beperkt is tot één subgroep. Structuurvoorspellingen met AlphaFold, gecombineerd met gedetailleerde biochemische metingen, onthullen dat PTRAMP en CSS samenkomen en een stabiel paar vormen, bijeengehouden door een specifieke disulfidebinding tussen twee geconserveerde cysteïnes. Dit tweeeiwitsplatform klemt zich vervolgens vast aan het staartuiteinde van Ripr en creëert een driedelig PTRAMP–CSS–Ripr (PCR) complex. Experimenten met eiwitten van P. falciparum, P. vivax en P. knowlesi tonen aan dat dit complex in alle drie soorten met hoge affiniteit vormt, en dat slechts een klein gebied aan het C‑terminale uiteinde van Ripr nodig is voor sterke binding. 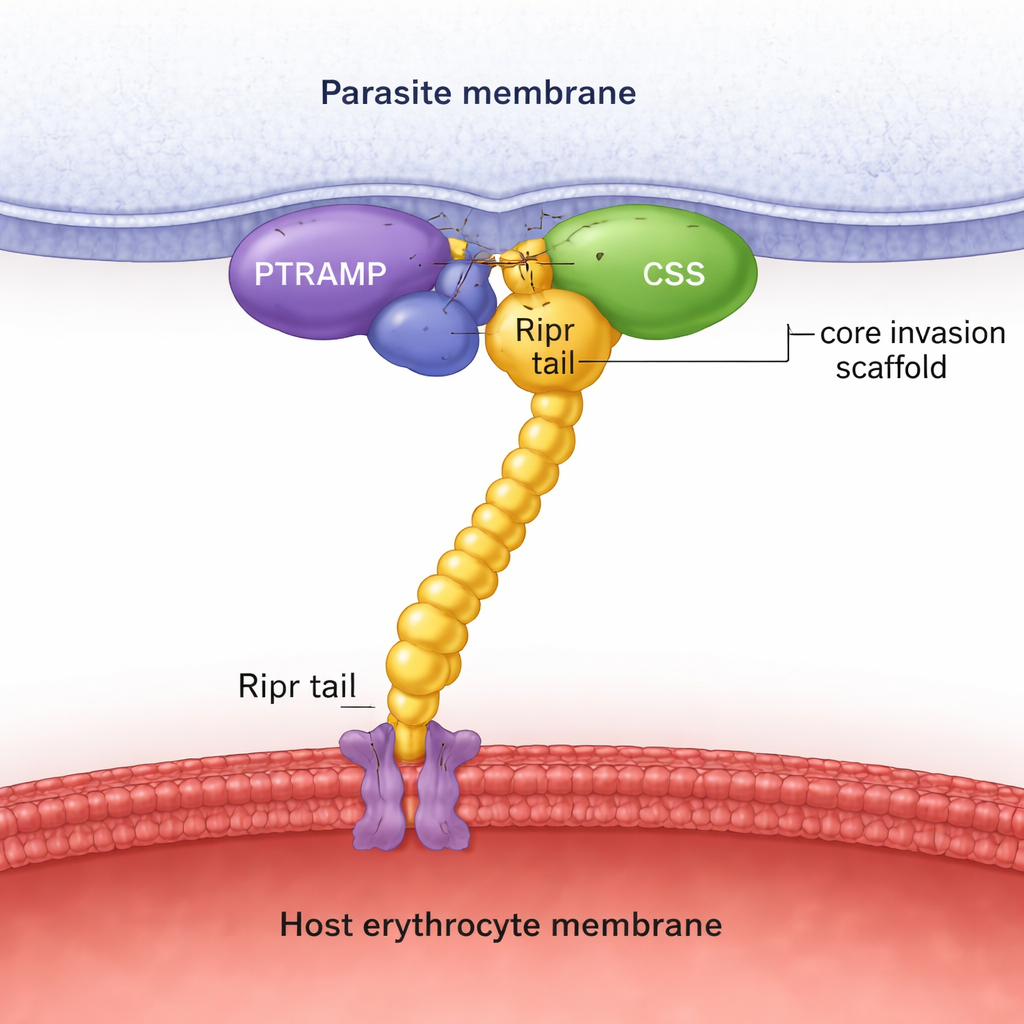
De structuur in atomaire details bekijken
Om verder te gaan dan voorspellingen, loste het team kristalstructuren op en verzamelde cryo‑elektronenmicroscopiebeelden. De kristalstructuur van het PTRAMP–CSS‑paar van P. vivax laat precies zien hoe een korte stretch van PTRAMP over CSS heen loopt en de sleutel‑disulfidebinding vormt. Een andere structuur toont een krachtige antilichaam gebonden aan twee van Ripr’s groeifactor‑achtige domeinen en brengt een remmend epitoop op de Ripr‑staart in kaart. Cryo‑EM‑analyse van het PCR-complex van P. knowlesi bevestigt de algehele vorm die door AlphaFold werd voorspeld: PTRAMP en CSS zitten dicht bij het parasietmembraan en klemmen Ripr vast, waarvan het uitgerekte lichaam zich uitstrekt richting de gastheercel. Samen ondersteunen deze structurele momentopnames het idee dat het PCR-drietal een stijve steunstructuur vormt die fysiek de kloof tussen parasiet en rode bloedcel overbrugt tijdens invasie.
Antilichamen die meer dan één soort herkennen
Omdat deze eiwitten geconserveerd zijn, vroegen de auteurs zich af of humane infecties van nature antilichamen genereren die tussen soorten kruisreageren. Plasma van patiënten geïnfecteerd met P. falciparum, P. vivax of P. knowlesi toonde sterke antilichaamreacties tegen CSS en Ripr van meerdere soorten, wat suggereert dat mensen antilichamen ontwikkelen tegen gedeelde regio’s van het PCR‑complex. Het team produceerde vervolgens monoklonale antilichamen en nanobodies gericht tegen P. vivax PTRAMP, CSS en Ripr, en testte of deze de parasietgroei in kweek konden blokkeren. Sommige antilichamen, vooral één genaamd 5B3 die bindt aan Ripr’s staart, konden de invasie door P. knowlesi remmen en, bij hogere concentraties, ook door P. falciparum. Verrassend genoeg stopten diezelfde antilichamen P. vivax of de nauw verwante apenparasiet P. cynomolgi niet, hoewel ze de eiwitten van die soorten wel konden binden.
Een gedeeld geraamte met soortspecifieke toevoegingen
Functionele tests tonen aan dat het PCR‑complex zelf zich niet vastgrijpt aan rode bloedcellen; in plaats daarvan dient het waarschijnlijk als een geconserveerd structureel geraamte waarop elke soort haar eigen receptorbindende partners opschroeft. In P. falciparum, bijvoorbeeld, werkt het PCR‑drietal samen met CyRPA en Rh5 om basigin op menselijke erytrocyten te engageren. In P. vivax en P. knowlesi blijven de equivalente receptorbindende eiwitten en gastheertargets onbekend, maar dezelfde PTRAMP–CSS–Ripr‑kern lijkt de invasie‑machinerie te organiseren. Het feit dat sommige antilichamen kunnen kruisreageren maar alleen bepaalde soorten remmen, onderstreept hoe subtiele verschillen in complexassemblage en timing de gevoeligheid voor immuunaanval kunnen veranderen.
Wat dit betekent voor toekomstige malariavaccins
Voor een niet‑specialist is de hoofdboodschap dat malariaparasieten van zeer verschillende soorten een gemeenschappelijke "plug" delen die ze gebruiken om in rode bloedcellen te komen — gemaakt van de eiwitten PTRAMP, CSS en Ripr — ook al verbinden ze die plug met verschillende receptoren op het celoppervlak. Deze geconserveerde plug is nu structureel in kaart gebracht en kan in sommige gevallen door antilichamen worden geraakt die tussen soorten werken. Hoewel meer werk nodig is om de volledige set partner‑eiwitten te identificeren en remmende antilichamen te verbeteren, opent de ontdekking van een universeel invasie‑geraamte de deur naar vaccinontwerpen die mogelijk tegen meerdere soorten malaria bescherming bieden in plaats van slechts één.
Bronvermelding: Seager, B.A., Lim, P.S., Xiao, X. et al. PTRAMP, CSS and Ripr form a conserved complex required for merozoite invasion of Plasmodium species into erythrocytes. Nat Commun 17, 1780 (2026). https://doi.org/10.1038/s41467-026-68486-1
Trefwoorden: malariainvasie, Plasmodium-eiwitten, merozoïtetoegang, vaccin voor meerdere soorten, erytrocyteninfectie