Clear Sky Science · nl
Cryo-elektronentomografie onthult gekoppelde flavivirusreplicatie, budding en rijping
Hoe herseninfecterende virussen celmembranen kapen
Flavivirussen, een grote groep virussen waar ook de veroorzakers van dengue en door teken overgedragen encefalitis toe behoren, kunnen de hersenen binnendringen en ernstige ziekte veroorzaken. Hoe deze kleine ziekteverwekkers precies hun genoom kopiëren en nieuwe deeltjes in onze cellen assembleren, bleef echter grotendeels onzichtbaar. Deze studie gebruikt geavanceerde driedimensionale elektronenbeeldvorming bij cryogene temperaturen om tekenoverdraagbare flavivirussen in actie te bekijken in menselijke cellen en muizenhersenen, en onthult een onverwacht nauwe koppeling tussen kopiëren van het genoom, virusassemblage en virusrijping.
Virale fabrieken verborgen in celmembranen
Flavivirussen drijven niet zomaar vrij in de cel tijdens replicatie. Ze herstructureren in plaats daarvan een cellulair membranesysteem dat het endoplasmatisch reticulum (ER) wordt genoemd en vormen gespecialiseerde holtes die replicatie-organellen worden genoemd. Deze lijken op kleine naar binnen gerichte uitsteeksels aan het ER-oppervlak en dienen als beschermde kamers waar virale RNA-genomen worden gekopieerd. Met cryo-elektronentomografie, een techniek die 3D-snapshots maakt van cellen die bliksemsnel in een bijna-natuurlijke toestand zijn ingevroren, visualiseerden de onderzoekers deze uitstulpingen in menselijke longcellen geïnfecteerd met een tekenoverdraagbaar flavivirus verwant aan het tekenencefalitisvirus. Ze ontdekten dat het ER rond geïnfecteerde gebieden opzwelt en vol raakt met clusters van deze replicatie-organellen, waarvan sommige leeg zijn terwijl andere gevuld zijn met dicht, draadvormig RNA.
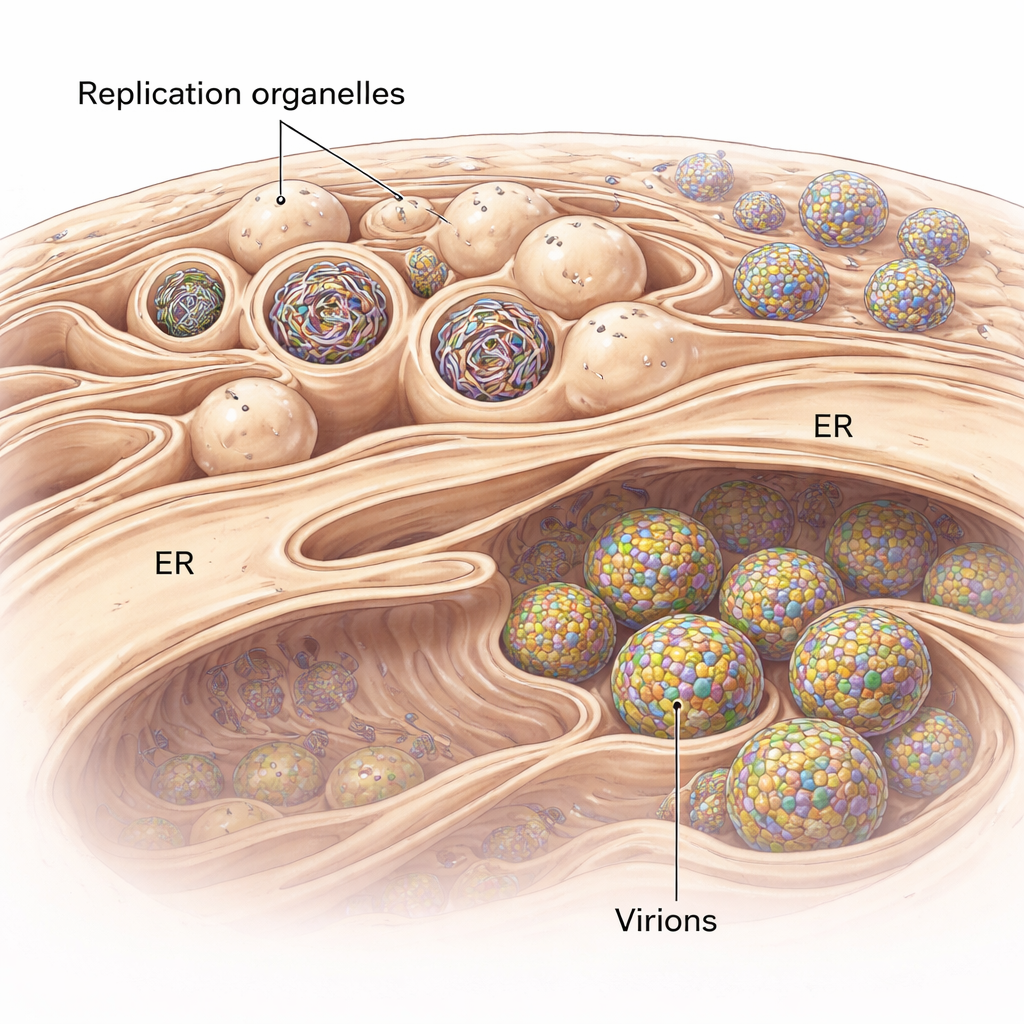
Het perfecte virale belletje bouwen
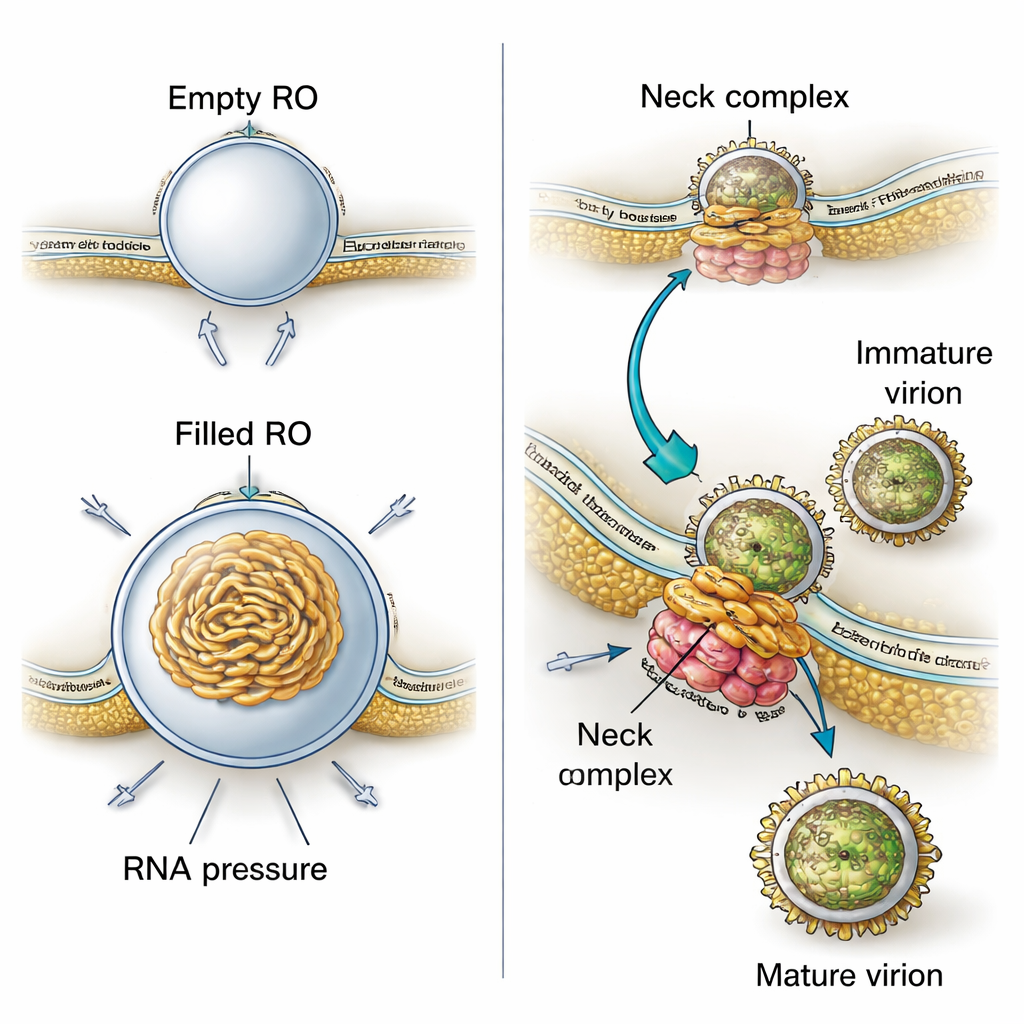
Waarom hebben deze membraanholtes zo’n precieze, knopachtige vorm? Door hun 3D-beelden te combineren met fysische modellering tonen de auteurs aan dat twee krachten samenwerken. Ten eerste is het membraan van de replicatie-organellen consistent dikker dan normaal ER, wat suggereert dat virale eiwitten of gewijzigde lipiden het membraan verstenen en krommen tot een stabiele knop nog voordat er RNA binnenkomt. Ten tweede, wanneer viraal RNA aanwezig is, krult het zich op binnen de holte en duwt naar buiten, waardoor de grootte van de knop toeneemt. Berekeningen gebaseerd op de gemeten afmetingen duiden erop dat elk gevuld organel waarschijnlijk druk bevat die overeenkomt met ongeveer één kopie van het virale genoom in dubbelstrengse vorm. Dit betekent dat het virus zowel een voorgevormd membraan als de fysieke druk van zijn eigen genetisch materiaal gebruikt om zijn miniatuurfabrieken te bouwen en te stabiliseren.
Assemblagelijn: van genoomkopiëren naar nieuwe virussen
De studie onthult ook hoe nauw de virusproductie is verbonden met deze replicatieplaatsen. In hun 3D-weergaven zagen de onderzoekers vaak nieuwe virusdeeltjes ontstaan vlak naast replicatie-organellen, uitpuilend in nabije ER-achtige compartimenten. Immature deeltjes hadden een stekelig oppervlak, terwijl meer rijpe deeltjes er glad uitzagen. Metingen in tomogrammen toonden aan dat immature deeltjes dichter bij de replicatie-organellen liggen dan rijpe, wat impliceert dat deeltjes tijdens hun korte verplaatsing door verweven membraancompartimenten de structurele veranderingen ondergaan die nodig zijn om infectieus te worden. Een grote eiwitassemblage bij de smalle 'nek' waar elke replicatieknop met het cytoplasma verbindt, lijkt het replicatie-organel te verankeren aan een aangrenzend membraan waar budding plaatsvindt. Dit complex fungeert waarschijnlijk als een moleculaire rits die RNA-productie coördineert met het verpakken van dat RNA in nieuwe virusdeeltjes.
Fijnregeling van rijping door één aminozuur
Om te onderzoeken hoe virusrijping wordt geregeld, vergeleek het team twee versies van een chimeer virus die slechts in één aminozuur verschillen op een plek die wordt herkend door een gastheer-enzym genaamd furine. Dit enzym knipt een viraal oppervlakte-eiwit, wat helpt bij de transformatie van immatueel stekelige deeltjes naar gladde, rijpe deeltjes. In in vitro-kleefproeven en in geïnfecteerde cellen werd de variant met arginine op deze positie sneller geknipt dan de variant met glutamine. Wanneer ze in cellen werden gevisualiseerd met cryo-elektronentomografie, produceerde het sneller gekniptende virus een hoger aandeel rijpe deeltjes nabij de replicatie-organellen. Ondanks deze microscopische verschillen vertoonden beide varianten vergelijkbare groeipatronen en ziekteverschijnselen in een muismodel, wat suggereert dat het virus een reeks rijpingsefficiënties kan verdragen terwijl het toch infectieus blijft.
Direct toekijken bij infectie in de hersenen
De meeste structurele virusstudies zijn gebaseerd op cellijnen, maar dit werk reikt tot levende weefsels. De onderzoekers isoleerden een hersenstructuur, het plexus choroideus, uit geïnfecteerde muizen en prepareerden die voor cryo-elektronentomografie met behulp van hogedrukvriezen en gefocusseerd ionenbundelfrezen. Zelfs in deze complexe omgeving observeerden ze dezelfde kenmerkende eigenschappen: clusters van replicatie-organellen, verdikte membranen en nabijgelegen blaasje vol met rijpe virusdeeltjes. Dit toont aan dat het membraanherstructureren en de nauw gekoppelde replicatie–assemblage–rijpingsvolgorde die in gekweekte cellen werd gezien ook in de hersenen plaatsvindt, waar deze virussen ziekte veroorzaken.
Waarom deze verborgen werkstromen ertoe doen
Voor niet-specialisten is de kernboodschap dat deze herseninfecterende virussen een sterk georganiseerde assemblagelijn binnen onze cellen draaien. Ze vormen celmembranen om tot kleine geperforeerde belletjes waarin genome worden gekopieerd, koppelen die belletjes direct aan plekken waar nieuwe deeltjes uitbollen, en beginnen zelfs de laatste rijpingsstappen binnen handbereik van de oorspronkelijke replicatieplaats. Het identificeren van de verdikte replicatiemembranen, het nek-overspannende eiwitcomplex en de nauw verweven rijpingscompartimenten verklaart niet alleen hoe flavivirussen zo efficiënt repliceren, maar wijst ook op nieuwe doelen voor antivirale middelen die de verborgen fabrieken en assemblagesporen van het virus willen verstoren.
Bronvermelding: Dahmane, S., Schexnaydre, E., Zhang, J. et al. Cryo-electron tomography reveals coupled flavivirus replication, budding and maturation. Nat Commun 17, 828 (2026). https://doi.org/10.1038/s41467-026-68483-4
Trefwoorden: flavivirus, cryo-elektronentomografie, replicatie-organellen, virusrijping, door teken overgedragen encefalitis