Clear Sky Science · nl
Spectro-elektrochemisch inzicht in koper-kobalt-katalysatoren voor de co-elektroreductie van CO2 en nitriet naar ureum
Afvalgassen omzetten in meststof
Ureummeststof vormt de ruggengraat van de moderne landbouw, maar de conventionele productie is energie-intensief en levert veel CO2-uitstoot op. Deze studie onderzoekt een heel andere benadering: met elektriciteit kooldioxide (CO2) en stikstofhoudend afval (zoals nitriet uit uitlaatgassen of afvalwater) rechtstreeks omzetten in ureum. Voor de niet-specialist is de aantrekkingskracht duidelijk: een route naar een essentiële meststof die de uitstoot kan verminderen, afvalstromen als grondstof kan gebruiken en mogelijk op termijn door hernieuwbare stroom kan worden aangedreven.
Waarom ureumproductie herbepalen?
Vandaag wordt ureum meestal via een keten gemaakt: eerst wordt ammoniak geproduceerd uit stikstof en fossiel waterstof (het Haber–Bosch-proces), en vervolgens reageert ammoniak met CO2 bij hoge temperatuur en druk. Deze reeks stappen is gecentraliseerd, kapitaalintensief en veroorzaakt bijna een ton CO2 per geproduceerde ton ureum. Naarmate de wereldwijde vraag naar meststoffen groeit, nemen ook de milieukosten toe. Een alternatief is fossiele brandstoffen volledig te omzeilen door de sleutelstappen elektrisch aan te drijven, bij voorkeur met hernieuwbare energie, en door CO2 en stikstofoxiden (NOx) te gebruiken die nu als afval worden behandeld.
Een nieuwe rol voor koper en kobalt
De auteurs ontwerpen dunne-filmkatalysatoren door samen koper (Cu) en kobalt (Co) op koolstofpapier te sputteren, waarbij ze de Cu:Co-verhouding nauwkeurig afstemmen. Ze richten zich op de gelijktijdige elektroreductie van CO2 en nitriet (NO2⁻) in water bij neutrale pH, een omgeving die de gevoelige vorming van koolstof–stikstof (C–N) bindingen kan bevorderen die nodig zijn voor ureum. De opvallende samenstelling is een 1:1-mengsel van Cu en Co, dat een ureumproductiesnelheid bereikt van ongeveer 61 millimol per uur per gram katalysator bij een matige aangelegde spanning. Microscopen en röntgenmetingen tonen aan dat de metalen op atomaire schaal nauw gemengd zijn en tijdens bedrijf grotendeels metallisch blijven, waardoor een robuust platform ontstaat waarop zowel CO2 als nitriet efficiënt kunnen reageren. 
Hoe de katalysator het werk verdeelt
Ureum op deze manier maken is uitdagend omdat eenvoudigere reacties — zoals waterstofvorming of de afzonderlijke reductie van CO2 of nitriet — sterk concurreren. De sleutel, zo vinden de onderzoekers, is een arbeidsverdeling tussen koper- en kobaltsites die samenwerken. Elektrochemische testen tonen dat koper op zichzelf vooral CO2 omzet naar koolstofgebaseerde brandstoffen en chemicaliën, terwijl kobalt op zichzelf vooral nitriet reduceert tot ammoniak, zonder ureum in beide gevallen. Alleen wanneer Cu- en Co-atomen nauw gemengd zijn, ontstaat er aanzienlijke ureumvorming. Spectroscopische ‘momentopnamen’ tijdens de reactie detecteren kenmerkende op het oppervlak gebonden fragmenten: koolstofspecies afgeleid van CO2 (*CO en *COOH) die de voorkeur geven aan koper, en stikstofspecies afgeleid van nitriet (*NH2 en verwante groepen) die de voorkeur geven aan kobalt. Aan de grensvlakken tussen Cu en Co kunnen deze fragmenten elkaar ontmoeten en koppelen om de C–N ruggengraat van ureum te vormen.
De juiste omstandigheden vinden voor bindingvorming
De studie laat zien dat alleen de samenstelling niet voldoende is; de omringende oplossing en membraan moeten ook worden afgestemd. Ureum verschijnt alleen in een neutraal bicarbonaat-elektrolyt, dat genoeg opgelost CO2 beschikbaar houdt en precies de juiste hoeveelheid protonen (waterstofionen) levert om stappen van 'proton-gekoppelde elektronoverdracht' te stimuleren zonder het oppervlak te overstelpen met waterstofontwikkeling. Onder sterk zure of sterk alkalische omstandigheden vormt ureum zich niet of valt het snel uiteen tot eenvoudigere producten. Experimenten met verschillende stikstofbronnen laten zien dat nitriet bijzonder effectief is voor ureumvorming, en beter presteert dan nitraat en hydroxylamine. Langdurige tests tonen aan dat de Cu–Co-films relatief stabiel zijn, met slechts bescheiden metaalverlies en aanhoudende ureumproductie.
Onder de motorkap kijken met theorie
Om te begrijpen waarom deze tandemkatalysator zo goed werkt, wendt het team zich tot computersimulaties op basis van dichtheidsfunctionaaltheorie. Deze berekeningen ondersteunen het idee dat koper de binding van CO2-afgeleide species bevoordeelt, terwijl kobalt nitriet beter activeert en stikstofhoudende fragmenten stabiliseert. De simulaties wijzen op een specifieke stap als de energetische beperkende factor: het koppelen van een *NH2-fragment (van nitriet) met een *COOH-fragment (van CO2) om een tussenproduct te vormen dat soms als *NH2CO wordt genoteerd. Zodra dit stuk aanwezig is, zijn de resterende stappen naar ureum relatief eenvoudig. Het Cu–Co-grensvlak verlaagt de energiekost van deze cruciale koppeling vergeleken met zuiver koper of zuiver kobalt, wat de experimenteel waargenomen toename in ureumopbrengst voor het bimetallische systeem verklaart. 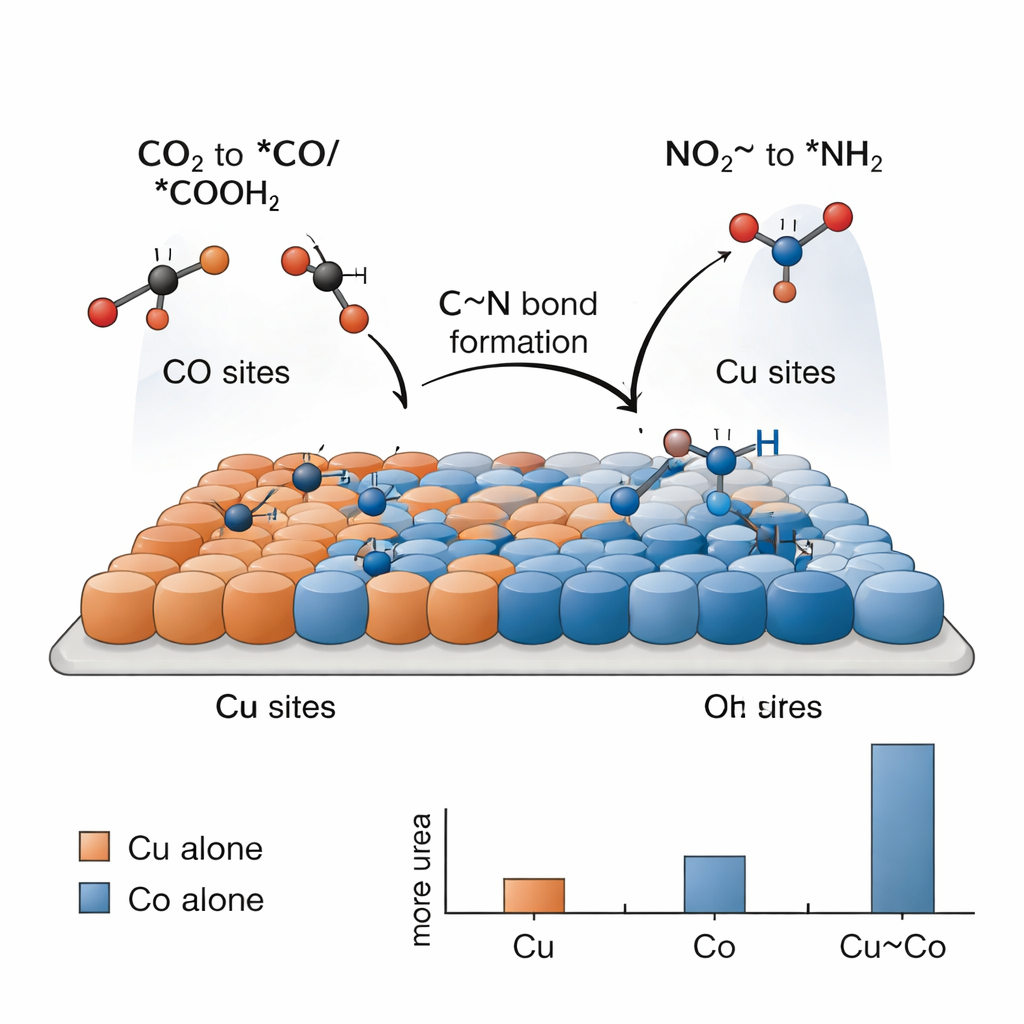
Van labinzichten naar groenere meststof
In praktische zin vervangt dit werk nog niet de huidige gigantische ureumfabrieken, maar het verduidelijkt hoe een toekomstige elektochemische route ontworpen zou kunnen worden. Door aan te tonen dat koper en kobalt in tandem kunnen werken — de één levert geactiveerde koolstofspecies, de ander geactiveerde stikstofspecies, beide onder zorgvuldig gecontroleerde protoncondities — schetst de studie een realistisch pad naar schonere, mogelijk gedecentraliseerde ureumproductie die CO2 en stikstofafval als hulpbronnen in plaats van verontreinigingen benut.
Bronvermelding: Ramadhany, P., Trần-Phú, T., Yuwono, J.A. et al. Spectroelectrochemical insight into copper cobalt catalysts for CO2 and nitrite co-electroreduction to urea. Nat Commun 17, 1776 (2026). https://doi.org/10.1038/s41467-026-68481-6
Trefwoorden: elektrochemische ureumsynthese, koper-kobalt-katalysator, CO2 benutting, nitrietreductie, C–N koppeling