Clear Sky Science · nl
Structurele basis voor selectieve remming van de menselijke GABA‑transporter GAT3
Waarom het dempen van hersensignalen ertoe doet
Onze hersenen functioneren dankzij een subtiel evenwicht tussen signalen die prikkelen en signalen die kalmeren. Een belangrijke kalmerende boodschapper is GABA, een stof die helpt voortijdige overactiviteit te voorkomen die gekoppeld is aan aandoeningen zoals epilepsie, schade door een beroerte en de ziekte van Alzheimer. Deze studie richt zich op een eiwit genaamd GAT3, dat GABA rondom zenuwcellen opruimt. Door op atomair niveau te laten zien hoe een nieuw molecuul zich aan GAT3 hecht en het uitschakelt, bieden de onderzoekers een structurele routekaart voor het ontwerpen van volgende‑generatie geneesmiddelen die het natuurlijke remsysteem van de hersenen zachtjes kunnen versterken.
Het eigen rempedaal van de hersenen
GABA is de belangrijkste remmende, of kalmerende, neurotransmitter in het centrale zenuwstelsel. Nadat GABA vrijkomt uit zenuwuiteinden, moet het snel worden verwijderd zodat hersencircuits zich kunnen herstellen. Die opruiming wordt uitgevoerd door transportereiwitten die GABA terugpompen in cellen. Twee van deze transporters domineren in de hersenen: GAT1, voornamelijk op neuronen aangetroffen, en GAT3, aanwezig op ondersteunende cellen die astrocyten worden genoemd. Hoewel een GAT1‑blokkerend geneesmiddel (tiagabine) al decennia wordt gebruikt bij de behandeling van epilepsie, zijn vergelijkbare middelen die GAT3 targeten achtergebleven. GAT3 is echter bijzonder interessant omdat het GABA‑niveaus buiten synapsen reguleert en langdurige, achtergrondremming vormgeeft die de hersenactiviteit fijnmazig kan bijstellen. 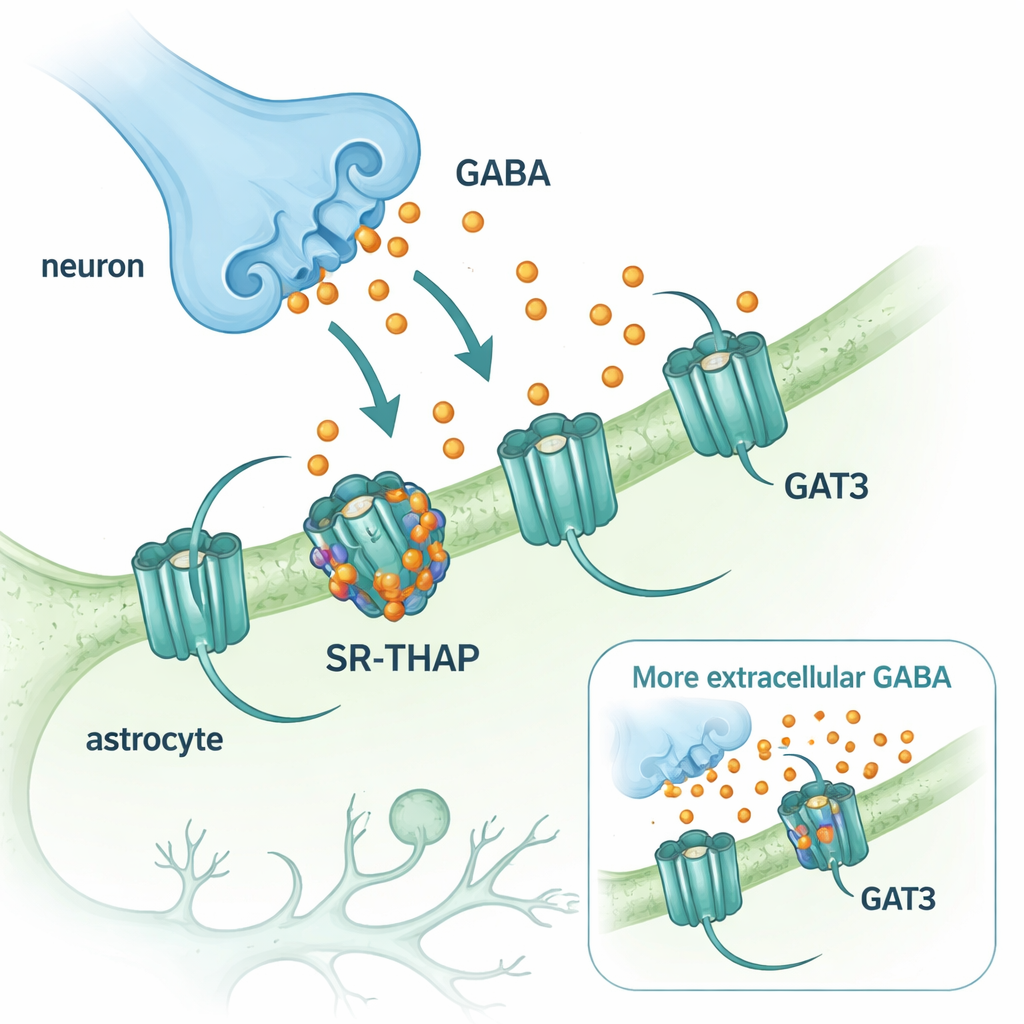
Het ontwerpen van een preciezer moleculair slot
Pogingen om GAT3 te remmen werden belemmerd door een gebrek aan gedetailleerde structurele informatie. Veel vorige verbindingen ontstonden door trial‑and‑error, vaak door volumineuze varianten te maken van bekende GABA‑achtige moleculen. Een van de bekendste, (S)‑SNAP‑5114, bleek chemisch onstabiel en lastig te gebruiken in levende dieren. Voortbouwend op een stabieler verwant van deze verbinding ontwikkelden de auteurs SR‑THAP, een nieuw klein molecuul dat is ontworpen om beter in GAT3 te passen en bestand te zijn tegen afbraak. Experimenten in humane celculturen toonden aan dat SR‑THAP GAT3 sterk blokkeert en dat op een niet‑competitieve manier: in plaats van simpelweg met GABA te concurreren op de gebruikelijke plaats, verandert het hoe de transporter werkt en verlaagt het de maximale transportcapaciteit.
GAT3 zien op bijna‑atomaire resolutie
Om precies te begrijpen hoe SR‑THAP werkt, gebruikte het team cryo‑elektronenmicroscopie, een techniek die flash‑bevroren eiwitten met elektronen afbeeldt en hun driedimensionale vorm reconstrueert. Ze losten drie vormen van menselijke GAT3 op: gebonden aan SR‑THAP, gebonden aan GABA en in een substraaatvrije toestand. Alle drie tonen de typische architectuur die wordt gezien bij verwante neurotransmittertransporters: 12 dicht opeengepakte helices die het membraan doorspannen en een centraal pad vormen voor GABA en de bijbehorende ionen, natrium en chloride. In de GABA‑gebonden structuur bevindt de transporter zich in een “inward‑occluded” toestand—GABA en een natriumion zijn geklemd in het midden, afgesloten van zowel buiten als binnen. Een sleutelaromaatzuur vormt een gespecialiseerde interactie met de aminogroep van GABA, wat helpt verklaren hoe GAT3 zijn substraat herkent.
Hoe SR‑THAP de transporter openzet
In scherp contrast vangt de SR‑THAP‑gebonden structuur GAT3 in een “inward‑open” toestand, waarbij de interne zijde van het eiwit naar het celinterieur openligt. SR‑THAP ligt diep in deze binnenste holte geklemd, geschoven tussen meerdere helices die normaal bewegen tijdens de transportcyclus. Het bezet drie kleine pocketjes met verschillende chemische eigenschappen en maakt deel uit van een netwerk van waterstofbruggen en hydrofobe contacten. Deze positionering blokkeert de transporter zodanig dat GABA en ionen hun reis niet meer kunnen voltooien. De auteurs tonen aan dat een paar specifieke aminozuren die deze holte bekleden verschillen tussen GAT3 en zijn naaste verwanten; het verwisselen van een van deze residuen verandert zowel de transportactiviteit als de werkzaamheid van SR‑THAP, wat helpt verklaren waarom de remmer veel selectiever is voor GAT3 dan voor GAT1 of verwante transporters. 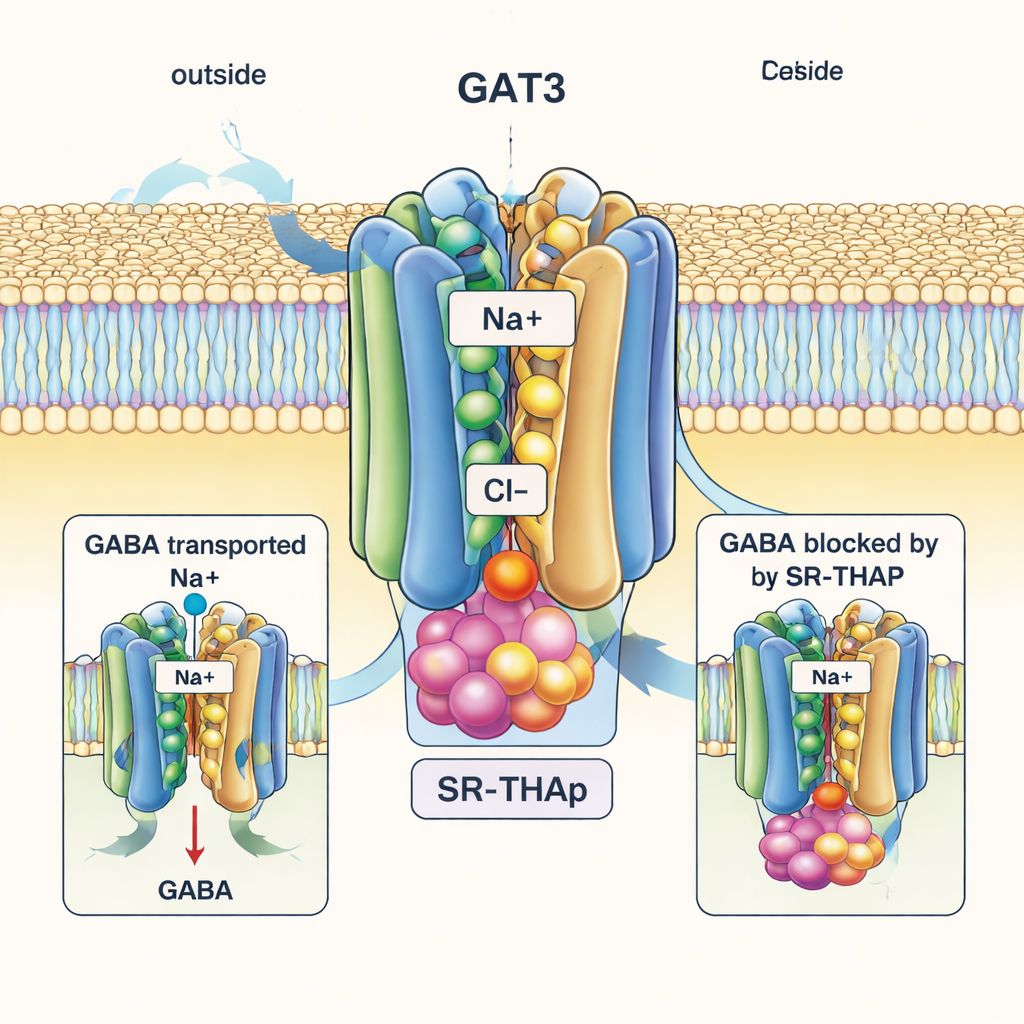
Deuren openen naar nieuwe geneesmiddelen voor epilepsie en hersengezondheid
Samen onthullen deze structuren hoe GAT3 wisselt tussen verschillende vormen om GABA te verplaatsen, en hoe SR‑THAP een minder geconserveerd binnenste pocket benut om die cyclus vast te zetten. Voor niet‑specialisten is de belangrijkste conclusie dat de studie een gedetailleerd moleculair blauwdruk levert om GAT3 op een hoog selectieve manier uit te schakelen. Zulke verbindingen zouden de kalmerende GABA‑niveaus op een fijner afgestemde manier kunnen verhogen dan bestaande medicijnen, en mogelijk leiden tot nieuwe behandelingen of onderzoekstools voor epilepsie, herstel na beroerte, de ziekte van Alzheimer en andere aandoeningen waarin remmende signalering verstoord is.
Bronvermelding: Mortensen, J.S., Bavo, F., Jensen, M.H. et al. Structural basis for selective inhibition of human GABA transporter GAT3. Nat Commun 17, 1774 (2026). https://doi.org/10.1038/s41467-026-68479-0
Trefwoorden: GABA‑transporter, GAT3, epilepsie, cryo‑EM, remming van neurotransmitters