Clear Sky Science · nl
Een stochastisch mechanisme stuurt snelle substraattranslocatie in het AAA+-apparaat ClpB
Hoe cellulaire machines eiwitten in beweging houden
In elke cel trekken, duwen en hervormen kleine moleculaire machines voortdurend eiwitten om te voorkomen dat ze klonteren en om schade te herstellen. Eén zo’n machine, ClpB genaamd, helpt bij het redden van verwarde eiwitten—een essentiële taak voor het overleven van de cel onder stress. Deze studie stelt een eenvoudige maar fundamentele vraag: hoe zet ClpB de chemische brandstof ATP om in het mechanische werk van het doortrekken van een eiwitketen door zijn centrale pore, en gebeurt dat in nette, klokwerkachtige stappen of op een meer willekeurige, diffusieve wijze?
Een reddingsring voor eiwitten in actie
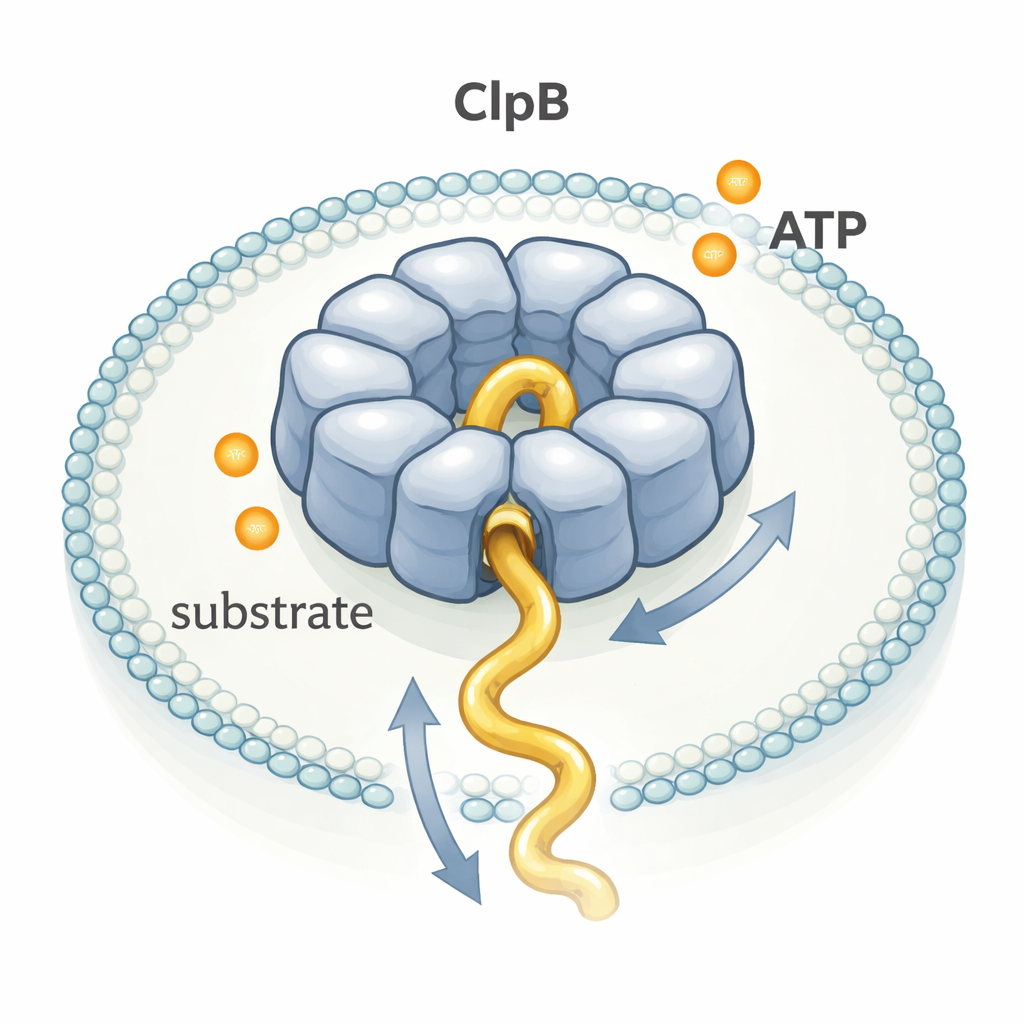
ClpB behoort tot een grote familie enzymen, de zogenaamde AAA+-machines, die zich vormen tot ringvormige structuren met een centrale tunnel. Veel van deze structuren zijn tot in detail afgebeeld met cryo-elektronenmicroscopie, wat heeft geleid tot het populaire "hand-over-hand"-model: elke verbruikte ATP zou een kleine, precieze stap aandrijven, zoals een team mensen dat opeenvolgend aan een touw trekt. Andere experimenten wezen er echter op dat ClpB eiwitten veel sneller zou kunnen verplaatsen dan de trage ATP-verbruikssnelheid lijkt toe te staan. Om dit raadsel op te lossen, volgden de auteurs individuele ClpB-moleculen in realtime terwijl ze een flexibel testeiwit, κ-caseïne, door hun pore trokken.
Één molecuul tegelijk bekijken
De onderzoekers vingen afzonderlijke ClpB-ringen en individuele κ-caseïne-moleculen samen in kleine lipidebelletjes die aan een glasoppervlak waren gehecht. Ze bevestigden fluorescente kleurstoffen op specifieke punten van ClpB en op de eiwitketen, en gebruikten vervolgens single-molecule FRET, een methode die afstandsveranderingen tussen kleurstoffen op nanometerschaal rapporteert. Wanneer κ-caseïne in de ClpB-pore schoof, kwamen de kleurstoffen dicht bij elkaar en schoot de FRET-waarde omhoog als een korte piek; wanneer de keten eruit gleed, zakte het signaal weer. Door de duur en hoogte van duizenden van dergelijke pieken te meten, konden ze afleiden hoe snel en hoe ver segmenten van het eiwit door de pore werden geleid.
Snel, zwak aangedreven en bijna temperatuur-onafhankelijk
Verrassend genoeg waren de translocatiegebeurtenissen extreem snel: het gelabelde segment van κ-caseïne doorliep doorgaans enkele nanometers van de pore in ongeveer 1–2 milliseconde—ongeveer duizendmaal sneller dan de gemiddelde tijd tussen ATP-hydrolysegebeurtenissen in ClpB. De meeste gebeurtenissen waren zo kort, en ze volgden een brede, machtswetachtige distributie in plaats van één kenmerkende tijdschaal. Het wijzigen van de temperatuur van 10 naar 32 °C vertraagde deze bewegingen nauwelijks, wat impliceert dat de energiedrempel voor beweging klein is vergeleken met die van klassieke "power-stroke"-motoren zoals kinesine. Evenzo verminderde het verlagen van de ATP-concentratie sterk hoe vaak gebeurtenissen plaatsvonden, maar had het bijna geen effect op hoe lang iedere gebeurtenis duurde. ATP regelde, met andere woorden, wanneer ClpB zich aanschakelde en hoe vaak het handelde, meer dan de snelheid van individuele threading-uitbarstingen.
Voor- en achterwaartse beweging met een voorwaartse bias
Om te zien of ketens altijd in één richting bewogen, voerde het team complexere drie-kleur FRET-experimenten uit, waarbij beide uiteinden van de pore en het substraat werden gekleurd. Hierdoor konden ze onderscheiden of κ-caseïne van boven of onder de ring binnentrad en of het helemaal doorging of terugtrok. Ze ontdekten zes verschillende patronen: volledige voorwaartse en achterwaartse threading, langere "gedeeltelijke" bezoeken waarbij de keten beide uiteinden van de pore beproefde voordat hij vertrok, en vluchtige ontmoetingen dicht bij slechts één uiteinde. Ongeveer driekwart van de volledige gebeurtenissen ging in de voorwaartse richting, maar een aanzienlijk deel ging achterwaarts, wat onthult dat ClpB bidirectionele diffusie van zijn substraat toestaat met slechts een bescheiden voorwaartse voorkeur. Wanneer ATP werd vervangen door een langzaam gehydrolyseerd analoog, werden gebeurtenissen zeldzaam en veel langzamer, en verdween de voorwaartse voorkeur vrijwel helemaal.
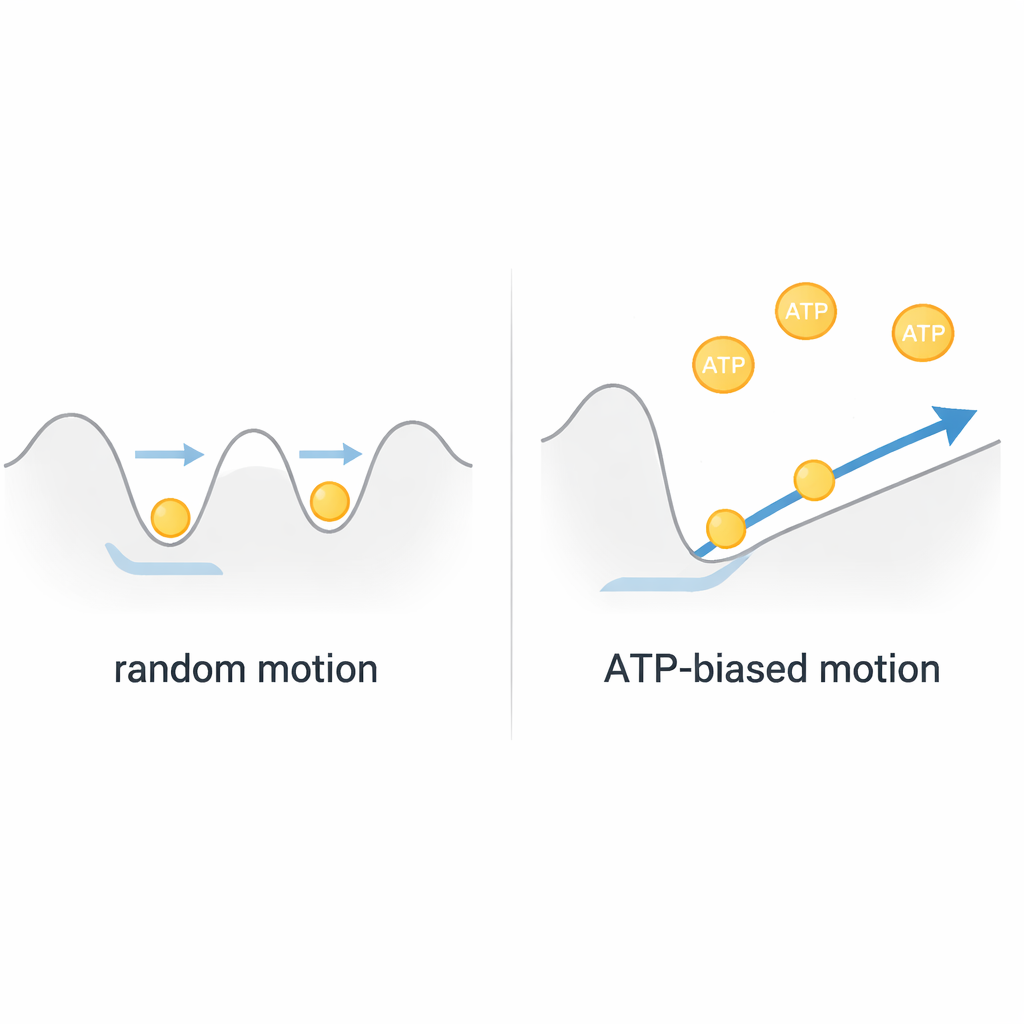
Een Brownse motor, geen eenvoudige lier
Als men deze observaties samenvoegt, concluderen de auteurs dat ClpB meer werkt als een Brownse motor dan als een starre, brandstofgedreven lier. De eiwitketen trilt thermisch binnen een ondiep energielandschap in de pore en beweegt snel heen en weer. ATP levert niet rechtstreeks krachtige, discrete trekkrachten; in plaats daarvan vormt het via snelle bewegingen van interne "pore loops" de vorm van dit landschap, waardoor beweging subtiel in één richting wordt bevoordeeld. Omdat elke volledige threading-gebeurtenis correleert met slechts ongeveer één of twee verbruikte ATP-moleculen, bereikt ClpB opmerkelijk efficiënte, snelle transporten door willekeurige beweging te rectificeren in plaats van ertegen te vechten. Dit beeld verandert onze kijk op veel AAA+-machines en suggereert dat biologische nanomotoren vaak die willekeur benutten in plaats van haar uit te sluiten.
Bronvermelding: Casier, R., Levy, D., Riven, I. et al. A stochastic mechanism drives fast substrate translocation in the AAA+ machine ClpB. Nat Commun 17, 1773 (2026). https://doi.org/10.1038/s41467-026-68478-1
Trefwoorden: eiwittranslocatie, AAA+-machine, Brownse motor, moleculaire chaperonne, single-molecule FRET