Clear Sky Science · nl
Structuur van een Brochothrix thermosphacta-bacteriofaag onthult mechanisme van celwandadsorptie bij Gram-positieve infecterende sifofagen
Virussen die ons voedsel vers houden
Door bacteriën dodende virussen, bacteriofagen genoemd, vormen stilletjes onze gezondheid en voedselvoorziening. Sommige veroorzaken dodelijke infecties, maar andere kunnen worden benut om voedselgerelateerde ziektekiemen en bederf te bestrijden. Deze studie onthult, met opvallende atomaire details, hoe zo’n virus, genoemd NF5, zich hecht aan en de taaie buitenlaag van een vleesbederfbacterie doorboort. Inzicht in deze microscopische strijd kan ons helpen veiligere methoden te ontwerpen om voedsel te bewaren en antibioticum‑resistente bacteriën te bestrijden.
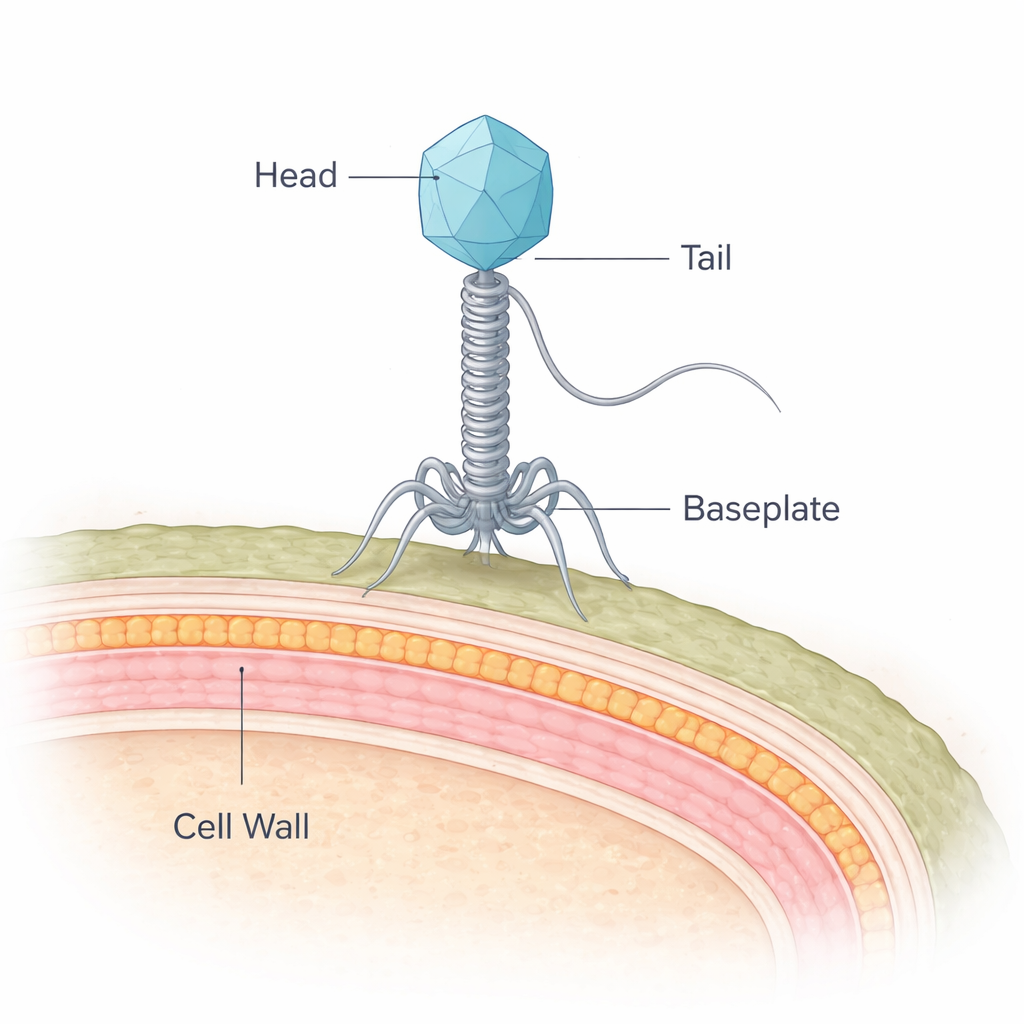
Een vleesbederver ontmoet zijn natuurlijke vijand
De bacterie in het middelpunt van dit werk, Brochothrix thermosphacta, is een veelvoorkomende oorzaak van de onaangename geuren en slijmvorming op gekoeld vlees. NF5 is een virus dat deze bacterie infecteert en behoort tot een groep die sifofagen wordt genoemd; zij dragen hun DNA in een eiwitmantel en leveren dit via een lange, flexibele staart af. Terwijl wetenschappers de structuren van veel virussen die zogenaamde Gram-negatieve bacteriën infecteren uitgebreid in kaart hebben gebracht, zijn die die Gram-positieven zoals B. thermosphacta aanvallen veel minder begrepen. Gram-positieve bacteriën vormen een speciale puzzel omdat ze beschermd worden door een dikke, meerlagige celwand in plaats van een dunne wand en buitenmembraan.
Een moleculaire spuit bouwen, atoom voor atoom
Met state-of-the-art kryo-elektronenmicroscopie vroren de onderzoekers miljoenen NF5-deeltjes in en reconstrueerden hun driedimensionale structuur op bijna atomair niveau. Ze identificeerden 11 verschillende virale eiwitten die samen de kop, nek, staartbuis en een ingewikkelde baseplaat aan de staartpunt vormen, in totaal 643 eiwitketens. De kop vormt een stevige icosaëdrische schaal rond het virale DNA, terwijl een 135-nanometer lange staart naar beneden uitstrekt als een flexibele spuit. Ringen van herhaalde eiwitten vormen een holle staartbuis waarvan het binnenoppervlak sterk negatief geladen is—een rangschikking die waarschijnlijk helpt het virus zijn DNA snel in de gastheer te schieten.
De slimme boor aan de staartpunt
Het meest ingewikkelde deel van NF5 is de baseplaat, een meerlaagse structuur die tegelijk fungeert als sensor, boor en anker. Dicht bij het centrum bevindt zich een “maatstaf”-eiwit dat de staartbuis vult en een aan de staart gekoppelde lysine die de buis afsluit totdat de infectie begint. Rond deze kern zitten eiwitten die het bacterieoppervlak herkennen en vastgrijpen. Sommige werken als veerachtige armen die dramatisch kunnen buigen en zo helpen de baseplaat te kantelen en vervolgens in een positie loodrecht op de celwand te klikken. Andere lijken op vezels die in verwante virussen voorkomen en zouden specifieke moleculen in de dikke Gram-positieve wand kunnen binden en zelfs delen van het suiker‑rijke netwerk van de celwand kunnen afknabbelen. Intrigerend genoeg lijkt één zijvezel-eiwit van NF5 functies te combineren die bij andere Gram-positieve virussen over meerdere eiwitten zijn verdeeld, wat wijst op een efficiënt, evolutionair gestroomlijnd ontwerp.
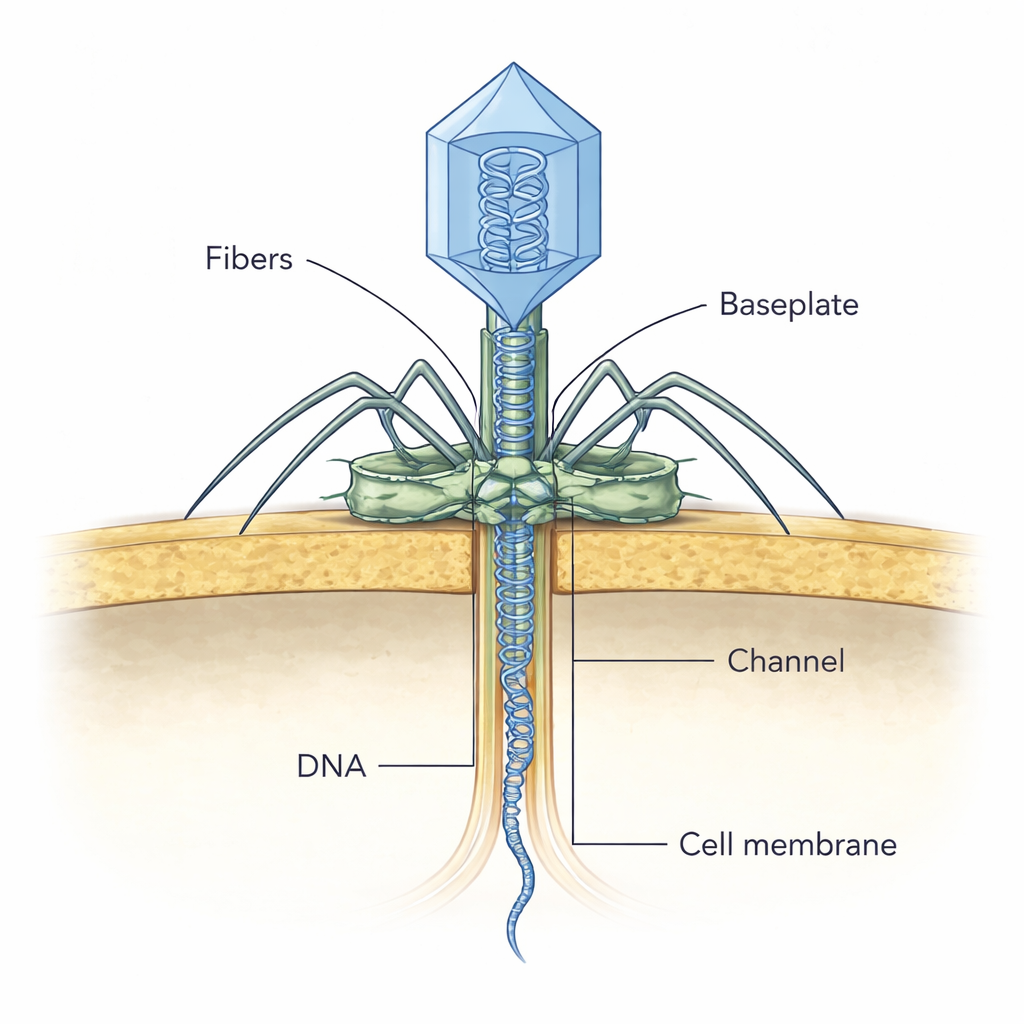
Een virus op heterdaad betrapt
Om te zien hoe deze onderdelen samenwerken tijdens infectie, gebruikte het team kryo-elektronentomografie op dunne plakjes van geïnfecteerde bacteriën. Ze legden NF5-deeltjes vast in verschillende ogenschijnlijke stadia van de aanval. In vroege beelden hecht het virus zich onder een hoek aan de celwand, waarschijnlijk met behulp van zijn buitenste vezels om geschikte receptoren te vinden. Later richt de baseplaat zich loodrecht op het celoppervlak en lijkt de aangehechte viruskop nog vol DNA. In volgende stadia vervaagt de inhoud van de kop naarmate het DNA vrijkomt, en verschijnt er een dunne, kanaalachtige dichtheid die de bacteriewand overspant richting het celmembraan. De auteurs stellen voor dat zodra het enzym aan de staartpunt de celwand aanraakt en afbreekt, het zich herschikt, de plug opent en het maatstaf‑eiwit naar buiten schuift en zo deze tijdelijke tunnel vormt waardoor het virale DNA veilig in de cel kan reizen.
Waarom dit verder reikt dan één virus
Door NF5 te vergelijken met virussen die andere bacteriën infecteren, laten de onderzoekers zien dat belangrijke staart- en baseplaat-eiwitten zich anders hebben ontwikkeld in Gram-positieve versus Gram-negatieve fagen om om te gaan met de zeer verschillende oppervlaktearchitecturen van hun gastheren. Deze structurele aanpassingen—extra domeinen, langere armen of gecombineerde functies in enkele eiwitten—lijken fijn afgestemde aanpassingen te zijn aan dikkere, complexere celwanden. Het werk levert een gedetailleerd bouwplan van hoe een virus een taaie bacteriële barrière kan herkennen, zich eraan hechten en die kan doorboren, en biedt een basis voor het ontwerpen van fagen of faag-geïnspireerde hulpmiddelen om bederf van voedsel beter te beheersen en mogelijk schadelijke Gram-positieve pathogenen aan te pakken.
Bronvermelding: Peng, Y., Pang, H., Zheng, J. et al. Structure of a Brochothrix thermosphacta bacteriophage reveals cell wall adsorption mechanism in Gram-positive infecting siphophages. Nat Commun 17, 1772 (2026). https://doi.org/10.1038/s41467-026-68477-2
Trefwoorden: structuur van bacteriofaag, Gram-positieve bacteriën, kryo-elektronenmicroscopie, bestrijding van bederf van levensmiddelen, faaginfectiemechanisme