Clear Sky Science · nl
Identificatie van thermotolerante niet-canonische PAMs voor robuuste éénpot CRISPR-Cas12a-detectie
De temperatuur opvoeren voor DNA-tests
Snelle, nauwkeurige tests voor infecties en genetische veranderingen zijn cruciaal voor de geneeskunde, maar de huidige DNA-tests vereisen vaak geavanceerde labapparatuur en kunnen zeldzame of subtiele doelen missen. Deze studie laat zien dat het simpelweg iets warmer draaien van een CRISPR-gebaseerde test veel meer bruikbare DNA-"handvatten" ontsluit, waardoor eentube-diagnostiek sneller, gevoeliger wordt en zelfs enkel-letterverschillen in de genetische code kan onderscheiden. 
Waarom CRISPR een postcode nodig heeft
CRISPR-gereedschappen zoals Cas12a richten zich op specifieke DNA-streken, geleid door een kort RNA dat als zoekstring fungeert. Maar ze kunnen alleen binden en actief worden als een nabijgelegen vierletterig label, een zogeheten PAM, de juiste sequentie heeft—traditioneel een beperkte set die begint met “TTT”. Dat is vergelijkbaar met het nodig hebben van een huisnummer voordat je een brief kunt bezorgen: ontbreekt het juiste nummer, dan komt het bericht niet aan. Deze PAM-eis beperkt de plekken waar CRISPR kan zoeken, wat problematisch is als clinici specifieke mutaties, resistentiemarkers of virusvarianten moeten opsporen die niet naast die klassieke tags liggen.
Nieuwe “deuren” ontdekken bij hogere temperaturen
De onderzoekers testten systematisch alle 256 mogelijke vierletterige PAM-combinaties om te onderzoeken hoe goed ze Cas12a’s "collateral" knipactiviteit aandrijven—het vermogen om veel nabije DNA-stukjes te verscheuren zodra het doel is gevonden, wat de basis vormt voor CRISPR-diagnostische signalen. Bij normale lichaamstemperatuur (37 °C) presteerden slechts enkele niet-standaard PAMs even goed als de klassieke. Maar toen ze de reactietemperatuur verhoogden tot ongeveer 45 °C, gebeurde er iets opvallends: 82 verschillende niet-canonische PAMs gaven plots sterke signaal-knipactiviteit, vergelijkbaar met de standaardtags. Het team vermoedt dat extra warmte de lokale DNA-structuur losser maakt en het Cas12a-complex flexibeler, waardoor de drempel voor herkenning van deze eerder "zwakke" PAMs daalt.
Sterk signaal, zacht voor het sjabloon
Cas12a kent twee knipmodi. In de "cis"-modus knipt het het specifieke DNA dat het moest vinden; in de "trans"-modus, eenmaal geactiveerd, versnelt het het afbreken van nabijgelegen signaaldraagstrengen, wat de test doet oplichten. De onderzoekers vonden dat bij hogere temperaturen niet-canonische PAMs zeer sterke trans-knipactiviteit gaven—ideaal voor een helder, snel signaal—terwijl cis-knippen van het hoofd-DNA relatief zwak bleef. Die combinatie is perfect voor eentube-tests, waarbij DNA eerst moet worden versterkt zonder te worden vernietigd. Ze toonden ook aan dat Cas12a bij deze warmere instellingen veel kieskeuriger wordt ten aanzien van mismatches tussen het gids-RNA en het doel: zelfs een enkele verkeerde letter kan het signaal uitschakelen, vooral bij gebruik van niet-canonische PAMs. 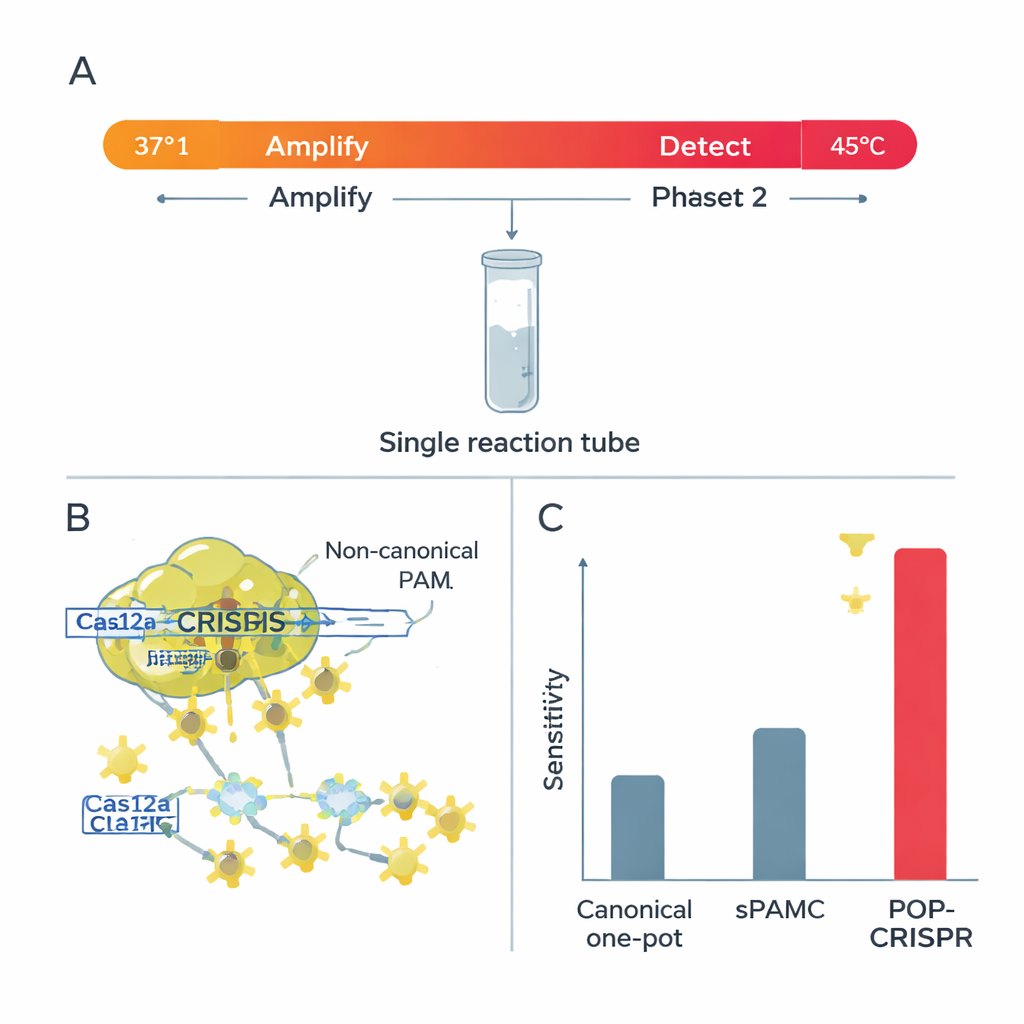
Een slimmer eentube-test: POP-CRISPR
Voortbouwend op deze inzichten ontwikkelde het team POP-CRISPR, een "poikilothermische" (variabele temperatuur) eentube-assay. De reactie begint rond 37 °C, waar een isotherme amplificatiemethode stilletjes het doel-DNA of RNA vermenigvuldigt terwijl Cas12a relatief inactief is. Na ongeveer 10 minuten wordt het mengsel verwarmd tot circa 45 °C, een zoete plek waar Cas12a—nu gericht op niet-canonische PAM-sites—krachtige trans-knipactiviteit activeert en een sterk fluorescent signaal genereert. Dit eenvoudige tweestappen-temperatuurprogramma verbeterde de detectiegevoeligheid ongeveer tienvoudig vergeleken met eerdere eentube-CRISPR-methoden die ook zwakkere PAMs gebruikten, en overtrof duidelijk conventionele eentube-formaten met canonische PAMs.
Van labbank naar patiënt binnen enkele minuten
Het POP-CRISPR-systeem werd getest op echte klinische monsters. Het detecteerde human papillomavirus (HPV-16) in vaginale uitstrijkjes en Mycoplasma pneumoniae in ademhalingsuitstrijkjes met hoge gevoeligheid, inclusief zeer laagniveau "grijze zone"-gevallen die standaardmethoden uitdagen. Cruciaal is dat POP-CRISPR resistente Mycoplasma-stammen kon onderscheiden die een enkel-letterverandering in een ribosomaal gen dragen, ook al lag er geen klassieke PAM nabij die mutatie—een taak die veel bestaande Cas12a-tests frustreert. Om de aanpak veldvriendelijk te maken, combineerden de auteurs een snelle twee minuten durende hitte- en Chelex-lyse stap (zonder volledige DNA-extractie) met een handzaam fluorescentie-leesapparaat dat door een smartphone wordt aangestuurd. Samen kan deze workflow een rauw uitstrijkje in ongeveer 20 minuten omzetten in een digitale ja/nee-uitkomst.
Wat dit betekent voor alledaagse tests
Door de reactietemperatuur te verhogen en een veel groter aantal PAM-"deuren" te benutten, verandert dit werk Cas12a in een flexibeler en preciezer sensor. POP-CRISPR levert snellere, gevoeliger en specifieker nucleïnezuurdetectie in één afgesloten buis, en breidt bovendien het bereik van genetische sites uit die kunnen worden gericht—including enkel-basemutaties geassocieerd met medicijnresistentie of kanker. Voor patiënten kan dat vertaald worden naar snellere diagnostiek ter plaatse en beter afgestemde behandelingen; voor onderzoekers en testontwikkelaars biedt het een krachtige nieuwe manier om CRISPR-diagnostiek te ontwerpen die zowel robuuster als scherper is.
Bronvermelding: Tian, T., Zhang, T., Zhang, W. et al. Identification of thermotolerant non-canonical PAMs for robust one-pot CRISPR-Cas12a detection. Nat Commun 17, 1771 (2026). https://doi.org/10.1038/s41467-026-68476-3
Trefwoorden: CRISPR-diagnostiek, Cas12a, PAM-sites, point-of-care testen, nucleïnezuurdetectie