Clear Sky Science · nl
Structurele mechanismen voor remming en activatie van het menselijke klein‑geleidings Ca2+‑geactiveerde kaliumkanaal SK2
Waarom kleine kaliumkanalen ertoe doen
Elke gedachte die u heeft en elke hartslag die u voelt berust op elektrische signalen in uw cellen. Die signalen worden gevormd door microscopische poriën, ionkanalen genoemd, die geladen deeltjes laten stromen. Eén familie daarvan, de klein‑geleidings calciumgeactiveerde kaliumkanalen (SK‑kanalen), helpt te regelen hoe zenuwcellen vuren en hoe het hart zijn ritme behoudt. Dit artikel onthult, tot op atomaire nauwkeurigheid, hoe verschillende geneesmiddelen en een bijengif één belangrijk lid van deze familie — het menselijke SK2‑kanaal — kunnen afsluiten of versterken. Die inzichten kunnen richting geven aan nieuwe behandelingen voor aandoeningen variërend van boezemfibrilleren tot tremor en geheugenstoornissen.
Hoe SK2‑kanalen als cellulaire remmen werken
SK2‑kanalen zitten in het celmembraan en fungeren als kleine remmen op elektrische activiteit. Wanneer het binnenste van een cel tijdens een elektrisch signaal kort met calciumionen gevuld raakt, merkt een hulpstofje genaamd calmoduline deze stijging op. Calmoduline is aan de binnenzijde van SK2 bevestigd en zodra het calcium bindt, trekt het aan een deel van het kanaal als een trekkoord, waardoor een poort opengaat die kaliumionen naar buiten laat stromen. Die uitgaande stroom helpt de cel tot rust te brengen nadat ze vuur heeft gegeven, en bepaalt hoe vaak neuronen signalen kunnen sturen en hoe betrouwbaar hartcellen slaan. Omdat SK1–3‑kanalen wijdverspreid zijn in hersenen en hart, en SK2 een bijzonder belangrijke subtype is, is het cruciaal voor het ontwerp van gerichte geneesmiddelen om precies te begrijpen hoe ze openen, sluiten en op stoffen reageren.
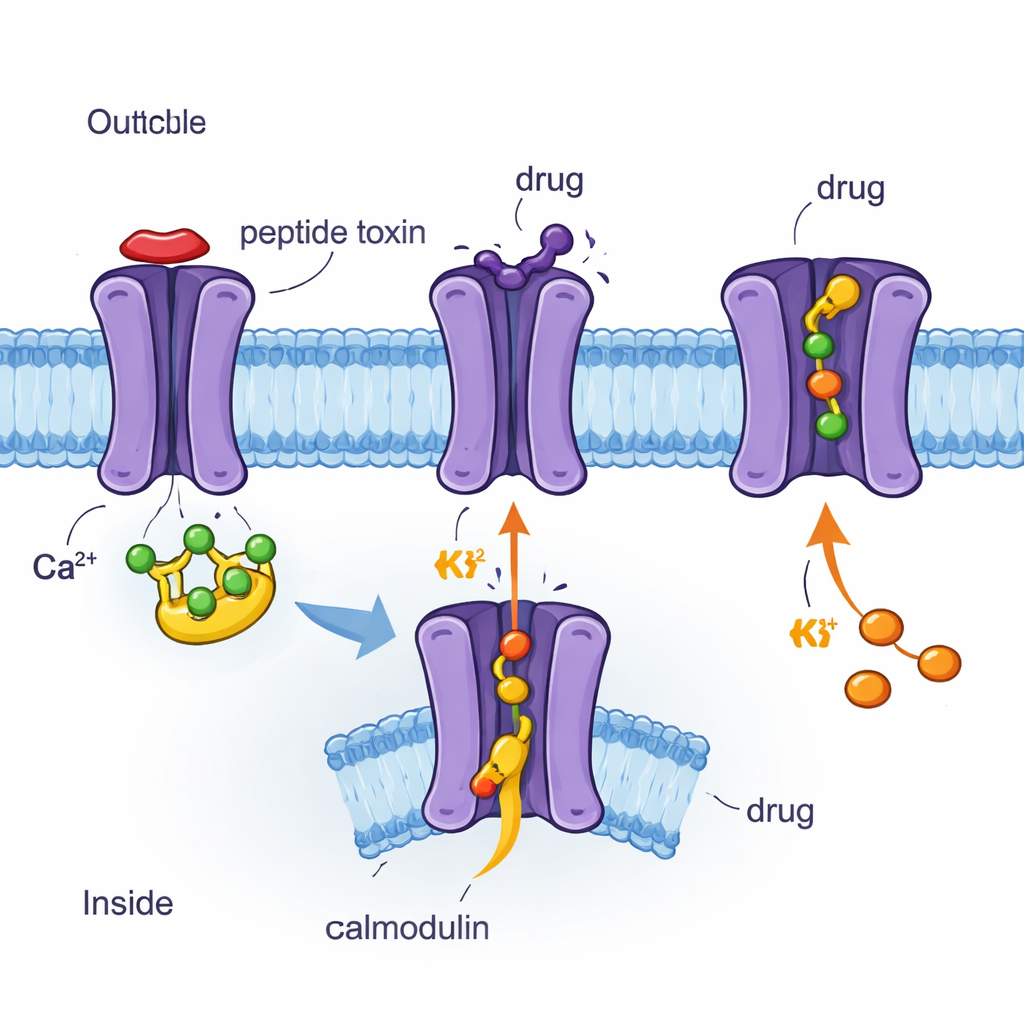
Met cryo‑EM kanalen en middelen atoom voor atoom in kaart brengen
De auteurs gebruikten cryo‑elektronenmicroscopie (cryo‑EM), een techniek die geflash‑vroren eiwitten afbeeldt met bijna atomische resolutie, om vier driedimensionale structuren vast te leggen van het menselijke SK2‑kanaal gebonden aan calmoduline en verschillende moleculen. Daartoe behoorden het bijengifpeptide apamin, de synthetische blokker UCL1684, de klinische remmer AP30663 en de klinische activator CAD‑1883. Alle vier structuren tonen SK2 als een viervoudige assemblage die het membraan doorkruist, met calmoduline aan de binnenzijde bevestigd. Vergelijking van deze momentopnamen onthulde welke delen van het kanaal star zijn, welke flexibel, en hoe calmoduline beweegt wanneer het kanaal in een gesloten of open staat verkeert. De onderzoekers combineerden deze beelden ook met elektrische metingen in cellen en testten hoe specifieke aminozuurveranderingen de reactie van het kanaal op elk middel veranderen.
Een bijengif en een labmiddel die de buitenmond afsluiten
Apamin, een klein peptide uit bijengif, staat al lang bekend als een buitengewoon krachtige en selectieve SK2‑remmer die in onderzoek wordt gebruikt. De nieuwe structuren laten zien dat apamin zich gedraagt als een kurk op de buitenmond van de SK2‑pore. Het nestelt zich in een bekerachtige vestibule gevormd door een korte lus tussen twee helices (de S3–S4‑linker) die bij SK2 goed geordend is maar bij een verwant kanaal, SK4, slapper, wat verklaart waarom SK4 ongevoelig is voor apamin. Belangrijke positief geladen residuen op apamin reiken tussen vier aromatische zijgroepen van het kanaal en vormen sterke elektrostatische en stapelingsinteracties die het kaliumpad volledig afsluiten. UCL1684, een synthetische bis‑quinoliniumverbinding, neemt in wezen dezelfde buitenste pocket in en blokkeert ook de ionuitgang, maar door zijn kleinere omvang kan het dieper zitten en de positie van apamins kritieke positieve ladingen nabootsen. Mutaties in kanaalresiduen die deze vestibule vormen verminderen de gevoeligheid voor apamin sterk en, in mindere mate, voor UCL1684, wat bevestigt dat deze gevormde buitenlus een belangrijke bepalende factor is voor werking van toxine en geneesmiddel.
Een centrale stop en een interne wig die de activiteit afstemmen
Daarentegen bindt de klinische kandidaat AP30663 in de centrale holte van SK2, net onder het selectiviteitsfilter dat kaliumionen selecteert. Daar fungeert het als een fysieke stop, geklemd tussen specifieke zijgroepen die de pore bekleden. Wijzigingen in deze bekledende residuen verzwakken het vermogen van AP30663 om SK2 te remmen, en sequentievergelijkingen verklaren waarom verwante analogen SK1–3 van SK4 kunnen onderscheiden. CAD‑1883, een positieve modulator ontwikkeld voor bewegingsstoornissen, gebruikt weer een andere strategie. Het schuift in een pocket op het grensvlak tussen de N‑lob van calmoduline en een korte linker (S4–S5) die de beweging van calmoduline aan de poort van het kanaal koppelt. Door de contacten in deze pocket te versterken, lijmt CAD‑1883 als het ware calmoduline en SK2 in een configuratie die de binnenpoort opent en de pore verwijdt. Structurele vergelijkingen tonen aan dat deze door CAD‑1883 gebonden toestand lijkt op een volledig open kanaal, hoewel het selectiviteitsfilter na langdurig openen mogelijk een geïnactiveerde vorm kan aannemen.
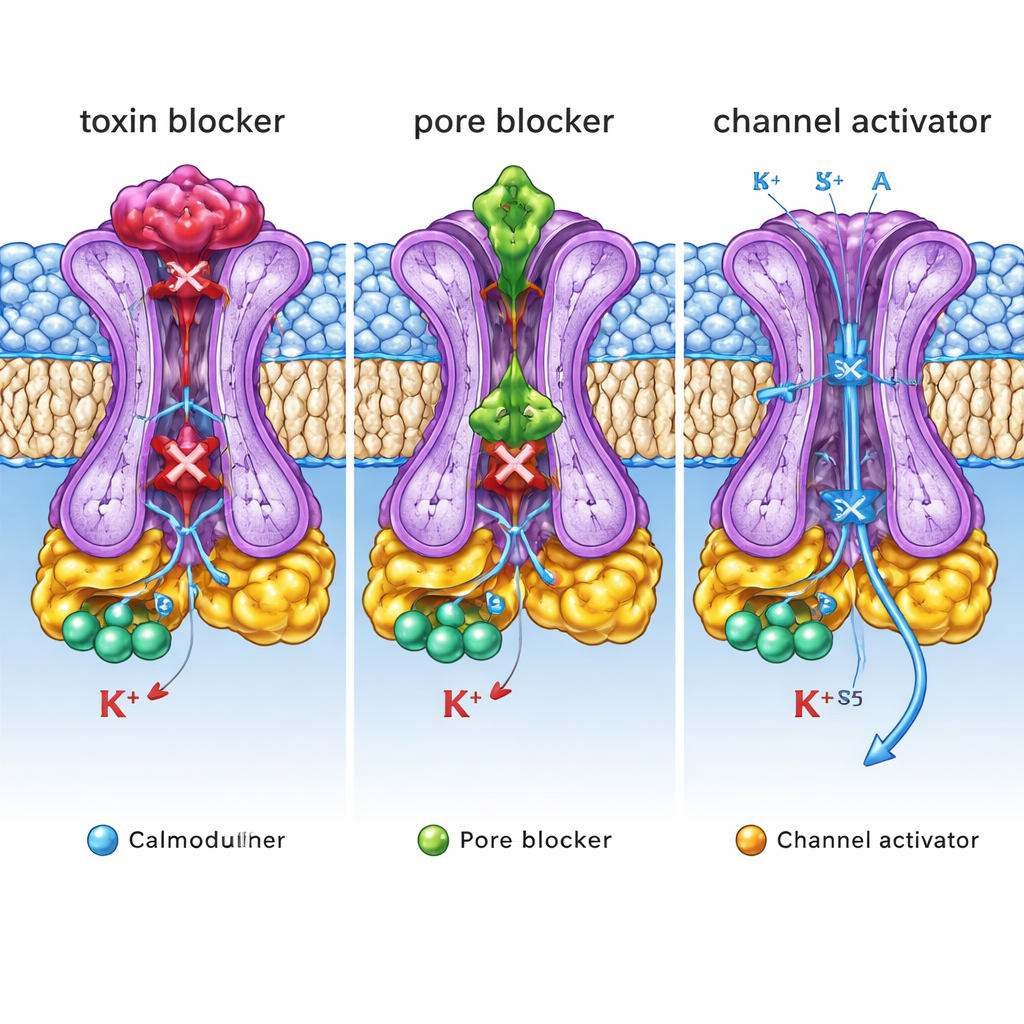
Wat deze structurele blauwdrukken betekenen voor de geneeskunde
Samen onthullen deze structuren drie verschillende “bedieningsknoppen” op één SK2‑kanaal: een buitenste deksel waar toxines en sommige blokkers zitten, een interne poreholte waar andere remmers de stroom blokkeren, en een zij‑pocket waar activatoren de opening stabiliseren. Voor de niet‑specialist is de kernboodschap dat hetzelfde ionkanaal omhoog of omlaag kan worden bijgesteld door geneesmiddelen die heel verschillende structurele handvatten grijpen. Door deze handvatten atomair in kaart te brengen en ze te koppelen aan functionele effecten, biedt dit werk een gedetailleerde blauwdruk voor het ontwerpen van volgende‑generatie moleculen die selectief SK2‑activiteit dempen of versterken. Zulke op maat gemaakte middelen zouden op een dag kunnen helpen abnormale hersenritmes te normaliseren, tremoren te verlichten of onregelmatige hartslagen te corrigeren met minder bijwerkingen.
Bronvermelding: Ma, B., Wu, D., Cao, E. et al. Structural mechanisms for inhibition and activation of human small-conductance Ca2+-activated potassium channel SK2. Nat Commun 17, 1770 (2026). https://doi.org/10.1038/s41467-026-68475-4
Trefwoorden: SK2‑kaliumkanalen, calciumgeactiveerde kanalen, cryo‑EM‑structuren, ionkanaalmodulatoren, boezemfibrilleren en tremor