Clear Sky Science · nl
Belemmerde migratie en deling van stamcellen bij Duchenne-spierdystrofie onthuld door live-imaging
Waarom dit spierverhaal ertoe doet
Duchenne-spierdystrofie (DMD) is een dodelijke kinderziekte die geleidelijk spieren vernietigt. Decennialang richtte het meeste onderzoek zich op de grote spiervezels die bij DMD afbreken. Deze studie laat zien dat er een tweede, stillere speler in de problemen is: de spierseigen stamcellen die normaal schade herstellen. Door deze cellen levend te filmen in muisspieren en op afzonderlijke vezels, tonen de auteurs hoe stamcellen bij DMD de weg kwijtraken, wat nieuwe ideeën oplevert voor behandelingen die spieren effectiever zouden kunnen laten regenereren.
De ingebouwde reparatieploeg van de spier
Rond elke skeletspiervezel bevinden zich een paar residentiële stamcellen, bekend als spier-satellietcellen. In gezonde spier zijn deze cellen meestal in rust. Bij verwonding worden ze actief, delen ze zich en vormen ze ofwel nieuwe stamcellen om de reserve aan te vullen, of gespecialiseerde cellen die in beschadigde vezels fuseren. Deze zorgvuldige balans tussen zelfvernieuwing en differentiatie houdt spierweefsel levenslang sterk. Bij DMD scheuren de spiervezels echter herhaaldelijk omdat ze dystrofine missen, een cruciaal structureel eiwit, wat de vraag oproept of de reparatieploeg zelf uitgeput of verkeerd gestuurd raakt.
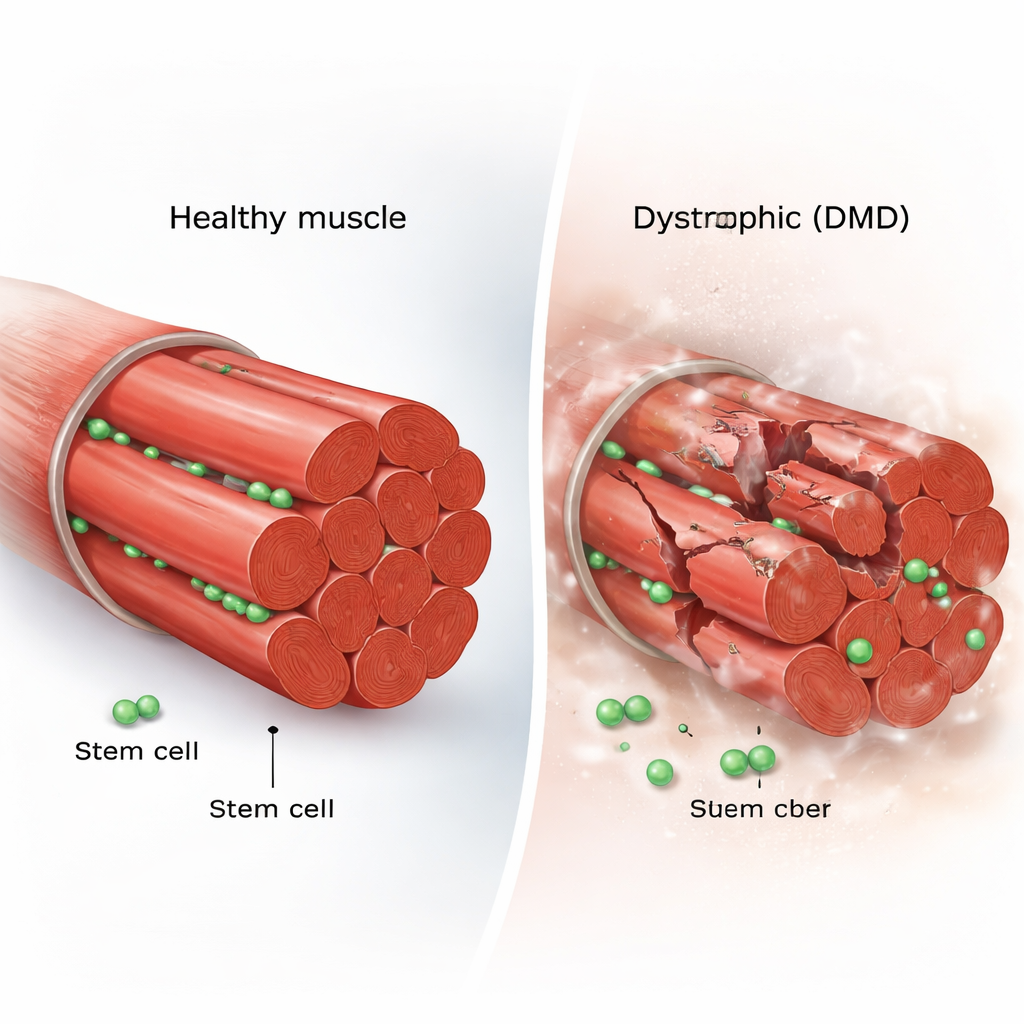
Stamcellen in actie filmen
Om dit te onderzoeken gebruikten de onderzoekers de mdx-muis, een standaardmodel voor DMD, en maakten ze de spierstamcellen fluorescerend onder de microscoop. Ze voerden vervolgens intravitale beeldvorming uit, een techniek waarmee men levende cellen in een onder anesthesie gebracht dier urenlang kan filmen. Daarnaast ontwikkelden ze een aangepast “microwell”-systeem om enkele spiervezels in cultuur te houden terwijl ze elke stamceldeling en -beweging volgden. Deze dubbele aanpak stelde hen in staat individuele cellen te volgen vanaf rustige rust tot herhaalde delingen, migraties en uiteindelijk fusie in nieuw spierweefsel, en gedrag vast te leggen dat statische beelden gemakkelijk zouden missen.
Wanneer reparatiecellen haasten en struikelen
In beschadigde gezonde spieren verlengden afstammende myogene cellen zich en kropen langs vezels met relatief rechte, gerichte paden, delend en zich efficiënt verspreidend. Daarentegen werden dystrofische (mdx) cellen vaak rond en traag. Ze bewogen langzamer en minder doelgericht, en een merkbaar deel bleef vrijwel onbeweeglijk. Het team vond ook dat mdx-cellen eerder dan normaal in nieuwe spiervezels fuseerden, en veel dochtercellen samen migreerden in plaats van na deling uit elkaar te gaan. Al met al toonden mdx-spieren tekenen van “vroegtijdige differentiatie”: stamcellen haastten zich tot spiercellen en vezelvorming in plaats van een robuuste reserve voor voortdurende reparatie te behouden.
Onevenwichtige celdelingen en een verwarde omgeving
Op geïsoleerde vezels konden de onderzoekers classificeren hoe elke stamcel zich deelde. In gezonde spieren waren de meeste delingen symmetrisch maar gebalanceerd—veel leverden twee prolifereerde dochters die de reparatiepool konden blijven uitbreiden, en minder leverden twee terminaal gedifferentieerde cellen. Asymmetrische splitsingen, waarbij één dochter een stamcel bleef en de andere zich toelegde op reparatie, kwamen relatief weinig voor maar wel voor. In mdx-spieren verschoof het patroon sterk: symmetrische delingen leken meer tweedelige differentiërende cellen op te leveren, met veel minder delingen die twee vernieuwende cellen voortbrachten. Cross-grafting-experimenten, waarbij gezonde stamcellen op dystrofische vezels werden geplaatst en omgekeerd, lieten zien dat migratiedefecten grotendeels werden bepaald door de beschadigde vezelomgeving, terwijl het te differentiëren gedrag van mdx-stamcellen de cellen zelf volgde, mede gevormd door hun inflammatoire geschiedenis.
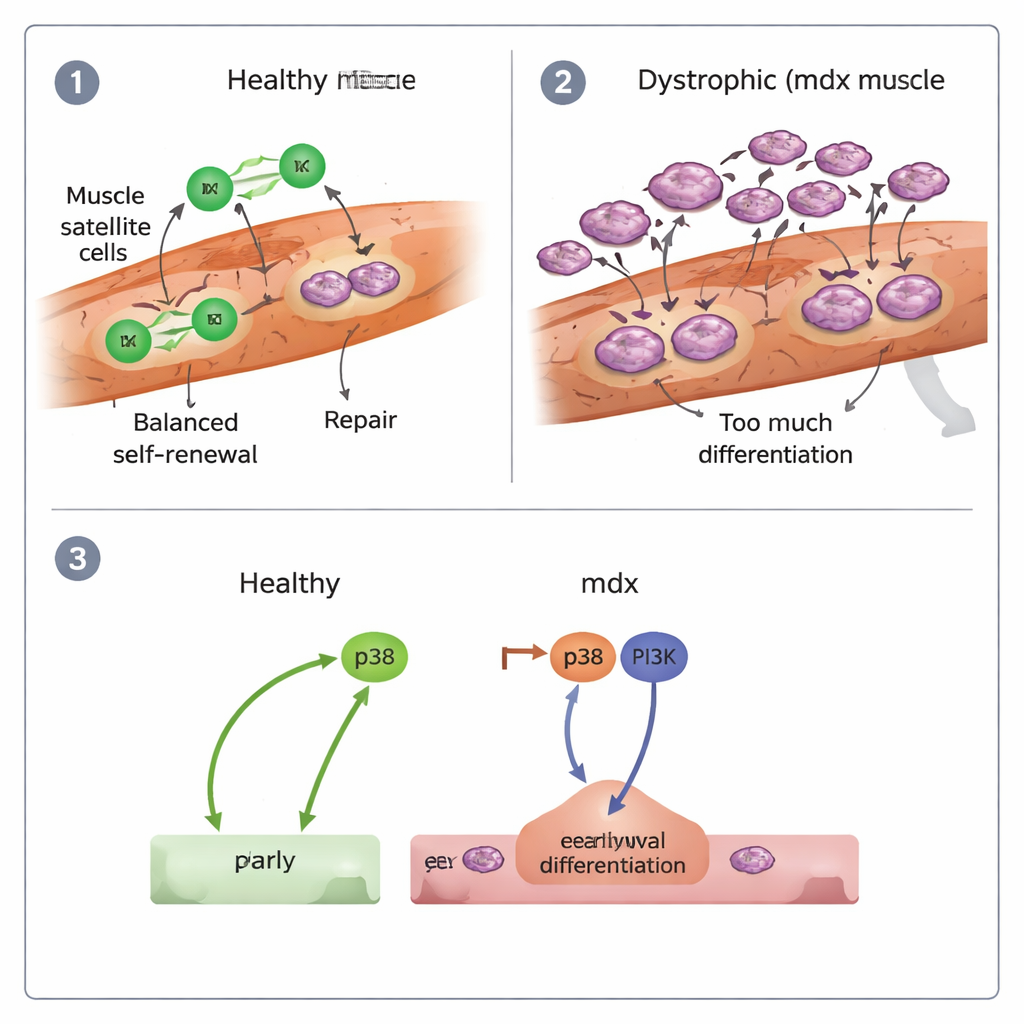
Verkeerd bedrade signalen en wat het voor therapie betekent
De auteurs onderzochten ook de moleculaire schakelaars die stamcellen naar differentiatie duwen. Ze richtten zich op twee signaleringsroutes, bekend als p38 en PI3K. In gezonde cellen reduceerde blokkering van p38 de differentiatie sterk, terwijl remming van PI3K weinig effect had. In mdx-cellen moesten echter beide paden samen worden geblokkeerd om de overmatige haast naar specialisatie te temperen, en zelfs dan bleef hun vermogen om te blijven prolifereren zwak. Dit suggereert dat DMD-stamcellen door gecombineerde p38- en PI3K-activiteit in een „vroege uitputting” terechtkomen, wat bijdraagt aan regeneratie die snel begint maar niet vol te houden is.
Een nieuw beeld van Duchenne: ook een stamcelziekte
Voor een lezer zonder vakkennis is de kernboodschap dat DMD niet alleen een probleem is van fragiele spiervezels; het is ook een probleem van het reparatiesysteem dat ze moet herstellen. In dystrofische spier bewegen stamcellen minder efficiënt, delen ze op een manier die de reserve uitput, en reageren ze abnormaal op sleutelgroeisignalen. Door te onderscheiden welke aspecten worden veroorzaakt door de beschadigde spieromgeving en welke ingebakken zijn in de veranderde staat van de stamcellen, suggereert dit werk nieuwe strategieën: therapieën die p38- en PI3K-signaalgeving temperen, evenwichtige celdelingen herstellen of de lokale niche verbeteren, zouden kunnen helpen spierweefsel effectiever op te bouwen en de voordelen van gen- of celgebaseerde behandelingen voor mensen met Duchenne-spierdystrofie te verlengen.
Bronvermelding: Sarde, L., Letort, G., Varet, H. et al. Impaired stem cell migration and divisions in Duchenne muscular dystrophy revealed by live imaging. Nat Commun 17, 1769 (2026). https://doi.org/10.1038/s41467-026-68474-5
Trefwoorden: Duchenne-spierdystrofie, spierstamcellen, celmigratie, deling van stamcellen, regeneratieve geneeskunde