Clear Sky Science · nl
Split-base-editingsystemen die door coiled-coil heterodimeren worden bijeengehouden maken flexibele en robuuste nucleotide-substituties mogelijk
DNA herstellen met minder bijwerkingen
Veel ziekten worden veroorzaakt door kleine typefouten in ons DNA—fouten van één letter die levensbedreigende gevolgen kunnen hebben. Wetenschappers beschikken over krachtige instrumenten, base-editors genoemd, die deze typefouten kunnen corrigeren zonder het DNA te knippen, maar die instrumenten zijn omvangrijk en moeilijk veilig in het lichaam af te leveren. Dit artikel introduceert een nieuwe manier om base-editors op te splitsen in kleinere, slimmere onderdelen die nog steeds even goed werken als—of soms beter dan—het origineel, en zo nieuwe wegen openen voor de behandeling van genetische aandoeningen in de lever, spieren en daarbuiten.
Waarom grootte een probleem is voor DNA-reparatiegereedschap
Base-editors combineren onderdelen van het CRISPR-systeem met enzymen die een DNA-letter in een andere kunnen omzetten, zoals A naar G of C naar T. Deze precieze omzettingen zijn veelbelovend voor de behandeling van aandoeningen zoals hoge cholesterol of spierdystrofie. Een toonaangevende aflevermethode voor gentherapie, het adeno-geassocieerde virus (AAV), kan echter maar ongeveer 4,7 duizend DNA-letters bevatten, terwijl standaard base-editors groter zijn dan dat. Eerder werk probeerde deze editors te splitsen met speciale eiwit-"scharen" genaamd inteïnen, of door ze te verkleinen met miniatuurenzymen, maar die benaderingen verminderden vaak de efficiëntie, maakten het ontwerp complexer of beperkten waar in het genoom de hulpmiddelen werkten.
Molair klittenband gebruiken om de editor weer op te bouwen
Om dit op te lossen, ontwierpen de onderzoekers een "gesplitste" base-editor die bijeengehouden wordt door kleine coiled-coil heterodimeren—als een stukje moleculair klittenband. Ze verdeelden de base-editor in twee delen: één met de DNA-richtende Cas9-nickase en het andere met het bewerkende enzym. Korte coiled-coil-peptiden op elk halfrond zoeken elkaar op en klikken in elkaar wanneer beide helften hetzelfde DNA-stuk bereiken. Dit creëert coiled-coil base-editors (CC‑BEs), inclusief typen die C bewerken (CC‑CBE), A (CC‑ABE), en complexere varianten die verschillende soorten letterveranderingen kunnen maken. 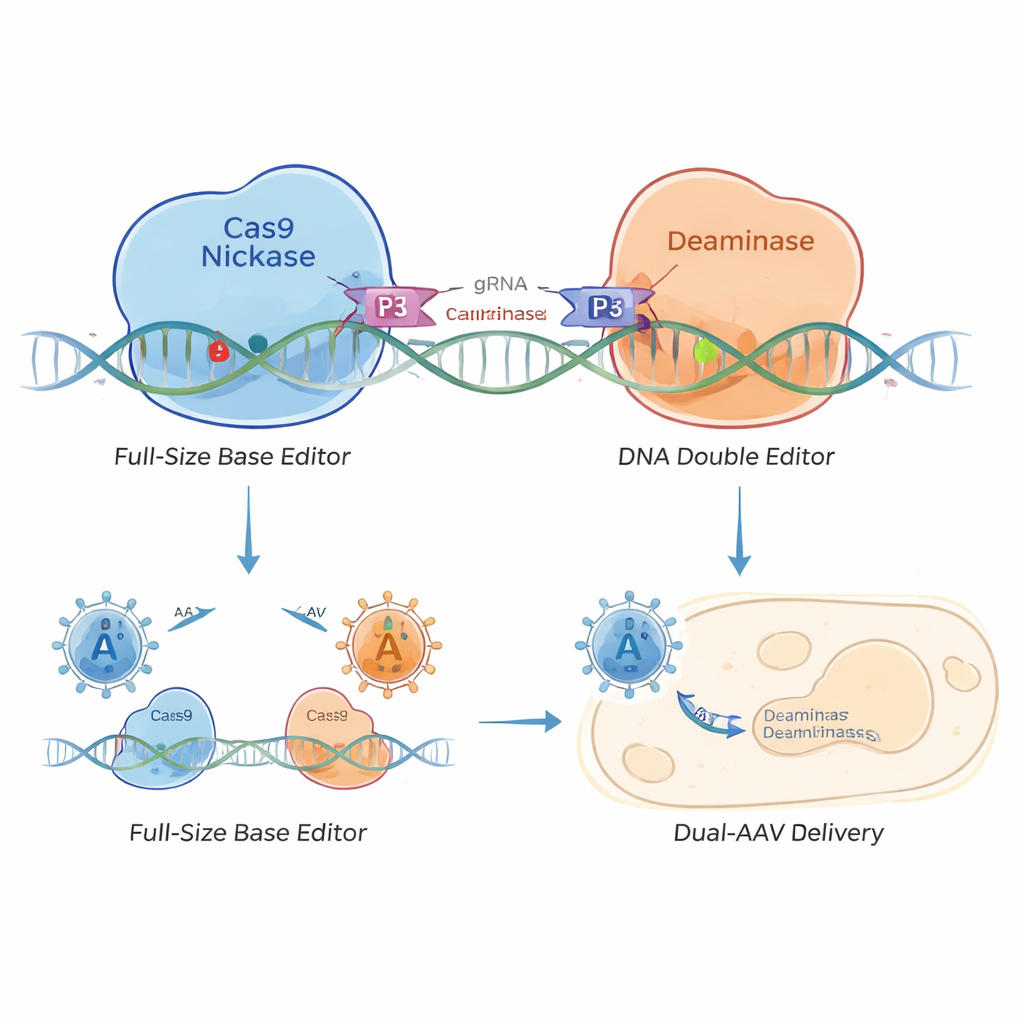
Flexibel, krachtig en nauwkeurig bewerken
Het team testte CC‑BEs in meerdere celtypes, waaronder humane cellen en primaire varkenscellen, en met verschillende vormen van Cas9 die een bredere reeks DNA-sequenties herkennen. De CC‑CBE-versies werkten niet alleen betrouwbaar op veel locaties, maar toonden ook een breder "bewerkingsvenster", wat betekent dat ze doelletters over een grotere stretch DNA konden veranderen, waardoor onderzoekers meer flexibiliteit hebben bij het kiezen van guide-RNA's. De CC‑ABE-versies bereikten vergelijkbare efficiëntie als de beste bestaande adenine-editors en produceerden daarbij vaak minder bijproducten op off-target locaties. De onderzoekers pasten de coiled-coilstrategie ook toe op nieuwere editorontwerpen—zoals compacte TadCBE en precieze ABE9—en vonden opnieuw dat het splitsen van de hulpmiddelen met coiled-coil-paren de prestaties behoudt of verbetert.
Van kweekschalen naar levende muizen
Cruciaal toonden de auteurs aan dat deze gesplitste editors werken in levende dieren met behulp van dual‑AAV-levering, waarbij elk virusdeeltje de helft van de editor draagt. In muizen bereikte een CC‑ABE gericht op het Pcsk9-gen in de lever A‑naar‑G-bewerkingen met percentages tot ongeveer 70%, wat het Pcsk9-eiwit en het LDL-cholesterol in het bloed sterk verlaagde zonder tekenen van leverbeschadiging. 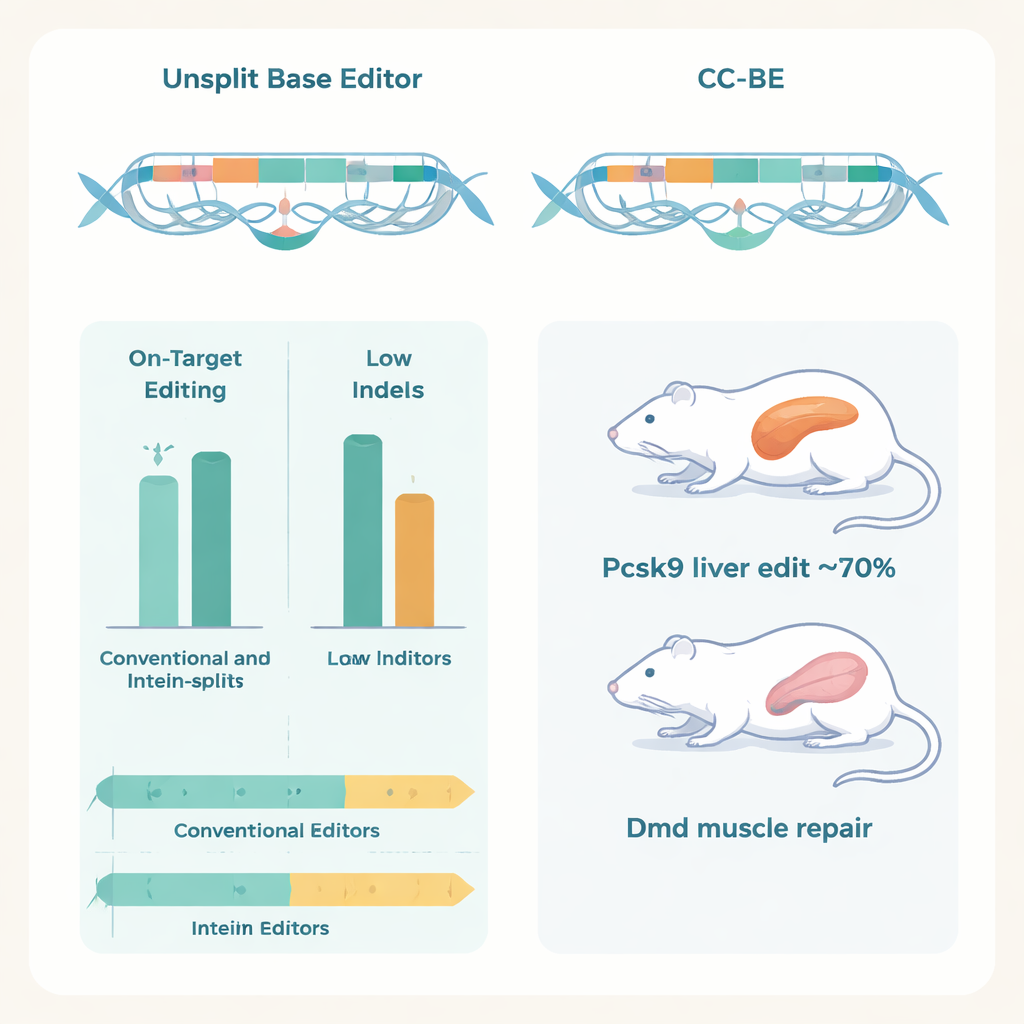
Een nieuwe weg naar praktische DNA-reparatie
In wezen presenteert deze studie een eenvoudige maar krachtige engineeringtruc: gebruik kleine coiled-coil "haakjes" om grote base-editors op te splitsen in AAV-formaat modules die alleen opzetten waar ze nodig zijn. Voor niet-experts is de kernboodschap dat wetenschappers nu zeer capabele DNA-reparatie-instrumenten kunnen verpakken in klinisch bewezen virusdragers zonder nauwkeurigheid of kracht in te leveren. Deze coiled-coil-aanpak kan het eenvoudiger maken om behandelingen te ontwerpen voor een breed scala aan single-letter genetische aandoeningen in organen zoals lever, hart en spier, en brengt fijn afgestemde gencorrectie een stap dichter bij therapieën in de echte wereld.
Bronvermelding: Mu, S., Li, Q., Chen, M. et al. Coiled-coil heterodimer-mediated split base editing systems enable flexible and robust nucleotide substitutions. Nat Commun 17, 1765 (2026). https://doi.org/10.1038/s41467-026-68469-2
Trefwoorden: base-bewerking, gentherapie, CRISPR, AAV-levering, genetische aandoening