Clear Sky Science · nl
In vivo CRISPR-screening identificeert SAGA-complexleden als belangrijke regulatoren van hematopoëse
Waarom het belangrijk is dat de bloedproductie in balans blijft
Elke dag maakt je lichaam stilletjes honderden miljarden nieuwe bloedcellen aan die zuurstof vervoeren, infecties bestrijden en bloedingen stoppen. Deze voortdurende productie hangt af van zeldzame "moedercellen" in het beenmerg, de bloedvormende stamcellen. Wanneer de regeling van deze cellen misgaat, kunnen mensen bloedarmoede, verzwakte immuniteit of kanker zoals leukemie krijgen. Deze studie stelt een eenvoudige maar krachtige vraag: van de duizenden genen in ons genoom, welke zijn werkelijk essentieel om de aanmaak van bloedcellen gezond en in balans te houden?
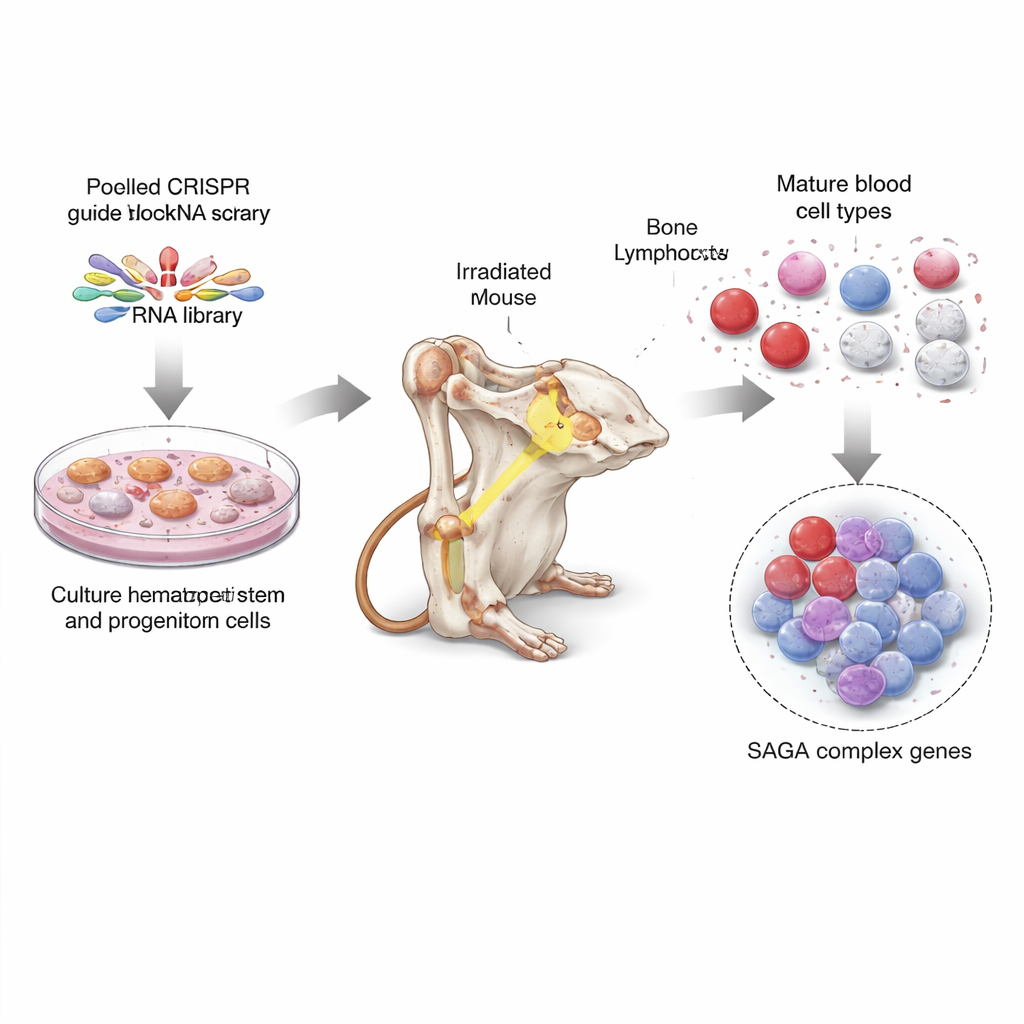
Een genoomwijde schatzoektocht in muizenstamcellen
Om dit aan te pakken gebruikten de onderzoekers CRISPR, het genbewerkingsinstrument dat vaak wordt vergeleken met moleculaire scharen, om bijna elk gen in het muizengenoom uit te schakelen, met tien gidsen per gen. Eerst kweekten ze grote aantallen beenmergstam- en progenitorcellen onder speciale kweekomstandigheden en infecteerden deze cellen vervolgens met gevoteerde CRISPR-gidsen zodat elke cel een knockout van een ander gen droeg. Daarna transplantkeerden ze deze gemengde, bewerkte cellen in tientallen bestraalde muizen, zodat de bewerkte cellen de bloedstelsels van de dieren konden herbouwen. Maanden later zuiverden ze diverse rijpe bloedceltypen en stamcelachtige cellen uit het beenmerg en bepaalden welke CRISPR-gidsen over- of ondervertegenwoordigd waren. Dit onthulde welke genverliezen onrijpe cellen bevoordeelden en welke de productie van volledig gevormde bloedcellen ondersteunden.
Een verborgen regelknooppunt genaamd SAGA komt in beeld
Temidden van vele bekende regulatoren van bloedvorming doemden een verrassende reeks hits op: verschillende structurele onderdelen van een groot eiwitcomplex genaamd het SAGA-complex, waaronder genen met de namen Tada2b, Taf5l en Tada1. SAGA maakt niet zelf bloedcellen; in plaats daarvan helpt het andere genen aan- of uit te zetten door chemische markeringen aan te brengen op DNA-verpakkende eiwitten die histonen worden genoemd. Toen het team deze SAGA-componenten afzonderlijk uitschakelde en de bewerkte cellen in muizen transfereerde, zagen ze een consistent patroon. Onrijpe beenmergcellen stapelden zich op, maar hun vermogen om uit te rijpen tot circulerende witte bloedcellen, rode bloedcellen en bepaalde immuuncellen was sterk verminderd. In wezen zaten de stam- en progenitorcellen vast in een knelpunt en konden ze de weg naar volledig functionele bloedcellen niet afmaken.
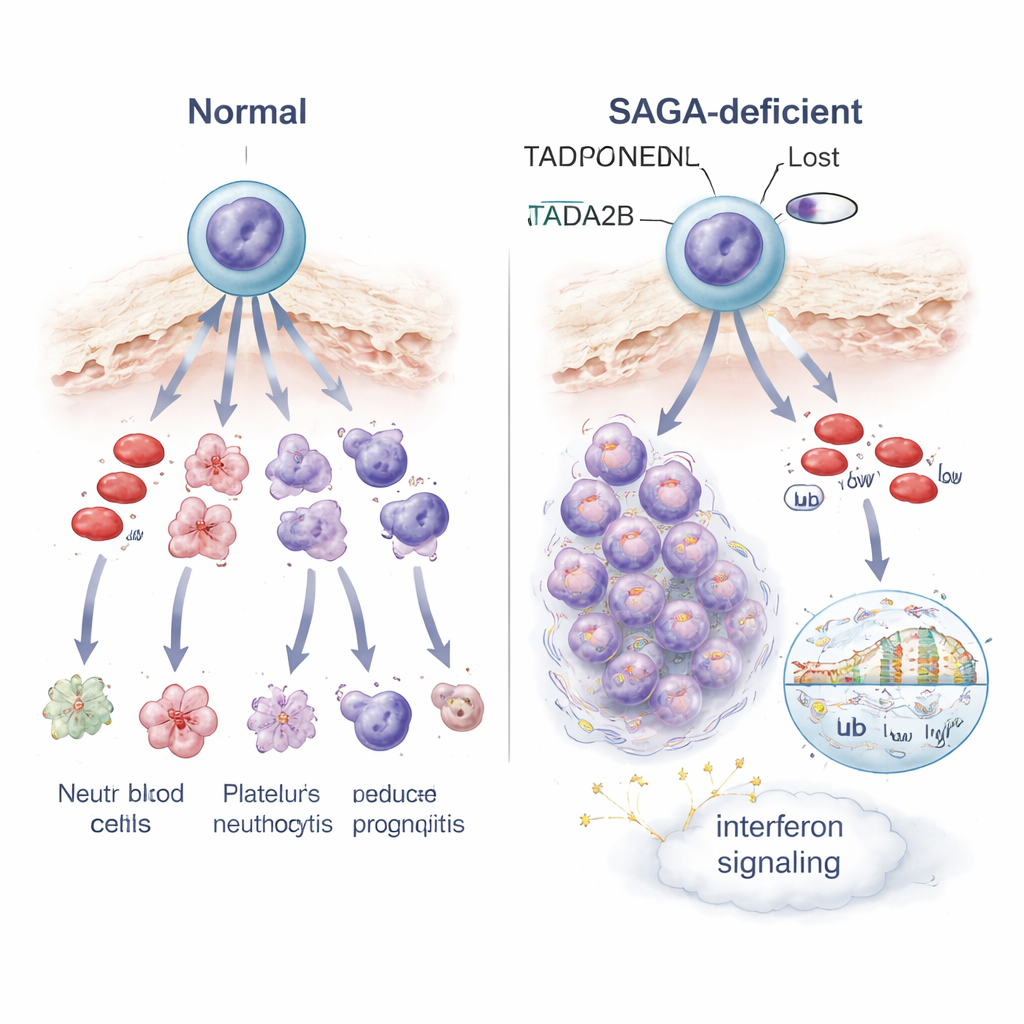
Hoe verstoorde genregulatie celbestemming en stresssignalen verandert
Om te begrijpen wat er misgaat in deze geblokkeerde cellen, brachten de wetenschappers de genactiviteit in kaart per cel en in bulk. Verlies van Tada2b of Taf5l herschakelde de activiteit van veel genen in stamcellen, met twee opvallende thema's. Ten eerste werden genen betrokken bij interferon-signalering — normaal onderdeel van de antivirale verdediging van het lichaam — aangezet, wat wijst op een intern alarm of stressreactie. Ten tweede werden de mitochondriën van de cellen, de kleine energiecentrales die het cellulaire werk aandrijven, minder actief, en de gewijzigde cellen werden gevoeliger voor een geneesmiddel dat gericht is op mitochondriale energieproductie. Op het niveau van DNA-verpakking lieten cellen zonder Tada2b verminderde niveaus zien van een histonmarkering die gekoppeld is aan open, actief chromatine, en veranderingen in een andere markering die te maken heeft met hoe genen worden afgelezen. Deze verschuivingen in chromatinechemie verklaren waarschijnlijk waarom veel genen, inclusief degenen die de juiste bloedrijping sturen, verkeerd gereguleerd raken.
Van basale mechanismen naar ziektmodellen
Het team vroeg zich vervolgens af of het op- of afschakelen van SAGA-activiteit deze effecten kon omkeren. Cellen dwingen extra Tada2b te produceren verlaagde de interferon-gerelateerde genactiviteit en verminderde het aandeel stamcelachtige cellen, het spiegelbeeld van de knockout. Het behandelen van normale stamcellen met een geneesmiddel dat de belangrijke enzymatische subunits van SAGA remt, reproduceerde veel van het Tada2b-verliessignatuur, wat het idee versterkt dat de chromatine-modificerende activiteit van SAGA centraal staat in zijn rol. Ten slotte richtten de onderzoekers zich op een humaan celmodel van myelodysplastisch syndroom, een pre-leukemische aandoening waarbij bloedproductie hapert en interferonroutes vaak verhoogd zijn. Toen ze SAGA-componenten in deze menselijke cellen uitschakelden en ze in immuundeficiënte muizen transplantkeerden, kregen de bewerkte cellen een groeivoordeel en activeerden opnieuw interferon- en myeloïde genprogramma's, wat suggereert dat dit regelknooppunt ook het ziektegedrag beïnvloedt.
Wat dit betekent voor bloedgezondheid en toekomstige therapieën
Voor een niet-specialistische lezer is de kernboodschap dat deze studie een krachtig regelcentrum onthult — het SAGA-complex — dat helpt bepalen wanneer bloedvormende stamcellen onrijp blijven, wanneer ze rijpen en hoe ze schadelijke stressreacties kunnen vermijden. Wanneer belangrijke SAGA-onderdelen ontbreken, stapelen stamcellen zich op maar produceren ze onvoldoende werkende bloedcellen, terwijl stress- en antiviraal-achtige signalen toenemen en mitochondriën verzwakken. Deze ontdekkingen verdiepen niet alleen ons begrip van hoe gezonde bloedproductie een leven lang wordt behouden, maar wijzen ook op dat subtiele veranderingen in SAGA-activiteit kunnen bijdragen aan ouderdomsgerelateerde bloedproblemen en aandoeningen zoals myelodysplastisch syndroom. Op de lange termijn kan het in kaart brengen van deze regelcircuiterie onderzoekers helpen therapieën te ontwerpen die defecte stamcellen terugsturen naar een evenwichtige, veerkrachtige bloedproductie.
Bronvermelding: Shankar, A., Olender, L., Hsu, I. et al. In vivo CRISPR screening identifies SAGA complex members as key regulators of hematopoiesis. Nat Commun 17, 1756 (2026). https://doi.org/10.1038/s41467-026-68465-6
Trefwoorden: hematopoëtische stamcellen, CRISPR-screening, SAGA-complex, interferon-signalering, myelodysplastisch syndroom