Clear Sky Science · nl
Afleiden van chromatine-architectuur op één locus via probabilistische in situ DNA-localisatie
Hoe de 3D-vorm van DNA bepaalt wanneer genen aan gaan
Ons DNA wordt vaak als een rechte ladder voorgesteld, maar in cellen vouwt het zich tot ingewikkelde lussen en spoelen. Die vormen doen ertoe: ze helpen bepalen welke genen aan gaan, wanneer en waar. Deze studie introduceert een nieuwe manier om de kleine 3D-ordening van DNA rond één gen in ontwikkelende fruitvliegembryo’s te onderzoeken en onthult hoe subtiele verschuivingen in DNA-opvouwing patronen van genactiviteit kunnen veranderen die het lichaamsplan bepalen.
Genregulatie observeren in een ontwikkelend embryo
Tijdens de ontwikkeling van een embryo moeten duizenden genen op precies het juiste moment in- en uitgeschakeld worden. Veel van die beslissingen worden genomen door korte DNA-stukken die enhancers worden genoemd, die tienduizenden basenparen van de genen die ze reguleren kunnen liggen. Om te werken moeten enhancers fysiek in de buurt komen van hun doelfgen in de driedimensionale ruimte, waarbij het DNA zich zodanig kringelt dat verre sites elkaar raken. Maar die lussen zijn klein, dynamisch en moeilijk zichtbaar. De auteurs concentreerden zich op één gen, brinker (brk), in de fruitvlieg Drosophila. Dit gen helpt bij het patroonteren van het vroege embryo en wordt in een streep langs de zijkant van het ei aangezet. Drie nabijgelegen DNA-regionelementen — twee enhancers (E1 en E2) en een promoter-proximaal element (PPE) naast het gen — werken samen om dit precieze patroon te genereren.
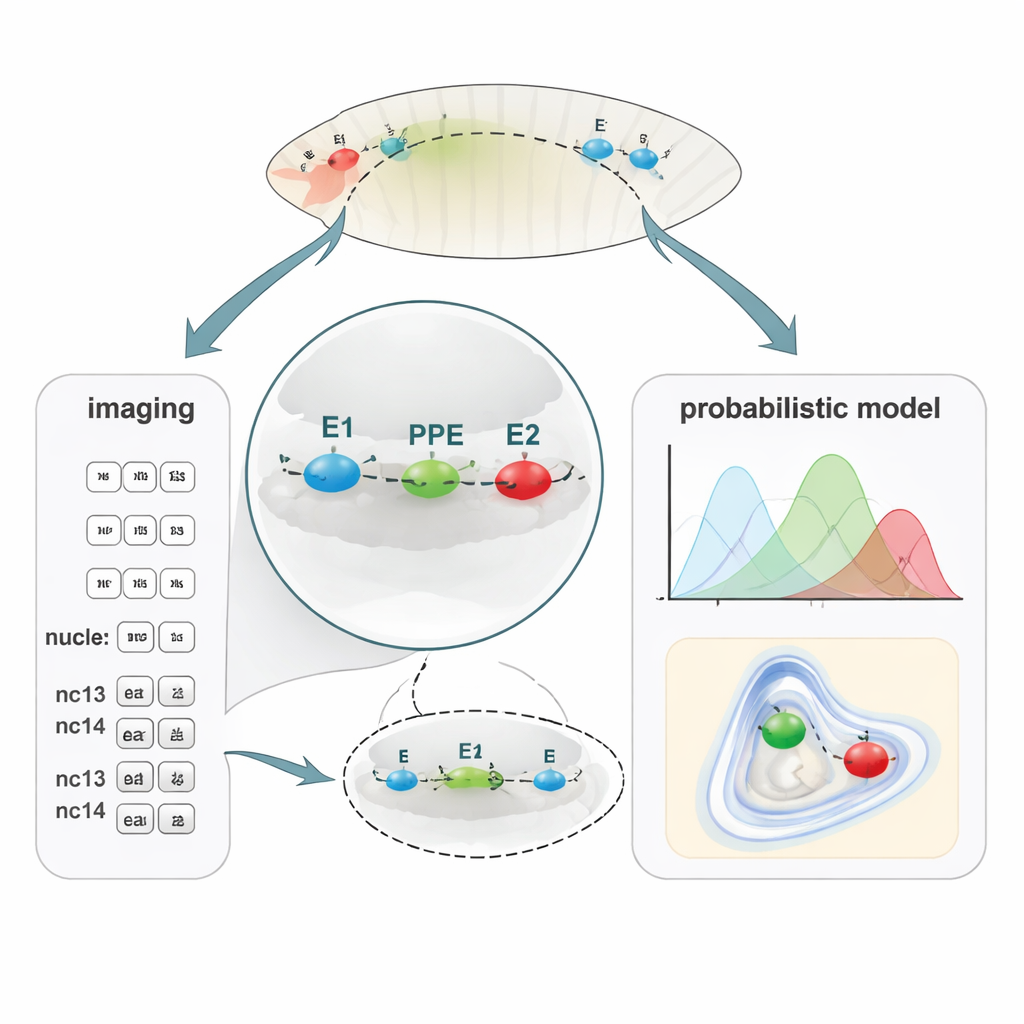
Een nieuwe manier om kleine DNA-afstanden in kaart te brengen
Om DNA-opvouwing aan genactiviteit te koppelen, ontwikkelde het team PLOTTED (Probabilistic Localization of Oligopaint Tagged Target Element Distances). Eerst gebruikten ze een DNA-labelingmethode genaamd Oligopaint FISH om drie verschillende fluorescente kleurstoffen aan de E1-, PPE- en E2-regio’s te binden in gefixeerde vliegembryo’s. Met een superresolutie-confocale microscoop maten ze 3D-afstanden tussen deze drie gekleurde punten in tienduizenden kernen in embryo’s tijdens opeenvolgende nucleaire cycli, van net voordat genactiviteit begint (pre-nc13) tot latere stadia (nc13 en nc14). Vervolgens voerden ze al deze afstanden in een aangepaste computationele pijplijn die ruisige metingen filtert en waarschijnlijkheidskaarten bouwt die laten zien waar elk element het waarschijnlijkst zit ten opzichte van de anderen. In plaats van één statische “lus” produceert PLOTTED een landschap van waarschijnlijke chromatinevormen voor elk ontwikkelingsstadium.
Wanneer DNA compacter wordt, ontwaakt het gen
In normale embryo’s vonden de onderzoekers dat zodra het embryo nucleaire cyclus 13 bereikt, beide enhancers dichter naar de PPE toe bewegen: de lokale DNA-buurt rond het brk-gen wordt compacter. Na dit punt blijven de afstanden tussen de drie elementen relatief stabiel. Belangrijk is dat dit tijdstip overeenkomt met het begin van brk-expressie, wat suggereert dat het aanstrakker worden van de DNA-configuratie helpt om het gen aan te zetten. PLOTTED toonde ook aan dat deze compacte rangschikking vaker voorkomt in regio’s van het embryo waar brk actief is, en lossere configuraties domineren waar het gen gerepresseeerd is, wat de koppeling tussen 3D-architectuur en transcriptie versterkt.
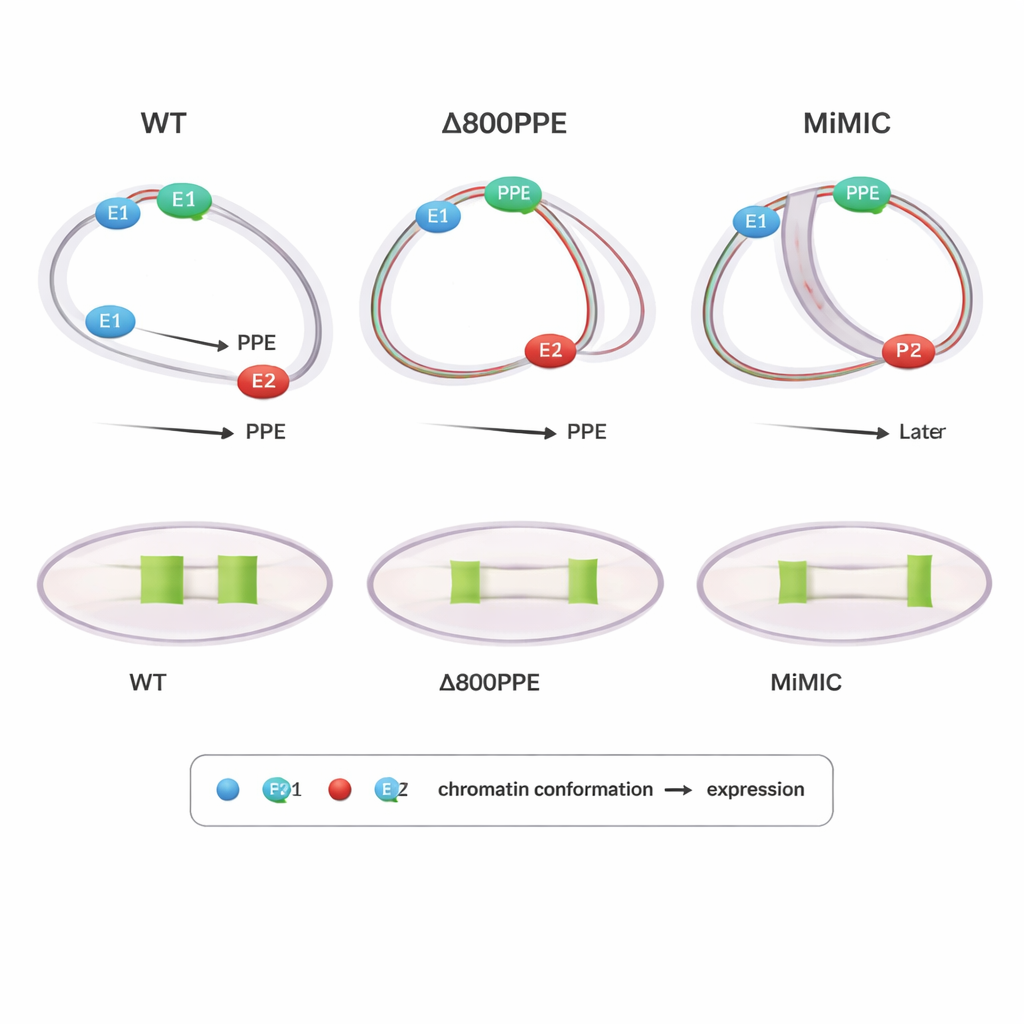
Mutaties laten zien waarom timing en positie belangrijk zijn
Om oorzaak en gevolg te onderzoeken bekeken de auteurs vliegen met ontworpen veranderingen op de brk-locus. In één mutant waren 800 basenparen van het PPE verwijderd, waardoor dit centrale element verzwakt werd; in een andere was een 7,3 kilobase DNA-cassette (MiMIC) tussen E1 en het PPE ingevoegd, waardoor ze verder van elkaar werden geduwd en er een extra promotor werd toegevoegd. Beide mutanten toonden vertraagde of verminderde brk-expressie. PLOTTED liet zien waarom: in de PPE-deletielijn trad de compacting van afstanden tussen het PPE en beide enhancers later dan normaal op, en in latere stadia bleef het PPE te dicht bij E1, waardoor E2 verhinderd werd het brede expressiepatroon te stimuleren dat in het wildtype te zien is. In de MiMIC-lijn associeerde het PPE te vroeg en te sterk met E2 en trok het pas later dichter naar E1, waardoor de normale overdracht tussen enhancers verstoord werd. Deze resultaten suggereren dat het niet alleen van belang is of elementen samenkomen, maar ook wanneer en met welke partner ze het dichts bij elkaar zijn, voor een correcte genuitvoer.
DNA-opvouwing verschilt door het embryo heen
Omdat PLOTTED ruimtelijke informatie in intacte embryo’s behoudt, kon het team ook nagaan of de DNA-architectuur varieert in verschillende lichaamsregio’s. Vergelijking van de laterale zones waar brk actief is met ventrale zones waar het gerepresseeerd is, toonde aan dat de drie elementen dichter bij elkaar liggen in actieve regio’s en verder uit elkaar staan in gerepresseeerde domeinen. Langs de kop-tot-staart-as observeerden ze dat de E1–PPE-afstanden anders veranderen aan de voorkant dan aan de achterkant van het embryo, wat suggereert dat regionale signalen de chromatine-architectuur fijn afstemmen om genexpressiepatronen te moduleren. Deze bevindingen ondersteunen het beeld dat de 3D-ordening van regulatorisch DNA contextafhankelijk is en tijd en positie in het ontwikkelende organisme volgt.
Waarom dit verder reikt dan fruitvliegen
In eenvoudige bewoordingen laat deze studie zien dat hoe DNA rond een enkel gen opgevouwen is nauw samenhangt met wanneer en waar dat gen wordt aangezet. De nieuwe PLOTTED-methode biedt een praktische manier om deze kleine DNA-buurten in intacte weefsels in kaart te brengen met wijdverspreide microscopen en eenvoudige chemie, gecombineerd met krachtige probabilistische modellering. Hoewel gedemonstreerd in vliegembryo’s, kan de aanpak op veel organismen en ziektemodellen worden toegepast. Nu wetenschappers steeds vaker ontdekken dat fout gevouwen chromatine ten grondslag ligt aan ontwikkelingsstoornissen en kanker, zullen tools zoals PLOTTED helpen onthullen hoe kleine verschuivingen in de 3D-layout van enhancers en genen kunnen uitmonden in grote veranderingen in celbestemming en gezondheid.
Bronvermelding: Le, M.T., McGehee, J., Dunipace, L. et al. Inferring chromatin architecture at a single locus through probabilistic in situ DNA localization. Nat Commun 17, 1752 (2026). https://doi.org/10.1038/s41467-026-68460-x
Trefwoorden: chromatine-architectuur, enhancer-promotorinteracties, Drosophila-embryogenese, genregulatie, superresolutie-imaging