Clear Sky Science · nl
Door neurale-kamcellen afkomstige DKK1 en NEDD4 moduleren Wnt‑signaal in het tweede hartveld om de ontwikkeling van de uitstroombreedt te orkestreren
Waarom kleine hartbouwers ertoe doen
Het vroege embryo‑hart begint als een eenvoudige buis, maar moet zich snel herstructureren tot een complex orgaan dat bloed zowel naar het lichaam als naar de longen stuurt. Subtiele foutjes in dit bouwproces kunnen ernstige geboorteafwijkingen veroorzaken, waaronder aandoeningen die kort na de geboorte geopereerd moeten worden. Deze studie onthult hoe twee celgroepen met elkaar communiceren tijdens het vormgeven van de belangrijkste uitgang van het hart en legt een moleculaire fout bloot die kan bijdragen aan aangeboren hartafwijkingen bij zowel muizen als mensen.
Twee teams die de uitgang van het hart bouwen
Het deel van het hart dat bloed uit de kamers voert — de uitstroombreedt — ontstaat uit een gebied dat het tweede hartveld wordt genoemd. Cellen hier moeten lang genoeg flexibel blijven als “progenitoren” om aan de groeiende uitstroombreedt te worden toegevoegd, en vervolgens op het juiste moment in rijpe spiercellen veranderen. Naast hen trekken neurale‑kamcellen, een rondtrekkende populatie die helpt bij het bouwen van de grote slagaders en kleppen. Eerder werk suggereerde dat deze neurale‑kamcellen het tweede hartveld op de een of andere manier beïnvloeden, maar hoe die kruisgesprekken werkten was onbekend. 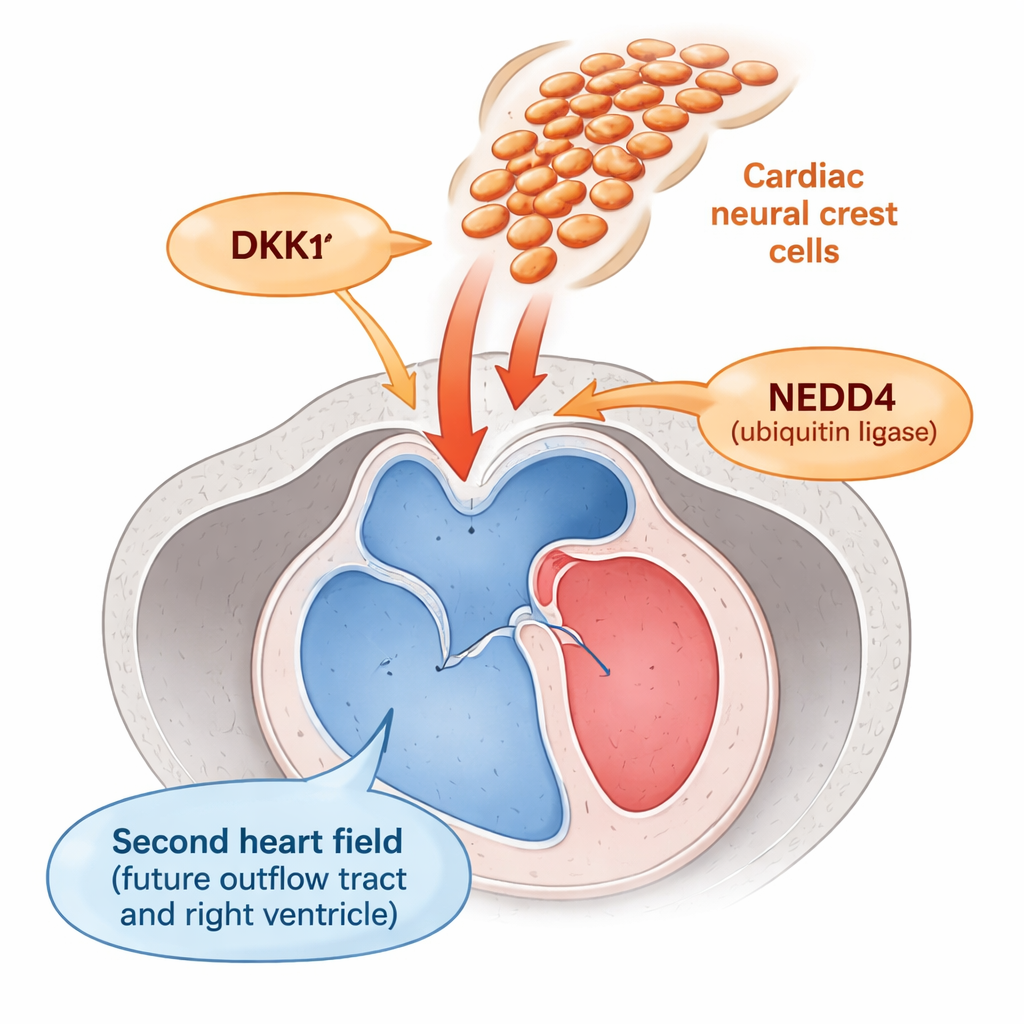
Een moleculaire dimmer voor groeisignalen
De auteurs ontdekten dat neurale‑kamcellen fungeren als een dimmer voor een belangrijk groeisignaal genaamd Wnt, dat progenitorcellen in deling houdt en hun rijping vertraagt. Ze vonden dat neurale‑kamcellen een belangrijke bron zijn van DKK1, een klein uitgescheiden eiwit dat Wnt‑signalering in nabijgelegen cellen uitschakelt. DKK1 zelf wordt normaal geremd door NEDD4, een eiwit dat DKK1 labelt voor afbraak. In muizembryo’s zonder Nedd4 specifiek in neurale‑kamcellen liep DKK1 abnormaal hoog op. Dit overtollige DKK1 zette de Wnt‑activiteit in het naburige tweede hartveld omlaag, zoals bleek uit verminderde nucleaire bèta‑catenine — een standaardmaat voor Wnt‑signalering — en lagere niveaus van meerdere Wnt‑responsieve genen.
Als de timing niet klopt, faalt de hartgeometrie
Te veel DKK1 en te weinig Wnt hadden een duidelijke consequentie: cellen van het tweede hartveld begonnen te vroeg te veranderen in hartspier. Merkers van rijpe spier verschenen vroeg in deze progenitorzone, en er bleven minder ongedifferentieerde cellen over om de uitstroombreedt te verlengen. Door delende cellen in de tijd te volgen, toonde het team aan dat er in de mutanten minder tweede‑hartveld‑cellen aan de uitstroombreedt werden toegevoegd. Als gevolg daarvan was de uitstroombreedt korter en draaide hij verkeerd, wat leidde tot misalignering tussen de grote slagaders en de kamers. Deze structurele fouten leken op menselijke conotruncale defecten zoals double‑outlet right ventricle en aanverwante misvormingen die ook gezien worden in volledige Nedd4 knockout‑muizen.
Het bewijs voor de rol van het signaal, en een link naar menselijke ziekte
Om te bevestigen dat veranderde Wnt‑signalering daadwerkelijk deze problemen veroorzaakte, manipuleerden de onderzoekers de route met geneesmiddelen bij drachtige muizen. Wnt blokkeren in anders gezonde embryo’s duwde hen richting dezelfde voortijdige differentiatie en rotatiefouten die werden gezien bij verlies van Nedd4, terwijl het verlagen van de Dkk1‑gendosis in de Nedd4‑deficiënte achtergrond de grootte en rotatie van de uitstroombreedt gedeeltelijk redde. Ten slotte identificeerde het team een kind met Tetralogie van Fallot dat een zeldzame geërfde variant in NEDD4 droeg die zijn vermogen om DKK1 te labelen voor afbraak verzwakte. Muizen die zo’nzelfde Nedd4‑variant kregen ingebracht ontwikkelden rechterzijde‑wand‑ en septumdefecten, wat de gedachte ondersteunt dat defecte NEDD4–DKK1‑controle kan bijdragen aan aangeboren hartafwijkingen bij mensen. 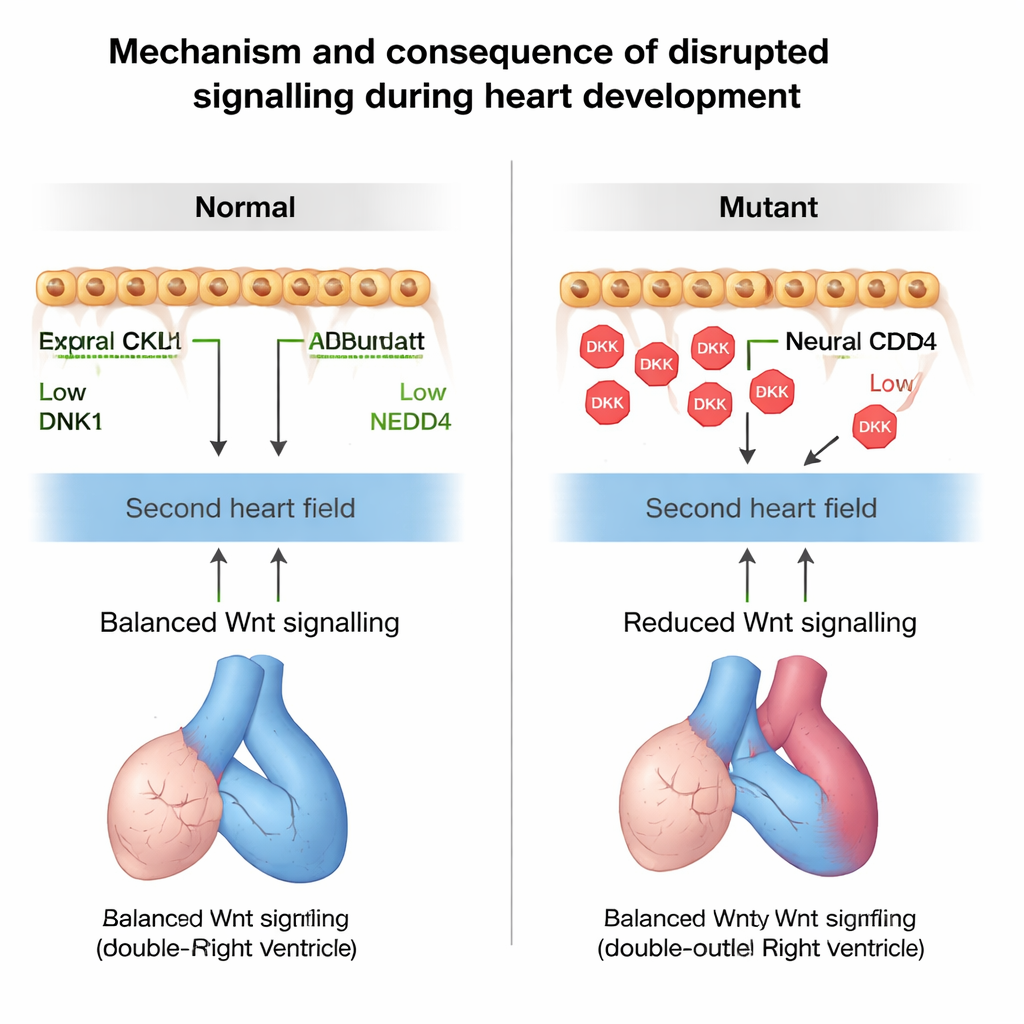
Wat dit betekent voor het begrip van hartafwijkingen
Voor niet‑specialisten is de kernboodschap dat de “uitgangsramp” van het hart afhankelijk is van precieze timing van wanneer de bouwstenen stoppen met delen en beginnen met het worden van spier. Deze timing wordt niet alleen intern in het hartweefsel geregeld, maar ook door naburige neurale‑kamcellen die een groeisignaal fijn afstellen via het NEDD4–DKK1‑paar. Als deze moleculaire dimmer te laag blijft, wordt de uitstroombreedt onvoldoende opgebouwd en verkeerd uitgelijnd, wat leidt tot ernstige geboorteafwijkingen. Door dit pad in kaart te brengen en het te koppelen aan een menselijke genvariant, biedt de studie nieuwe aanwijzingen voor hoe sommige aangeboren hartafwijkingen ontstaan en benadrukt ze mogelijke moleculaire doelen voor toekomstige diagnostiek of interventie.
Bronvermelding: Wiszniak, S., Alankarage, D., Lohraseb, I. et al. Neural crest cell-derived DKK1 and NEDD4 modulate Wnt signalling in the second heart field to orchestrate outflow tract development. Nat Commun 17, 1751 (2026). https://doi.org/10.1038/s41467-026-68459-4
Trefwoorden: aangeboren hartafwijking, hartontwikkeling, neurale-kamcellen, Wnt-signaal, cardiale uitstroombreedt