Clear Sky Science · nl
Een veelvoorkomende DNA-verwijdering die de 3’UTR van mdr1 wijzigt, wordt geassocieerd met verminderde gevoeligheid voor mefloquine in P. vivax‑parasieten van Cambodjaanse patiënten
Waarom deze malariastudie ertoe doet
Voor mensen die in of naar gebieden met malaria reizen, zijn effectieve geneesmiddelen van levensbelang. Maar malariaparasieten vinden voortdurend nieuwe manieren om behandeling te overleven. Deze studie richt zich op Plasmodium vivax, de belangrijkste veroorzaker van malaria buiten Afrika, en onthult een subtiele genetische verandering die het parasite al kan helpen om één belangrijk geneesmiddel, mefloquine, beter te verdragen. Het vroegtijdig begrijpen van deze verschuiving kan volksgezondheidsinstanties helpen om een stap voor te blijven bij het opkomen van medicijnresistentie.
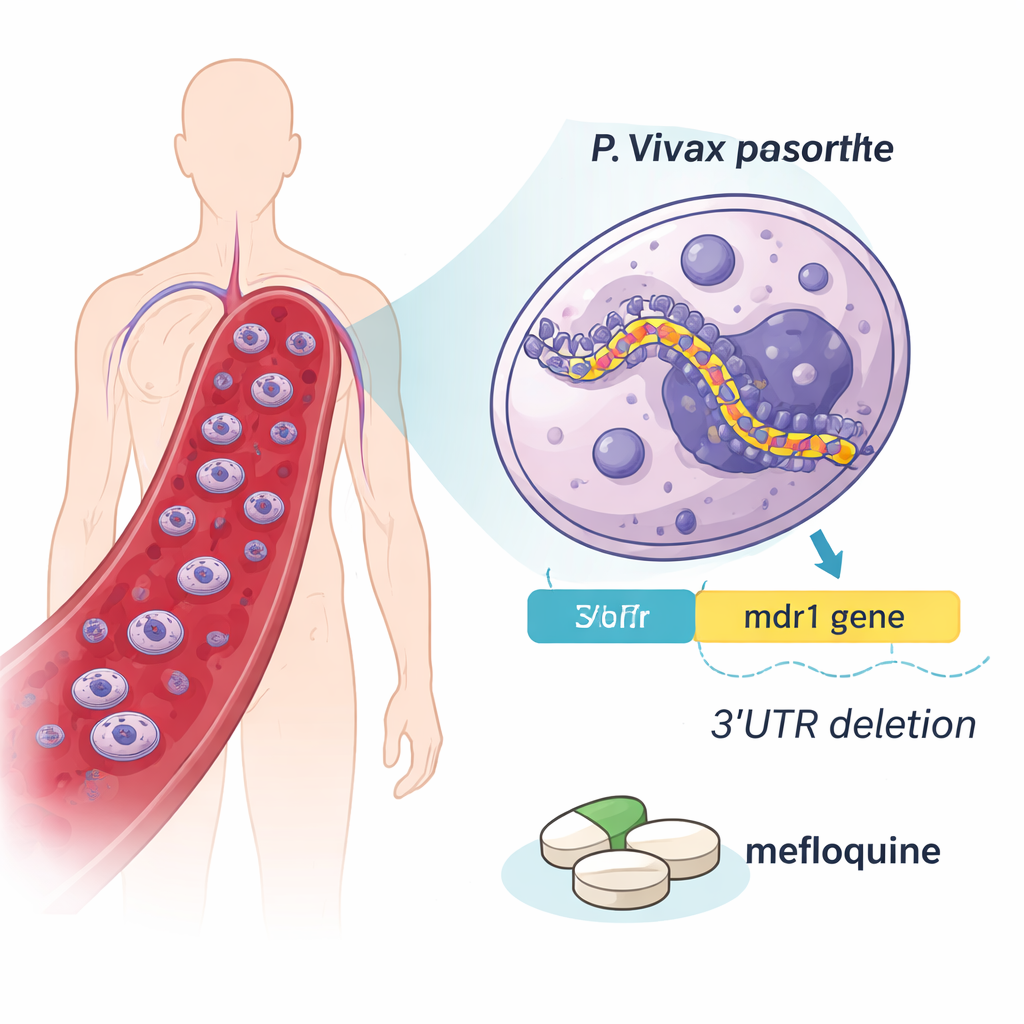
Een taaie parasiet en krimpende behandelingsopties
Malaria bij de mens wordt veroorzaakt door meerdere verwante parasieten, maar P. vivax is bijzonder moeilijk uit te roeien. Hij kan maanden in de lever verscholen blijven voordat hij opnieuw in de bloedbaan verschijnt, en circuleert vaak op niveaus die te laag zijn voor standaardtests om op te merken. Decennialang werkte het eerstelijnsgeneesmiddel chloroquine goed tegen P. vivax, maar tekenen van resistentie zijn verspreid. Daarom raadt de Wereldgezondheidsorganisatie nu aan artemisinin-gebaseerde combinatietherapieën (ACT’s) te gebruiken, die een snelwerkend middel combineren met een langwerkende partner zoals mefloquine. Omdat P. vivax in het laboratorium moeilijk te kweken is, vertrouwen wetenschappers sterk op patiëntmonsters en genetische aanwijzingen om te volgen hoe de parasiet op deze medicijnen reageert.
Een klein ontbrekend DNA-stuk in een sleutelfactor voor medicijnresistentie
De onderzoekers sequentieerden de genomen van 206 P. vivax‑monsters die tussen 2021 en 2023 van malariapatiënten in Cambodja waren genomen. Ze zochten naar DNA‑segmenten die verwijderd of verdubbeld waren. Tussen vele herschikkingen stak er één uit: meer dan 80% van de parasieten droeg een kleine DNA‑verwijdering die net na het einde van de coderende regio van een gen genaamd mdr1 (multidrug resistance 1) lag. Dit gen codeert voor een transportereiwit dat verschillende verbindingen, waaronder geneesmiddelen, door een membraan binnenin de parasiet kan pompen. In tegenstelling tot eerder gerapporteerde mutaties veranderde deze deletie van 837 basenparen de eiwitsequentie zelf niet. In plaats daarvan bevond hij zich in de zogenaamde 3'untranslated region (3'UTR), een segment van het gen dat niet vertaald wordt naar eiwit maar sterk kan beïnvloeden hoeveel eiwit uiteindelijk wordt gemaakt.
Onafhankelijke deleties en gewijzigde boodschapper-RNA’s van hetzelfde gen
Om te zien of soortgelijke veranderingen elders voorkwamen, heranalyseerde het team bijna 830 P. vivax‑genomen uit 25 landen. Ze ontdekten een andere, kortere deletie die overlapt met hetzelfde downstreamgebied van mdr1 bij parasieten uit Zuid‑Amerika. Gedetailleerde vergelijkingen en bevestigende PCR‑tests toonden aan dat de Zuidoost‑Aziatische en Zuid‑Amerikaanse deleties verschillend waren, wat suggereert dat ze onafhankelijk zijn ontstaan — een aanwijzing dat natuurlijke selectie veranderingen in deze regulatorische regio kan bevoordelen. Met behulp van RNA‑sequencing op 95 Cambodjaanse infecties lieten de onderzoekers zien dat parasieten met de deletie een alternatieve versie van het mdr1 boodschapper‑RNA produceerden, met een andere 3'UTR. Na correctie voor transcriptlengte hadden parasieten die de deletie droegen bijna twee keer zoveel mdr1 mRNA als die zonder, wat impliceert dat het ontbrekende DNA of de nieuwe 3'UTR‑sequentie helpt om de expressie van het gen te stabiliseren of te verhogen.
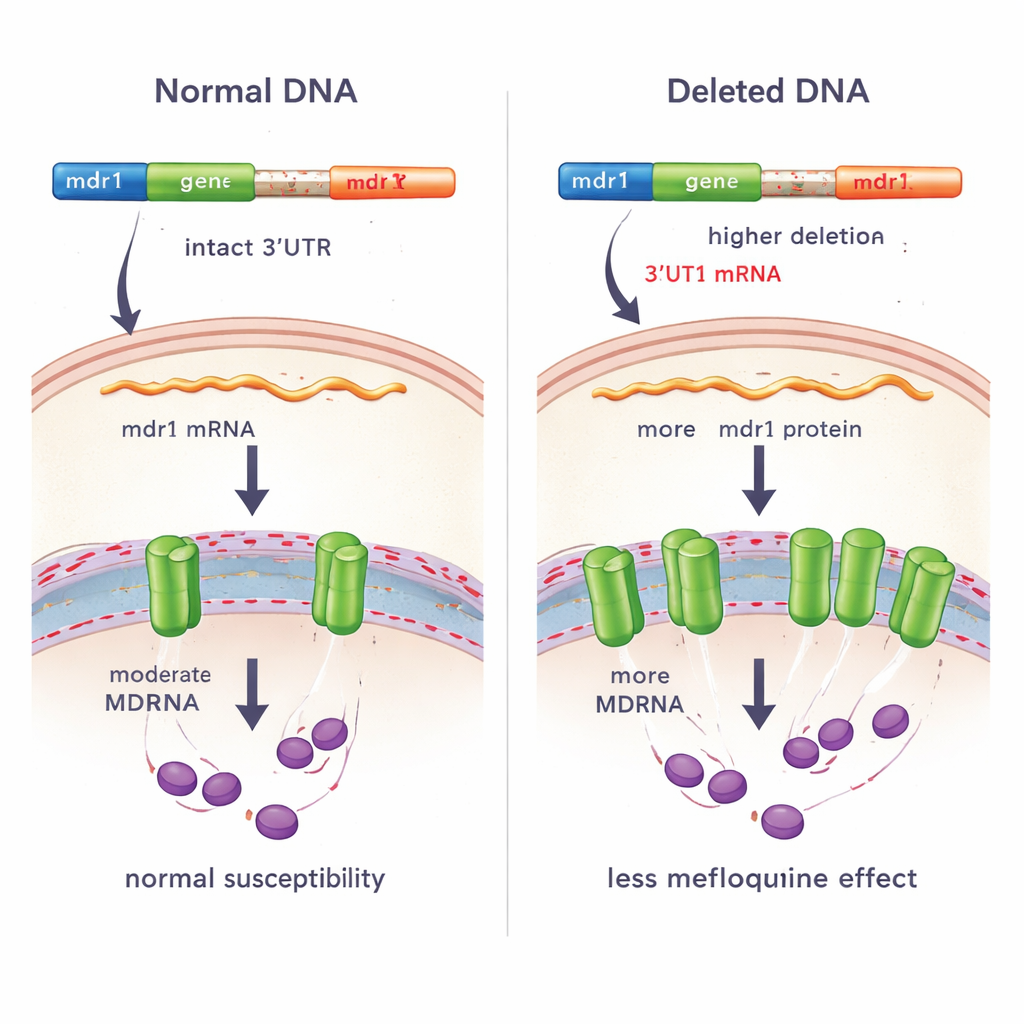
De deletie koppelen aan medicijnrespons bij patiënten en labtests
Aangezien mdr1 in verband is gebracht met resistentie tegen meerdere antimalariamiddelen, onderzocht het team of de deletie verband hield met hoe parasieten op behandeling reageerden. Ze vergeleken eerst hoe snel parasieten uit het bloed van patiënten werden verwijderd na behandeling met artesunaat. Bij 167 infecties was er geen significant verschil in klaringssnelheden tussen parasieten met en zonder de deletie, wat suggereert dat deze genetische verandering de gevoeligheid voor artesunaat zelf niet direct beïnvloedt. In een kleinere set van 14 infecties, waarbij de onderzoekers de parasietengroei in aanwezigheid van mefloquine buiten het lichaam maten, neigden parasieten met de deletie naar hogere IC50‑waarden — wat betekent dat ze meer geneesmiddel nodig hadden om groei te remmen — dan parasieten zonder de deletie. Dit patroon komt overeen met verminderde gevoeligheid voor mefloquine, hoewel de steekproefomvang beperkt was.
Een verontrustende toename in de tijd en wat dat kan betekenen
Om te begrijpen hoe wijdverspreid de deletie is geworden, screenden de auteurs 592 gearchiveerde P. vivax‑monsters die tussen 2014 en 2024 in Cambodja waren verzameld. Voor de introductie van mefloquine als onderdeel van ACT’s voor vivax‑malaria rond 2016–2017 droeg ongeveer 30% van de parasieten de deletie. Na de omschakeling steeg de frequentie tot boven 60% en stabiliseerde daarna; deze trend was statistisch sterk en bleef bestaan bij een focus op oostelijk Cambodja alleen. De deletie was al op lage niveaus aanwezig voordat mefloquine veelvuldig tegen P. vivax werd gebruikt, mogelijk door indirecte blootstelling toen het middel tegen P. falciparum werd ingezet of omdat de verandering ook de respons op andere medicijnen beïnvloedt. Gecombineerd met recente meldingen van iets tragere parasietenklaring na artemisininebehandeling, wekt de uitkomst bezorgdheid dat P. vivax in Cambodja richting een verminderde effectiviteit van de huidige artesunaat–mefloquinecombinatie beweegt.
Wat dit betekent voor malariabestrijding
Voor niet‑specialisten is de kernboodschap dat, zelfs wanneer het belangrijkste gen voor medicijnresistentie van een parasiet intact lijkt, kleine veranderingen in de nabije "bedradings‑regie" van het DNA kunnen beïnvloeden hoe sterk het gen wordt aangezet. In dit geval lijkt een veelvoorkomende deletie in een niet‑coderende regio van mdr1 de activiteitsniveaus van het gen te verhogen en wordt deze geassocieerd met iets zwakkere effecten van mefloquine op P. vivax. Hoewel er nog geen duidelijke aanwijzingen zijn voor behandelingsfalen in Cambodja, suggereert de stijgende frequentie van deze deletie dat medicijndruk stilletjes parasieten met deze eigenschap kan bevoordelen. Het vroegtijdig herkennen en monitoren van zulke subtiele genetische waarschuwingssignalen kan gezondheidsautoriteiten helpen medicijnbeleid aan te passen, betere surveillancetools te ontwerpen en het krimpende arsenaal van effectieve antimalariabehandelingen te beschermen.
Bronvermelding: Ko, K., Tebben, K., Andrianinarivomanana, T. et al. A common DNA deletion altering the 3’UTR of mdr1 is associated with reduced mefloquine susceptibility in P. vivax parasites from Cambodian patients. Nat Commun 17, 1748 (2026). https://doi.org/10.1038/s41467-026-68456-7
Trefwoorden: Plasmodium vivax, resistentie tegen malariamedicatie, mefloquine, mdr1-gen, Cambodja