Clear Sky Science · nl
Af-CUT&Tag: een gevoelige en antibody-vrije methode voor chromatineprofilering met genetisch gecodeerde tags en hoogaffiniteitsbinders gefuseerd aan Tn5
Een kijkje in onze DNA-regiekamer
Elke cel in je lichaam beslist voortdurend welke genen aan of uit moeten, en daarmee beïnvloedt ze alles van leverherstel tot kanker‑risico. Wetenschappers bestuderen deze beslissingen door in kaart te brengen waar sleutelproteïnen op ons DNA zitten, maar de beste instrumenten daarvoor waren lange tijd afhankelijk van kwetsbare, dure antilichamen die niet altijd goed werken. Dit artikel introduceert een nieuwe, antibody‑vrije manier om deze DNA–eiwitinteracties in kaart te brengen, Af‑CUT&Tag, die gevoeliger, betrouwbaarder en krachtig genoeg is om zelfs op kleine monsters en individuele cellen toe te passen.
Waarom antilichamen ons beperken
Traditionele methoden voor chromatinekaarten hebben antilichamen nodig—grote Y‑vormige eiwitten die een specifiek doeleiwit herkennen—om een enzym naar de juiste plekken op het DNA te leiden. Wanneer antilichamen perfect werken, maken ze het mogelijk om te zien waar transcriptiefactoren en andere regulatoren over het genoom gebonden zijn. In de praktijk zijn antilichamen echter soms moeilijk te verkrijgen, inconsistente kwaliteit, en kunnen ze geblokkeerd worden door veelvoorkomende chemische modificaties op eiwitten, zoals fosforylering of acetylatie. Die problemen kunnen de resulterende kaarten vervagen, beperken welke eiwitten bestudeerd kunnen worden en het moeilijk maken om resultaten tussen laboratoria of experimenten te vergelijken.
Kleine tags en slimme binders vervangen antilichamen
Af‑CUT&Tag omzeilt antilichamen volledig door het doelwit‑eiwit een klein genetisch naamlabel te geven. Met CRISPR‑genoomediting fuseren de onderzoekers korte peptidetags, zoals HiBiT of ALFA, aan het natuurlijke eiwit in cellen of weefsels. Vervolgens gebruiken ze ontworpen partner‑eiwitten—hoogaffiniteitsbinders die deze tags herkennen—rechtstreeks gefuseerd aan het Tn5‑enzym, dat DNA knipt en sequentieadapters aanbrengt. Wanneer de binder–Tn5‑fusie aan de tag op het doeleiwit bindt, knipt het nabijgelegen DNA en markeert die locaties voor sequencing. Omdat de tags erg klein zijn en de binder–Tn5‑fusie veel kleiner is dan een antilichaam, dringt dit systeem gemakkelijk cellen en kernen binnen, bindt met uitzonderlijke precisie en wordt het niet verstoord door chemische modificaties op het doeleiwit. 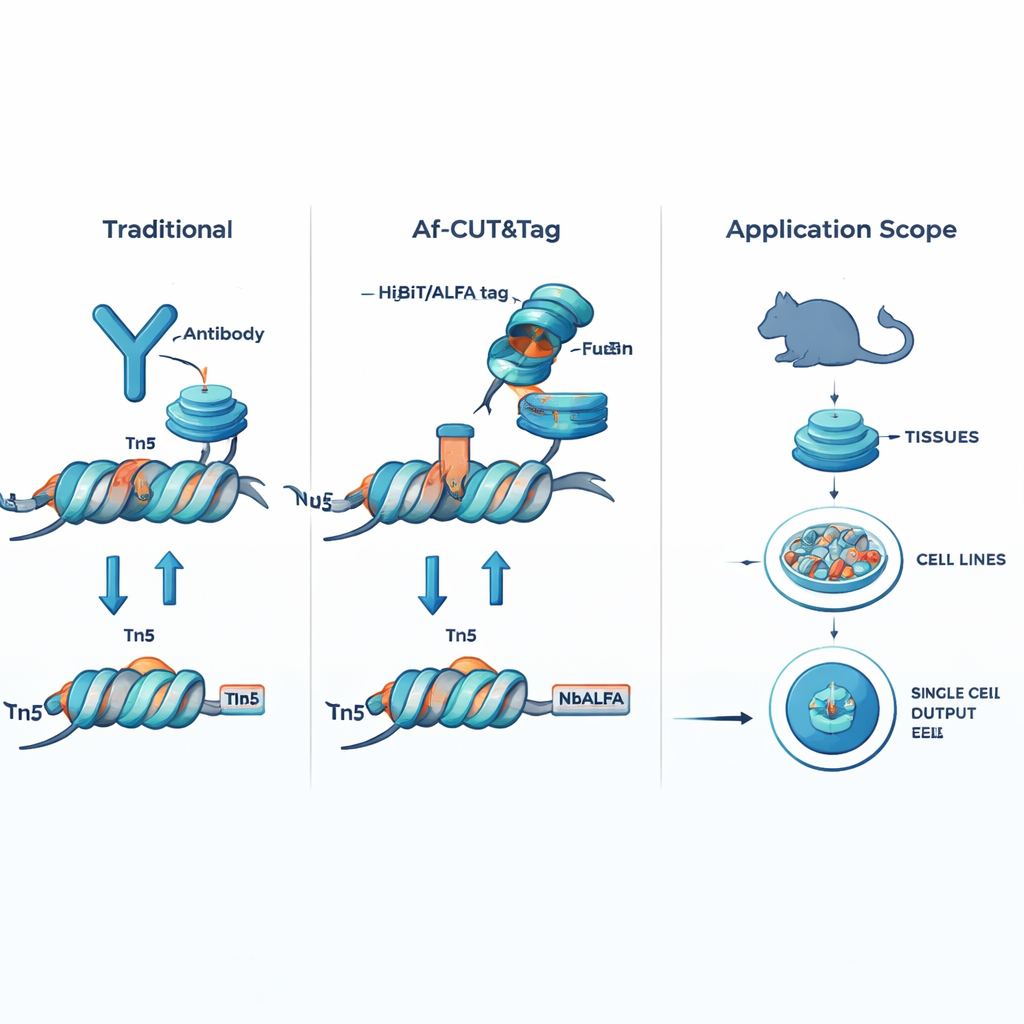
Scherpere kaarten van minder cellen
Het team toonde eerst aan dat hun binder–Tn5‑fusies de tags nog steeds zeer sterk grijpen en DNA efficiënt knippen. Daarna vergeleken ze Af‑CUT&Tag met geavanceerde antilichaam‑gebaseerde methoden voor het in kaart brengen van RNA polymerase II, het enzym dat coderende genen afleest, en het CTCF‑eiwit, een belangrijke organisator van genoomstructuur. Over menselijke cellijnen heen produceerde Af‑CUT&Tag schonere signalen bij genstartpunten, minder off‑target knipplaatsen in open maar irrelevante DNA‑regio’s en hogere kwaliteit sequencingbibliotheken. Opmerkelijk genoeg genereerde het robuuste kaarten van slechts ongeveer 500 cellen, en dezelfde strategie kon worden aangepast aan veel verschillende binders die op uiteenlopende DNA‑kenmerken richten. De methode werd ook uitgebreid naar enkele cellen door elk celfragment te barcoderen, waardoor gedetailleerde chromatinekaarten per cel konden worden opgebouwd.
Leverherstel in realtime volgen
Om te laten zien wat deze technologie in levende dieren kan onthullen, pasten de auteurs Af‑CUT&Tag toe op muisleverregeneratie. Ze gebruikten virussen en CRISPR om HiBiT‑tags toe te voegen aan twee sleutelregelaars van de “Hippo‑route”, YAP1 en TAZ, die helpen orgaangrootte en herstel te controleren. Na het chirurgisch verwijderen van een deel van de lever isoleerden ze levercelkernen voor de operatie en 24 uur daarna, en gebruikten Af‑CUT&Tag om te zien waar YAP1 en TAZ op het genoom gebonden waren. De kaarten toonden dat deze eiwitten vroeg na het letsel hun aanwezigheid verminderen bij genen die vetverwerking en synthese aansturen, terwijl levercellen tijdelijk vetdruppels ophopen. Tegelijkertijd nam YAP1/TAZ‑binding toe bij genen die betrokken zijn bij het opruimen van heem, een potentieel toxisch bloedcomponent, en bij Mir122, een gen dat een microRNA produceert dat sterk in de lever is verrijkt.
miR‑122 als beschermer van regeneratie
miR‑122 is een klein RNA‑molecuul dat helpt de activiteit van vele andere genen fijn af te stemmen. Met Af‑CUT&Tag zagen de onderzoekers sterkere YAP1/TAZ‑binding dicht bij de Mir122‑regio, samen met meer open chromatine en toegenomen chemische markeringen die aan genactivatie zijn gekoppeld. Experimenten bevestigden dat miR‑122‑niveaus stijgen tijdens het vroege regeneratievenster. Wanneer het team specifiek miR‑122 verwijderde in muislevercellen, toonden dieren meer vetophoping, sterkere ontstekingsreacties en minder levercellen die na de operatie de celcyclus ingingen. Samen suggereren deze resultaten dat YAP1/TAZ de lever helpen een zorgvuldig evenwicht te bewaren tijdens herstel: tijdelijk vet opslaan voor energie, schade door heem en ontsteking beperken, en miR‑122 gebruiken om overmatige stress te remmen terwijl weefselgroei wordt bevorderd. 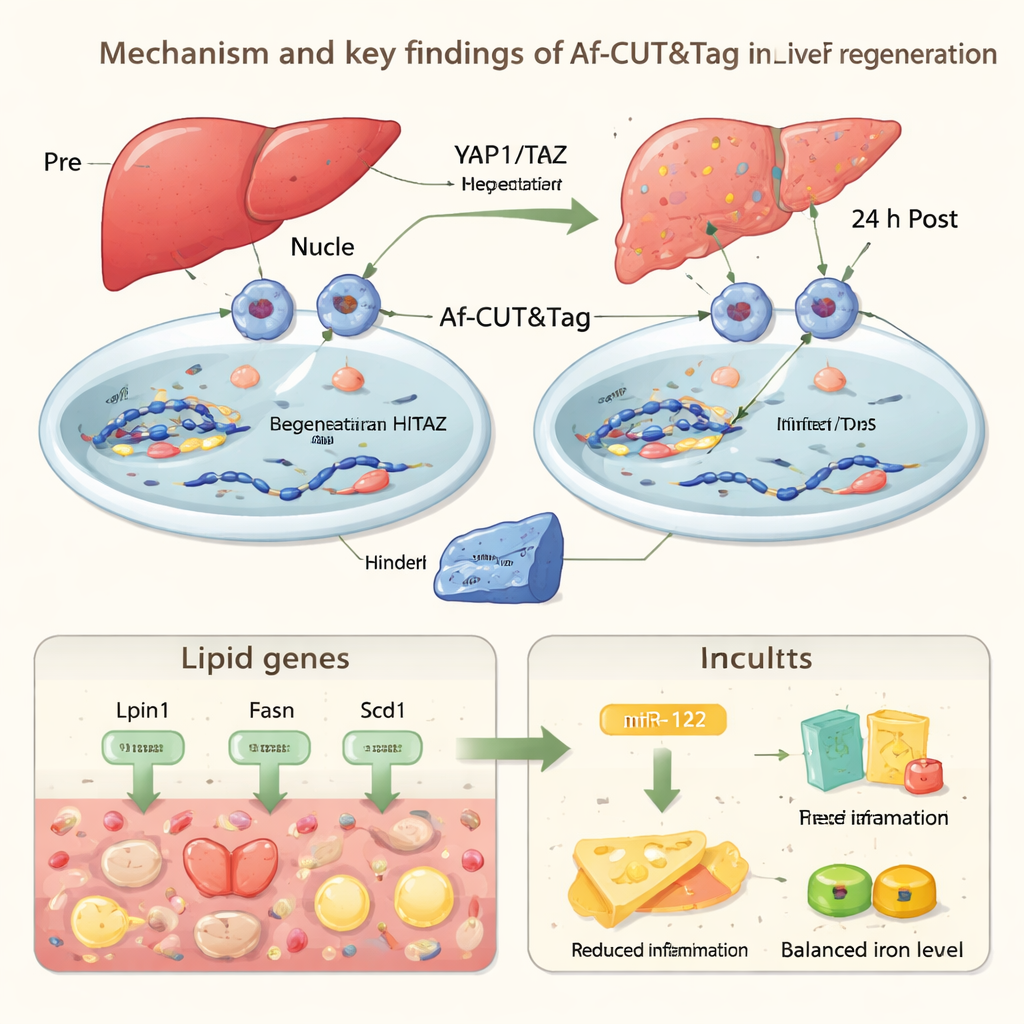
Een veelzijdige nieuwe lens op genregulatie
Af‑CUT&Tag biedt een modulaire, antibody‑vrije manier om te zien waar sleutelproteïnen op DNA zitten in cellijnen, weefsels en zelfs individuele cellen. Door onvoorspelbare antilichamen te vervangen door kleine genetische tags en ontworpen binders levert het scherpere, beter reproduceerbare kaarten uit veel minder cellen. Toegepast op leverregeneratie onthulde het hoe YAP1 en TAZ metabolisme, ijzerhuishouding en het microRNA miR‑122 coördineren om vroeg herstel te ondersteunen. Naarmate genoomediting en designerbinders blijven verbeteren, kan deze strategie een standaardtool worden voor het ontleden van hoe genregulatie goed gaat in ontwikkeling en regeneratie—en fout gaat bij ziekten zoals kanker en leverfalen.
Bronvermelding: Wang, X., Deng, X., Qiu, L. et al. Af-CUT&Tag: a sensitive and antibody-free chromatin profiling method using genetically encoded tags and high-affinity binders fused to Tn5. Nat Commun 17, 1746 (2026). https://doi.org/10.1038/s41467-026-68454-9
Trefwoorden: chromatineprofilering, epigenetica, leverregeneratie, YAP1 TAZ, microRNA-122