Clear Sky Science · nl
Functionele varianten op 1p36.23 geven risico op schizofrenie door modulatie van RERE
Waarom kleine DNA-veranderingen ertoe doen voor geestelijke gezondheid
Schizofrenie is een ernstige psychische aandoening die beïnvloedt hoe mensen denken, voelen en relaties aangaan met anderen. De aandoening komt sterk in families voor, maar de meeste betrokken genetische veranderingen zijn kleine, verspreide aanpassingen in ons DNA. Deze studie zoomt in op één zo’n regio van het genoom en laat stap voor stap zien hoe twee subtiele DNA-varianten de ontwikkeling en communicatie van hersencellen kunnen veranderen op manieren die het risico op schizofrenie kunnen vergroten. 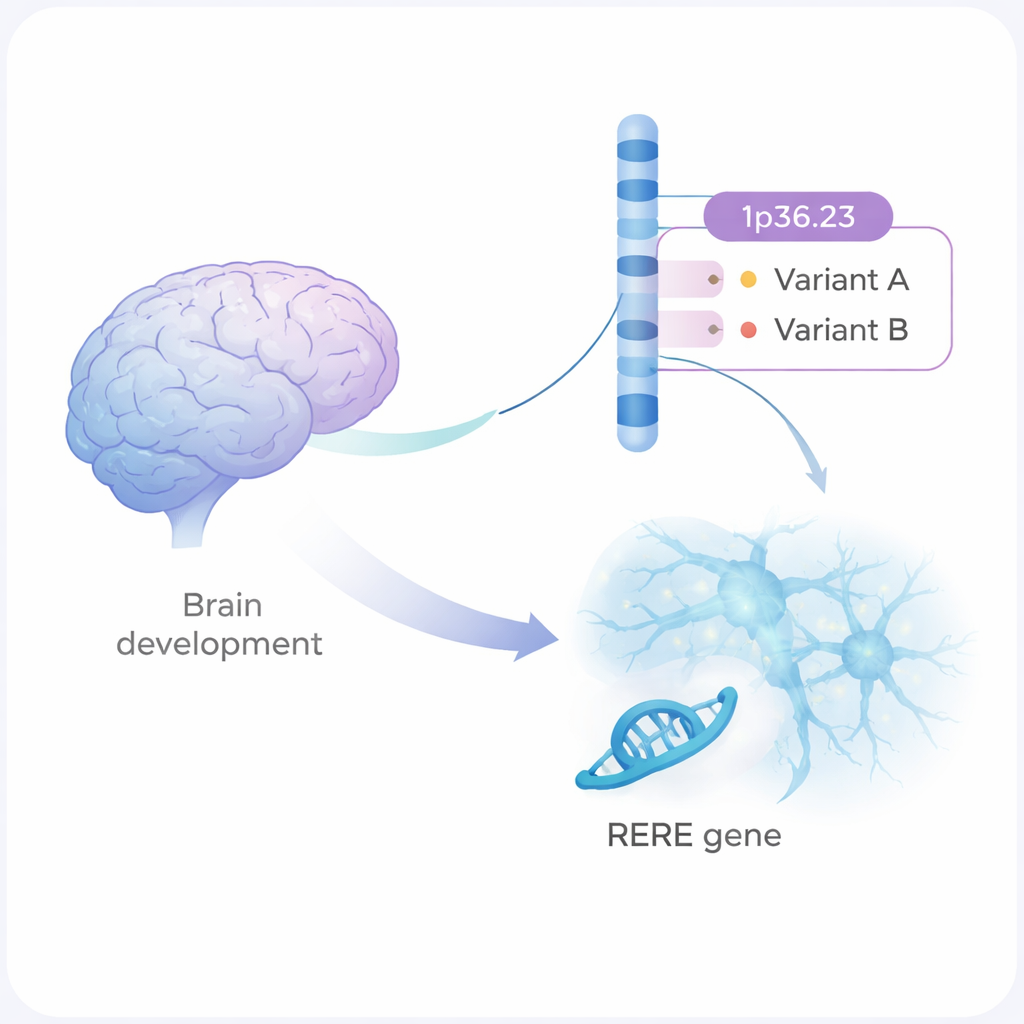
Een genetische hotspot op chromosoom 1
Grote genetische studies hebben meer dan 300 regio’s van het menselijk genoom geïdentificeerd die gekoppeld zijn aan schizofrenie. Een daarvan is een DNA-stuk op chromosoom 1, aangeduid als 1p36.23. Tot nu toe wisten wetenschappers niet welke exacte veranderingen in dit gebied, of welk gen, daadwerkelijk schade veroorzaken. De auteurs combineerden statistische genetica met laboratoriumexperimenten en wezen twee DNA-varianten aan, rs159961 en rs301792, gelegen in een gen dat RERE heet. Deze varianten veranderen het RERE-eiwit niet zelf; ze bevinden zich in plaats daarvan in regulatorische “schakelaar”-zones binnen het gen die bepalen hoe sterk RERE wordt aangeschakeld.
Hoe risicovarianten het volume van RERE opvoeren
Het team vroeg eerst of deze twee varianten daadwerkelijk als functionele schakelaars werken. Met reporterassays—testen waarbij een DNA-fragment een lichtproducerend gen aanstuurt—toonden ze aan dat de schizofrenie-geassocieerde vormen van rs159961 en rs301792 in zenuwachtige cellen functioneren als sterkere enhancers (versterkers), maar niet in niet-gerelateerde celtypes. Biochemische bindingsassays verklaarden waarom: de risicovorm van de ene variant verzwakt de binding van REST, een eiwit dat gewoonlijk genactiviteit dempt, terwijl de risicovorm van de andere variant de binding van POLR2A versterkt, een kernonderdeel van het afleesmachinerie van genen. Samen vergroten deze verschuivingen in eiwitbinding de activiteit van de enhancersegmenten en verhogen ze de expressie van RERE.
Van verhoogd RERE naar veranderde hersencelgroei
Vervolgens onderzochten de onderzoekers wat extra RERE in de hersenen doet. Ze vonden dat mensen die overleden met schizofrenie hogere RERE-niveaus in hun hersenweefsel vertoonden vergeleken met niet-getroffen personen. Om dit te modelleren, verhoogden ze kunstmatig RERE-niveaus in muis-neurale stamcellen—de onrijpe cellen die neuronen en gliacellen voortbrengen. Wanneer RERE overgeproduceerd werd, deelden deze stamcellen minder, bleven ze vastzitten in een laat stadium van de celcyclus en produceerden ze minder rijpe neuronen terwijl andere celtijpen grotendeels ongewijzigd bleven. In gekweekte neuronen veranderde teveel RERE ook hun vertakkingspatronen en verminderde het aantal en het type kleine uitsteeksels, dendritische spines genoemd, waar synapsen ontstaan. Deze veranderingen passen bij lang bestaand bewijs dat schizofrenie gepaard gaat met verstoorde hersenontwikkeling en verlies van spines. 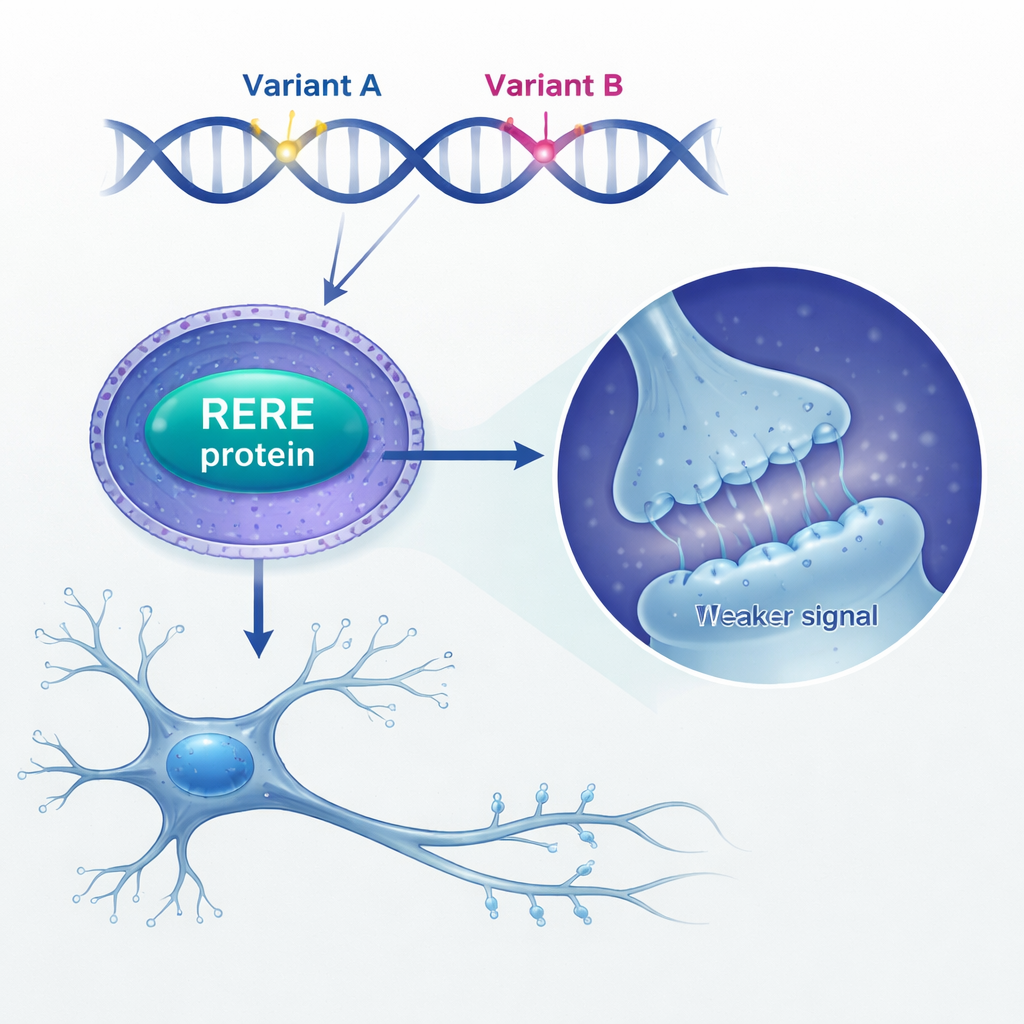
Het verstoren van het glutamaat-"gesprek" in de hersenen
Bij nadere bestudering van genactiviteit vonden de onderzoekers dat RERE-overexpressie netwerken van genen verstoorde die betrokken zijn bij dendrietgroei en belangrijke chemische signaalroutes, vooral de glutamaatweg. Eén belangrijk doelwit sprong eruit: het gen GRIN2A, dat een cruciale subunit (GluN2A) van NMDA-type glutamaatreceptoren codeert, lang in verband gebracht met schizofrenie. De auteurs toonden aan dat RERE samenwerkt met twee andere nucleaire eiwitten, RARB en RXRA, om direct te binden aan de promotor van GRIN2A en diens activiteit te dempen. In neuronen met te veel RERE daalden de GluN2A-niveaus en lieten elektrische opnamen zwakkere NMDA-receptorgemedieerde synaptische stromen zien, ook al bleef de frequentie van synaptische gebeurtenissen ongewijzigd. Met andere woorden: het “volume” van individuele exciterende signalen werd omlaag gezet.
Het verbinden van DNA-varianten met hersenfunctie
Door genetica, moleculaire biologie, celkweek en elektrofysiologie samen te brengen, schetst dit werk een duidelijke causale keten: risico-DNA-varianten op 1p36.23 versterken regulatorische elementen binnen het RERE-gen, wat leidt tot hogere RERE-expressie in hersencellen. Verhoogde RERE verstoort op zijn beurt de groei en rijping van neuronen, verandert de vorm en het aantal synaptische spines en verzwakt glutamaat-gebaseerde signalering via NMDA-receptoren—vooral die met GluN2A. Voor de niet-specialist is de kernboodschap dat zeer kleine DNA-veranderingen de activiteit van één gen licht kunnen verschuiven, en dat dit, over vele hersencellen en vele jaren, de hersenontwikkeling en communicatie net genoeg kan ontregelen om bij te dragen aan schizofrenie.
Bronvermelding: Liu, Y., Wang, J., Yang, H. et al. Functional variants at 1p36.23 confer risk of schizophrenia through modulating RERE. Nat Commun 17, 1742 (2026). https://doi.org/10.1038/s41467-026-68449-6
Trefwoorden: genetica van schizofrenie, RERE-gen, neurale ontwikkeling, glutamaat-signaalgeving, synaptische functie