Clear Sky Science · nl
Verbeteren van erectiele functie bij mannelijke diabetische muizen door herstel van depalmitoyleerd FBP1 om cavernieuze lactaat te verminderen
Waarom dit belangrijk is voor mannen met diabetes
Erectieproblemen komen veel voor bij mannen met diabetes: ze treden vaak eerder op en reageren slecht op standaardmiddelen zoals Viagra. Deze muizenstudie onthult een verrassende boosdoener: een ophoping van melkzuur (lactaat) in het erectieweefsel van de penis. De onderzoekers volgen niet alleen hoe die ophoping het weefsel schaadt, maar testen ook een experimentele RNA-gebaseerde therapie ingebed in kleine vetbolletjes die de erectiele functie herstelt. Hun werk suggereert een toekomst waarin de behandeling van diabetische erectiestoornissen de onderliggende stofwisseling herstelt, in plaats van slechts tijdelijk de bloedstroom te vergroten.
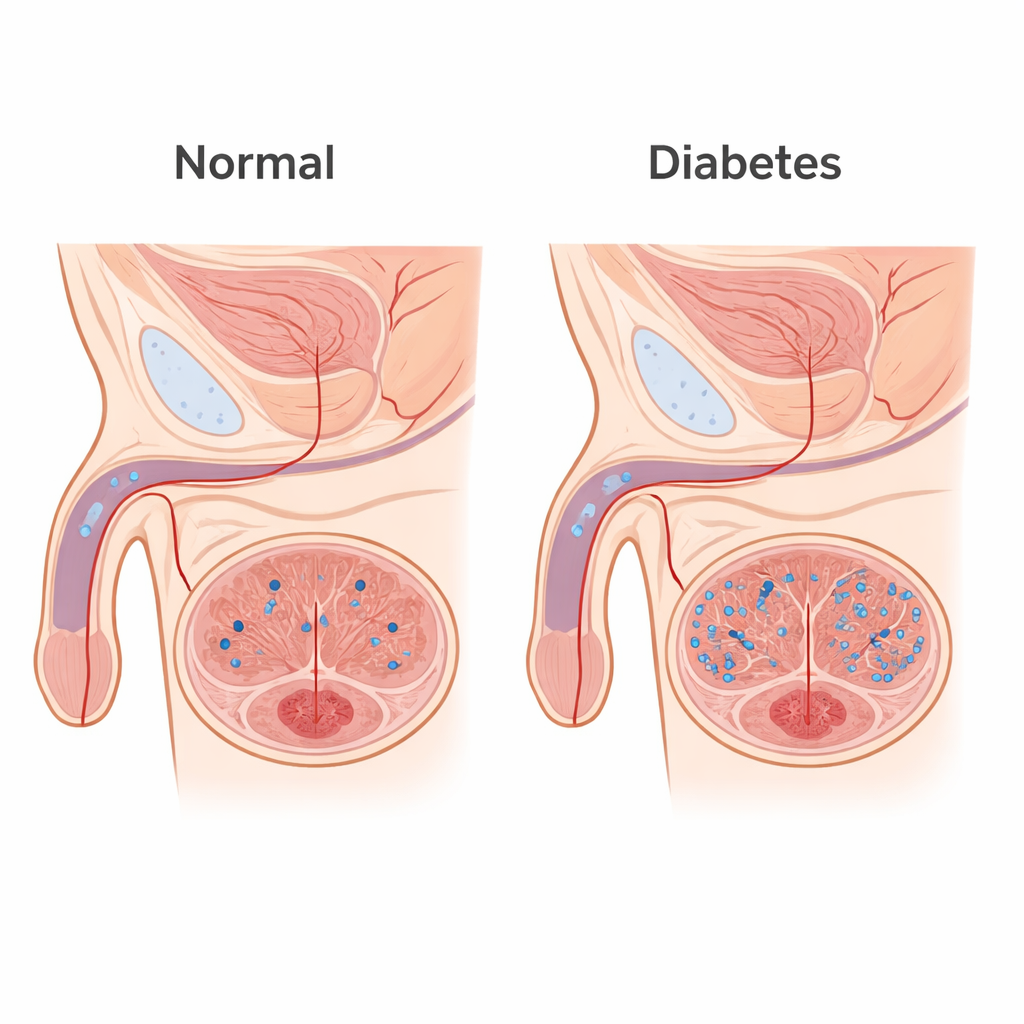
Van energieverspilling naar weefselschade
Lactaat wordt vaak gezien als eenvoudig “afval” van hardwerkende spieren, maar het is ook een krachtig signaalmolecuul. Bij mannen met diabetes-gerelateerde erectiestoornissen vonden de auteurs hogere lactaatniveaus in het bloed dan bij leeftijdsgepaste controles. In een diabetisch muismodel nam het lactaat in het sponsachtige erectieweefsel van de penis (corpus cavernosum) geleidelijk toe, terwijl de tijdens een erectie gegenereerde druk afnam. Gezonde muizen die extra lactaat kregen, stapelden lactaat op in het peniele weefsel, kregen lagere erectiedruk en microscopisch onderzoek toonde verlies van glad spierweefsel en meer collageenzwelling. In gekweekte gladde spiercellen van de penis vertraagde hoog lactaat de cellulaire verplaatsing en schoof de cellen van een contractiele, “werkklare” toestand naar een synthetische, littekenvormende toestand, deels door overactivering van zelfafbraakpaden die bekendstaan als autofagie.
Een sleutelenzym verdwijnt
Om te begrijpen waarom lactaat opstapelt, vergeleek het team genen die betrokken zijn bij twee tegengestelde energiepaden: glycolyse, die lactaat produceert, en gluconeogenese, die lactaat terugrekent naar glucose. Ze zagen geen aanwijzingen dat glycolyse overactief was. In plaats daarvan was een centraal gluconeogenisch enzym, FBP1, consequent verminderd in penisweefsel van diabetische muizen, diabetische ratten en in single-cell data van menselijke mannen met diabetes-gerelateerde erectiestoornissen. Toen de onderzoekers Fbp1 genetisch verlaagden in muizen, steeg het lactaat in de penis en verslechterde de erectiele prestatie, zelfs onder relatief lage lactaatcondities. In gladde spiercellen hielp het terugbrengen van werkend FBP1 beschermen tegen de schadelijke effecten van hoog lactaat, terwijl een inactieve FBP1-variant dat niet deed. Dit toonde aan dat de enzymatische activiteit van FBP1 cruciaal is om lactaat in toom te houden en gezond erectieweefsel te behouden.
Epigenetische sloten en vette “tags” op FBP1
Waarom is FBP1 in diabetes verminderd? De studie onthult een dubbel controlemechanisme. Ten eerste wordt het Fbp1-gen op DNA-niveau dichtgeknepen. Chemische merken op histon-eiwitten—specifiek twee “uit”-schakelaars genaamd H3K9me3 en H3K27me3—stapelen zich op bij de Fbp1-promotor in diabetisch penisweefsel. Deze merken worden geschreven door enzymen zoals SUV39H1 en EZH2 en gelezen door een eiwit genaamd CBX3, die samen een represserend complex vormen dat Fbp1 uitgeschakeld houdt. Geneesmiddelen en ontworpen degrader-moleculen die deze enzymen richten, konden deze repressie in cellen gedeeltelijk opheffen maar leverden slechts bescheiden verbeteringen bij diabetische muizen. Ten tweede kan, zelfs wanneer het FBP1‑eiwit aanwezig is, het worden uitgeschakeld door een vetachtige modificatie genaamd palmitoylering op één aminozuur, Cys282. Het team identificeerde het enzym ZDHHC13 als de palmitoyltransferase die deze vetgroep toevoegt. Palmitoylering verandert subtiel de vorm van FBP1 nabij een kritisch residu, waardoor het vermogen om lactaat te verwerken wordt afgezwakt. Het blokkeren van Zdhhc13 in cellen en muizen verbeterde de stofwisseling en erectiele functie slechts gedeeltelijk, wat benadrukt dat noch epigenetische medicijnen noch palmitoyleringsblokkers op zichzelf voldoende zijn.
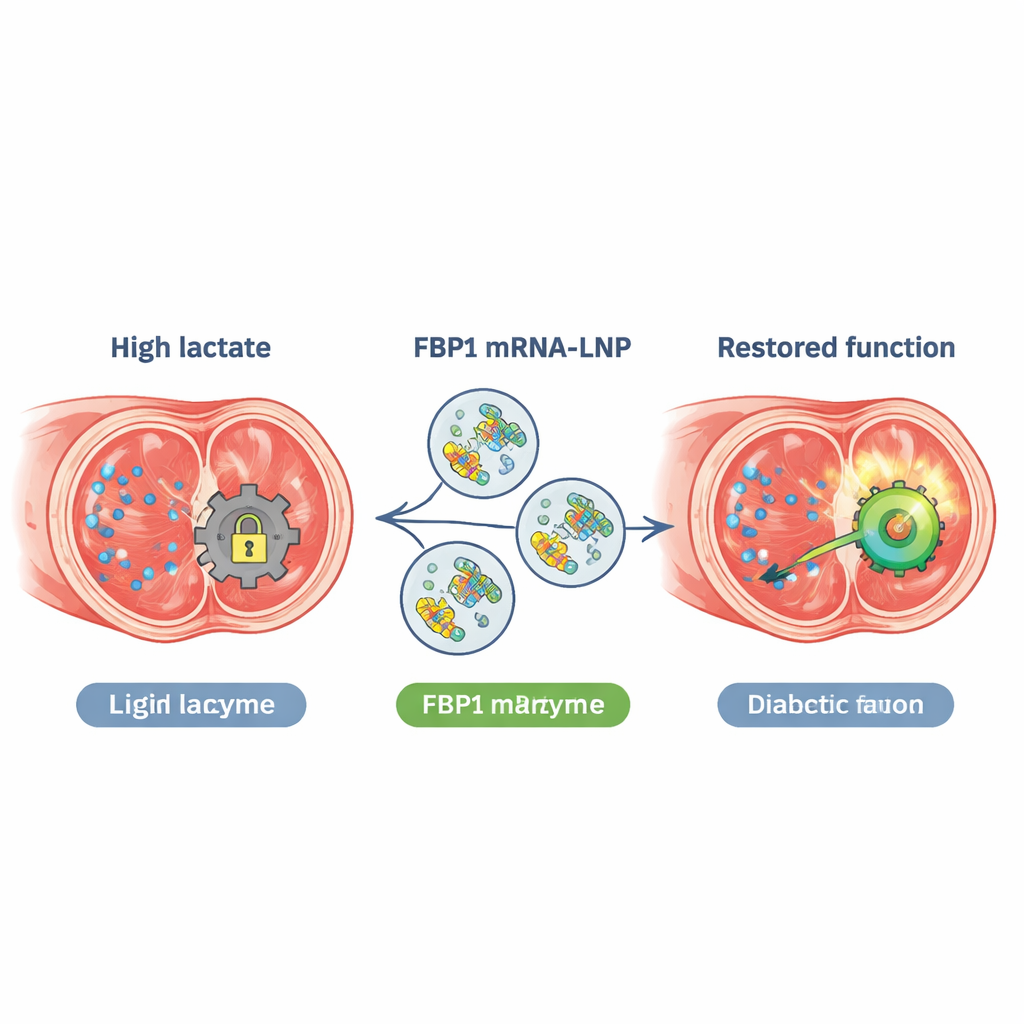
RNA-gevulde nanodeeltjes als reparatieset
Om beide problemen tegelijk aan te pakken, ontwikkelden de onderzoekers een mRNA dat codeert voor een palmitoyleringsbestendige Fbp1-mutant (C282S) en verpakte dit in lipide-nanodeeltjes—vergelijkbaar in opzet met mRNA-COVID-19-vaccins. Direct in het peniele weefsel van diabetische muizen geïnjecteerd, werden deze deeltjes efficiënt opgenomen door gladde spiercellen. De behandelde muizen toonden hogere FBP1-eiwitniveaus, sterk lagere cavernieuze lactaatwaarden, betere erectiedruk, meer glad spierweefsel en minder fibrose. Een middeldosis werkte het best; hogere doseringen boden geen extra voordeel. De therapie normaliseerde ook de overactieve autofagie die in diabetesmodellen werd gezien en verbeterde erectiele uitkomsten in meerdere typen diabetische muizen, zonder duidelijke lever- of niertoxiciteit gedurende de studieduur.
Wat dit kan betekenen voor toekomstige behandelingen
Eenvoudig gezegd herkaderen deze bevindingen problematische erecties bij diabetes als een probleem van “zure” stofwisseling in de penis: te veel lactaat en te weinig functioneel FBP1. Door een niet-palmitoylerende, actieve versie van FBP1 precies daar terug te brengen waar het nodig is, herstelt de mRNA–nanodeeltje-therapie het energiebalans van het weefsel, behoudt glad spierweefsel en maakt het mogelijk dat normale erecties terugkeren—althans bij muizen. Terwijl veel vragen blijven over langetermijnveiligheid, dosering en vertaling naar mensen, wijst de studie op een nieuwe klasse behandelingen die de metabole gezondheid van erectieweefsel herbouwen en mogelijk op termijn patiënten kunnen helpen die niet reageren op huidige geneesmiddelen.
Bronvermelding: Xiao, M., Guo, W., Zeng, R. et al. Improving erectile function in diabetic male mice by rescuing depalmitoylated FBP1 to reduce cavernosal lactate. Nat Commun 17, 1740 (2026). https://doi.org/10.1038/s41467-026-68443-y
Trefwoorden: diabetische erectiestoornis, lactaatmetabolisme, FBP1-enzym, lipide-nanodeeltje mRNA-therapie, peniele gladde spier