Clear Sky Science · nl
Verbeterde in vivo genuitval met hoge specificiteit door gebruik van meervoudige Cas12a-sgRNA's
Genen betrouwbaarder bewerken
Genbewerking belooft nieuwe manieren om biologie te bestuderen, ziektes te behandelen en zelfs insectenplagen te bestrijden, maar in levende dieren werkt het vaak minder schoon dan krantenkoppen doen geloven. Veel cellen ontsnappen aan bewerking of worden slechts gedeeltelijk gewijzigd, wat experimentele uitkomsten kan vertroebelen en het gebruik in de praktijk beperkt. Dit artikel beschrijft een nieuwe CRISPR-gebaseerde methode in fruitvliegjes die genuitvals gebeurtenissen vollediger en preciezer maakt, en biedt een blauwdruk voor betrouwbaardere genoombewerking in complexe organismen.
Waarom standaard-CRISPR vaak tekortschiet
Traditionele CRISPR-instrumenten zoals Cas9 knippen DNA op een gekozen plek met één of een klein aantal gids-RNA's. In levende dieren stuit deze aanpak op verschillende hindernissen. Sommige gidsen werken eenvoudigweg slecht; sommige doelplaatsen zijn moeilijk bereikbaar voor het enzym; en het herstelmechanisme van de cel „herstelt" de breuk vaak met kleine veranderingen die het gen alsnog functioneel laten. Het resultaat is een mozaïek: aangrenzende cellen in hetzelfde weefsel kunnen verschillende mutaties of helemaal geen mutatie dragen. Die ongelijkmatigheid bemoeilijkt het vaststellen wat er gebeurt wanneer een gen echt uitgeschakeld is en vormt een uitdaging voor toepassingen zoals gentherapie of gen-drives die in de meeste cellen efficiënt moeten werken.
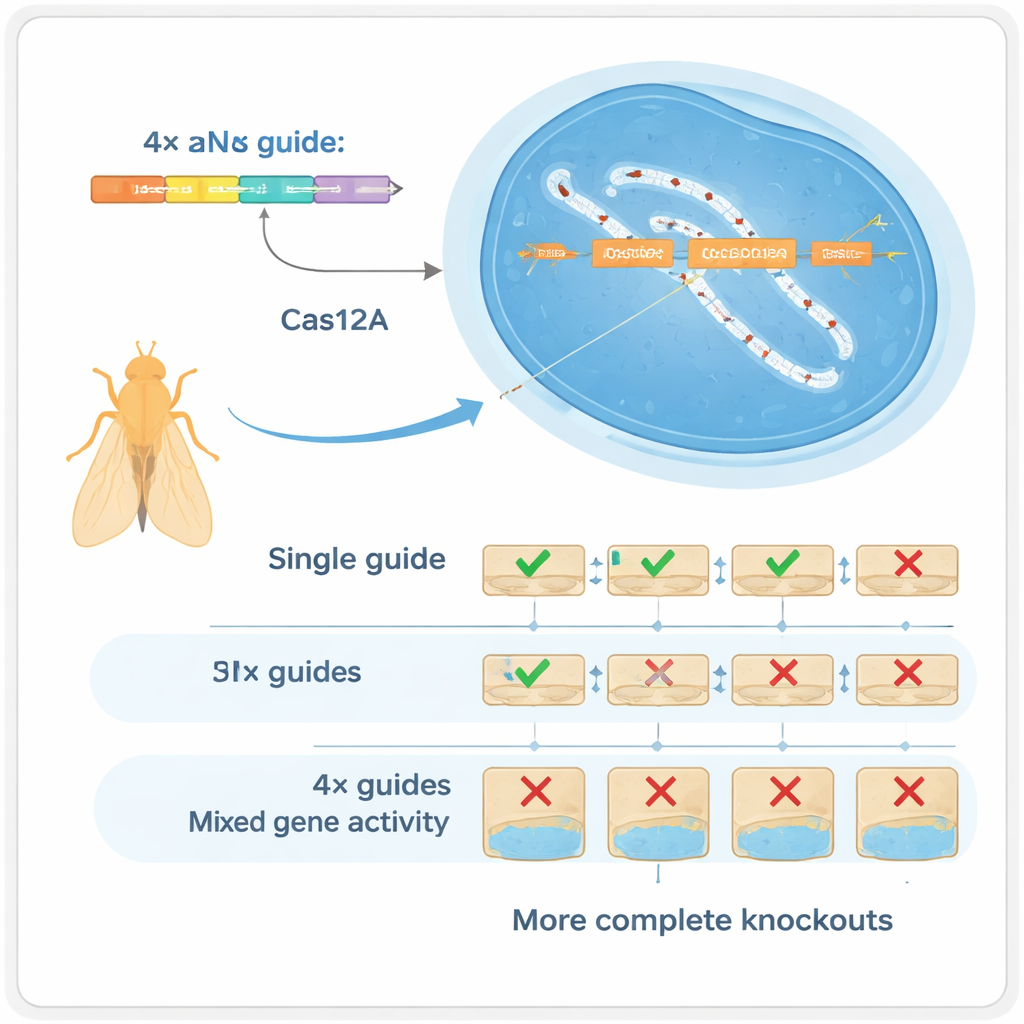
Vier gidsen zijn beter dan één
De auteurs schakelden over op een ander CRISPR-enzym, Cas12a, dat compacte arrays van gidsen veel gemakkelijker kan verwerken dan Cas9. Ze bouwden een Drosophila-toolkit waarin elk gen wordt gericht door een array van vier gids-RNA's, allemaal gecodeerd op één klein DNA-fragment dat in massa geproduceerd kan worden. In zorgvuldig gecontroleerde testen toonden ze aan dat het gebruik van vier gidsen per gen de soorten DNA-veranderingen drastisch verandert: in plaats van voornamelijk kleine inserties of deleties op één plaats, creëert het systeem vaak grotere deleties tussen knipplaatsen die vrijwel altijd de genfunctie vernietigen. Deze "multiplexing" werkt op twee manieren: als één gids faalt kunnen anderen het werk nog doen (redundantie), en wanneer meerdere tegelijk knippen kunnen ze grotere stukken van het gen weghalen (synergie).
Hoge efficiëntie zonder extra nevenschade
Meer DNA-breuken creëren roept begrijpelijke veiligheidsvragen op. Zouden meerdere knippen in één regio per ongeluk nabijgelegen genen kunnen wissen? Zou er vaker sprake kunnen zijn van ongewenste knipactiviteiten elders in het genoom? Om dit te onderzoeken maten de onderzoekers celdood, onderzochten ze effecten op naburige genen en ontwikkelden ze een slimme test om chromosomaal herstel zichtbaar te maken, loss of heterozygosity, over grote DNA-streken. Ze vonden dat het clusteren van vier knippen binnen één gen goed werd verdragen: het verhoogde de celdood niet vergeleken met conventionele Cas9-benaderingen en verstoorde zelden naburige genen, tenzij een gids extreem dicht bij een regulatoir element terechtkwam. Grootschalige screenings met meer dan 2.000 gidsen over een derde van het vliegen-genoom toonden dat meer dan 99% van de gids-arrays actief was op het beoogde doel, terwijl reproduceerbare off-target activiteit onder de 1% lag, wat wijst op zeer hoge specificiteit zelfs in een gemultiplexte opzet.
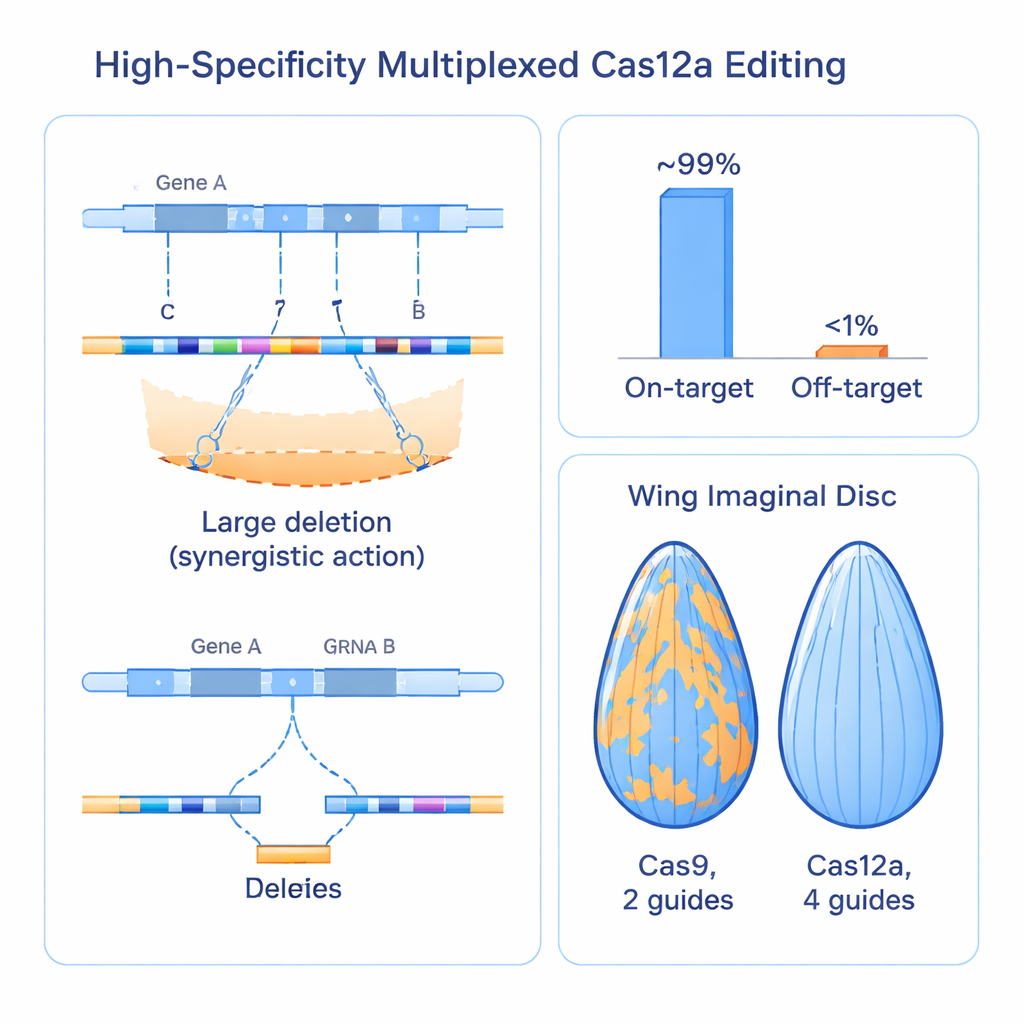
Cas12a-systemen overtreffen gevestigde Cas9-systemen in echte weefsels
Om te zien of deze moleculaire verbeteringen zich vertalen naar helderder biologie, vergeleek het team hun Cas12a–vier-gids systeem direct met veelgebruikte Cas9-bronnen die meer dan 100 genen in de vlieg richten. In weefsels zoals het oog, de darm en de ontwikkelende vleugel produceerde de Cas12a-aanpak sterkere en meer uniforme verlies-van-functie effecten dan Cas9, dat vaak duidelijke plekken met ongewijzigd, normaal weefsel achterliet. Toen ze vleugelgrootte als kwantitatieve maat gebruikten, genereerde het nieuwe systeem consequent grotere en beter reproduceerbare groeidefecten voor bekende regulatoren, wat aantoonde dat sommige genen die eerder als zwak of niet-essentieel werden aangemerkt in feite gemist waren omdat oudere hulpmiddelen ze niet grondig genoeg inactiveerden. De verhoogde kracht van de methode onthulde zelfs een eerder onbekende, essentiële rol voor een gen genaamd trade embargo in vleugelontwikkeling en overleving.
Wat dit betekent voor toekomstige genbewerking
In eenvoudige bewoordingen laat dit werk zien hoe je CRISPR kunt omvormen van een soms rommelig scalpel tot een beslissender schakel om genen uit te schakelen in levende dieren. Door Cas12a te combineren met vier gidsen per gen bereiken de auteurs bijna volledige knock-outs met zeer weinig onbedoelde effecten, alles in een formaat dat praktisch te schalen is over honderden genen. Hoewel ontwikkeld in fruitvliegjes, zijn de onderliggende principes — het gebruik van meerdere gidsen voor redundantie en synergie, en het zorgvuldig controleren op chromosomale neveneffecten — breed toepasbaar. Deze strategie kan fundamenteel onderzoek verbeteren, genetische screens aanscherpen en bijdragen aan veiligere ontwerpen voor toekomstige medische en ecologische toepassingen van genbewerking.
Bronvermelding: Port, F., Buhmann, M.A., Zhou, J. et al. Improved in vivo gene knockout with high specificity using multiplexed Cas12a sgRNAs. Nat Commun 17, 877 (2026). https://doi.org/10.1038/s41467-026-68434-z
Trefwoorden: CRISPR, Cas12a, genuitval, Drosophila, specificiteit van genoombewerking