Clear Sky Science · nl
Controle van telomerase-rekrutering en eindbescherming door onafhankelijke shelterin-componenten
Hoe cellen hun chromosoomeinden veilig houden
Elke keer dat een cel zich deelt, worden de uiterste uiteinden van haar chromosomen — telomeren genoemd — een beetje korter. Om te voorkomen dat belangrijke genetische informatie verloren gaat, gebruiken cellen een speciaal enzym, telomerase, en een groep beschermende eiwitten om deze uiteinden te onderhouden. Deze studie onderzoekt hoe twee van die eiwitten, TPP1 en POT1, het delicate evenwicht beheersen tussen het binnenlaten van telomerase om telomeren te vernieuwen en het veilig afgesloten houden van chromosoomeinden tegen schade.
Het probleem van verouderende chromosoomeinden
Telomeren functioneren als plastic dopjes op veters en voorkomen dat chromosomen rafelen of worden aangezien voor beschadigd DNA. Als een cel een chromosoomeinde verkeerd interpreteert als schade, kan dat nooddiensten voor reparatie activeren die chromosomen aan elkaar lijmen of de cel stoppen met delen. Tegelijkertijd moeten telomeren af en toe open kunnen gaan zodat telomerase ze kan verlengen, vooral in stamcellen die vaak delen. Biologen zagen lang voor zich dat telomeren konden schakelen tussen een “gesloten” beschermde toestand en een “open” toestand die telomerase toegang geeft maar tijdelijke schade-signalen risico loopt. Of deze twee toestanden verschillende fysieke vormen van het telomeer weerspiegelen of echt afzonderlijke regelmechanismen zijn, bleef een open vraag.
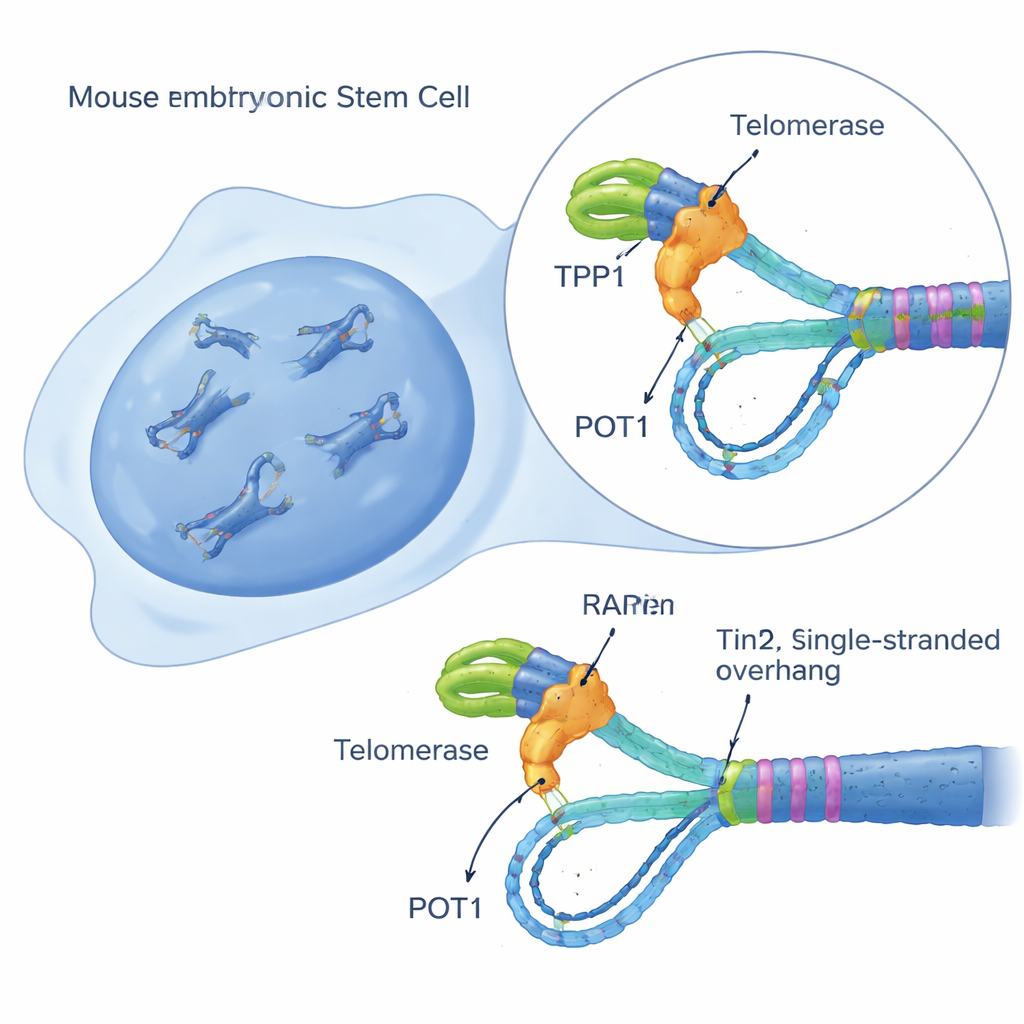
Een sensor voor telomerase-activiteit in enkele cellen bouwen
Om dit raadsel te ontrafelen creëerden de onderzoekers een gevoelige test in levende cellen, iTAP (induceerbare Telomerase Activity Probing), in muis-embryonale stamcellen. Ze ontwierpen de cellen zo dat ze een iets gewijzigde versie van het telomerase-RNA-template produceerden alleen wanneer ze het middel doxycycline kregen. Dit “gemuteerde” template zorgt ervoor dat telomerase een aangepast DNA-sequentie aan telomeren toevoegt die visueel te onderscheiden is van normaal telomeer-DNA. Met fluorescerende probes, DNA-blots en een sequenstechiek die telomeerfragmenten verrijkt, kon het team direct, cel voor cel, zien wanneer en waar telomerase actief was. Cruciaal was dat dit systeem de celgroei niet schaadde en op zichzelf geen schade-respons uitlokte, waardoor zuivere metingen van telomerase-gedrag in anderszins gezonde cellen mogelijk waren.
TPP1 haalt telomerase binnen, POT1 houdt het tegen
Gewapend met iTAP onderzochten de auteurs hoe twee sleutelproteïnen van telomeren, TPP1 en POT1, bijdragen aan telomerase-activiteit. Beide behoren tot een groter complex dat bekendstaat als shelterin, dat telomeren omsluit. Toen ze TPP1 verwijderden met genbewerkingstools, verdwenen de gemuteerde telomeersequenties vrijwel geheel, hoewel het gemuteerde telomerase-RNA nog normaal geproduceerd werd. Verdere experimenten lieten zien dat TPP1 fysiek met een andere shelterin-component, TIN2, verbonden moet zijn om telomerase te rekruteren; het verstoren van TPP1’s verbinding met TIN2 schakelde de telomerase-activiteit uit. Verrassend genoeg had het verbreken van TPP1’s interactie met POT1 dat effect niet, en het verwijderen van POT1 zelf verminderde de telomerase-activiteit niet. Sterker nog, cellen zonder POT1 vertoonden een bescheiden toename van de toegevoegde gemuteerde sequentie, wat suggereert dat POT1 normaal fungeert als een rem — het beperkt hoe vaak telomerase zich aan telomeren bindt, in plaats van het te helpen.
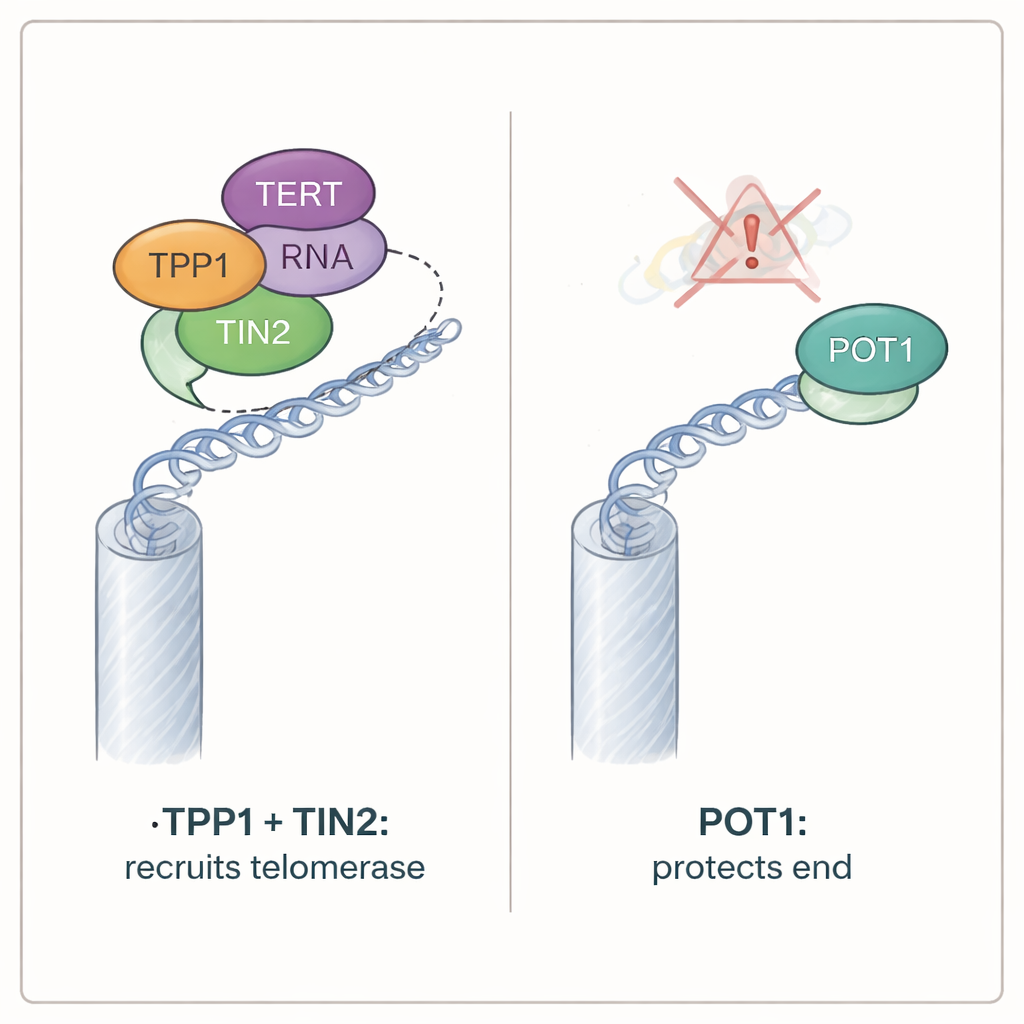
POT1 bewaakt de uiteinden, terwijl TPP1 soms overbodig kan zijn
Hoewel POT1 niet nodig was voor de rekrutering van telomerase, bleek het essentieel voor het beschermen van chromosoomeinden. Cellen die beide versies van POT1 in muizen misten, stopten snel met prolifereren en vertoonden alle kenmerken van blootgestelde telomeren: DNA-schademarkers stapelden zich op bij chromosoomtips, een schade-sensorend enzym genaamd ATR werd geactiveerd, en chromosoomeinden fuseerden. Daarentegen bleven cellen zonder TPP1 doorgroeien en toonden ze weinig tekenen van telomeer-stress, ondanks dat ze normale telomerase-activiteit waren kwijtgeraakt. Aanvullende tests toonden aan dat POT1’s verdedigende rol afhangt van zijn vermogen het enkelstrengige overhang bij telomeren te binden. Gemuteerde POT1-eiwitten die dit blootgestelde DNA niet langer konden grijpen, faalden in het onderdrukken van schadesignalen, zelfs als ze nog met TPP1 konden interageren. Omgekeerd beschermden varianten van POT1 die het overhang konden binden maar niet langer aan TPP1 hechtten, wel de chromosoomeinden.
Een nieuw, modulair beeld van telomeercontrole
Deze bevindingen doorbreken het eenvoudige beeld van telomeren die schakelen tussen één “open” toestand voor telomerase en één “gesloten” toestand voor bescherming. In plaats daarvan laat de studie zien dat de rekrutering van telomerase en de eindbescherming worden geregeld door aparte moleculaire circuits. TPP1, werkend via TIN2, is de belangrijkste poort die telomerase naar telomeren brengt, terwijl POT1 onafhankelijk het blootgestelde DNA aan chromosoomeinden bewaakt en schadereacties onderdrukt. Voor een niet-specialist is de conclusie dat cellen niet vertrouwen op één universele schakel aan chromosoomtips. In plaats daarvan gebruiken ze afzonderlijke maar gecoördineerde knoppen — één om telomerase binnen te laten en een andere om de uiteinden veilig te houden — om de genoomstabiliteit levenslang te behouden.
Bronvermelding: Sandhu, R., Tricola, G.M., Lee, S.Y. et al. Control of telomerase recruitment and end protection by independent shelterin components. Nat Commun 17, 1733 (2026). https://doi.org/10.1038/s41467-026-68433-0
Trefwoorden: telomeren, telomerase, stamcellen, DNA-schade, chromosoombescherming