Clear Sky Science · nl
Dynamisch allelegebruik van X-gebonden genen verzacht neuroontwikkelingsziektefenotypes in hersenorganoïden
Hoe het “stille” X-chromosoom de hersenen helpt beschermen
Elke cel van een vrouw bevat twee X-chromosomen, maar decennialang zeiden biologieteksten dat één daarvan grotendeels uitgeschakeld is—als een reserveboek dat gesloten op een plank ligt. Deze studie toont aan dat dat “stille” X, vooral in de zich ontwikkelende hersenen, meer lijkt op een dynamische back-uplibrary. Hij kan worden aangesproken wanneer dat nodig is, en die extra flexibiliteit kan helpen verklaren waarom veel aandoeningen van de hersenontwikkeling mannen zwaarder treffen dan vrouwen.
Een verborgen backupsysteem op het X-chromosoom
Bij vrouwelijke zoogdieren wordt vroeg in de ontwikkeling één X-chromosoom in elke cel uitgeschakeld om een dubbele dosis X-gebonden genen te voorkomen. Wetenschappers weten echter al lang dat sommige genen aan deze uitschakeling weten te ontsnappen. De nieuwe studie stelt een dieperliggende vraag: is dat ontsnappen vastliggend, of kan het veranderen naarmate cellen zich ontwikkelen? Met behulp van menselijke stamcellen en mini-hersenweefsels genaamd organoïden volgden de onderzoekers welke kopie van elk X-gebonden gen—moederlijk of vaderlijk—werd gebruikt toen cellen zich ontwikkelden van stamcel tot zenuwcel. Ze ontdekten dat veel genen op het verondersteld inactieve X aan- en uitgaan op een stadium- en celtype-specifieke manier, in plaats van volgens een eenvoudige aan/uit-regel.
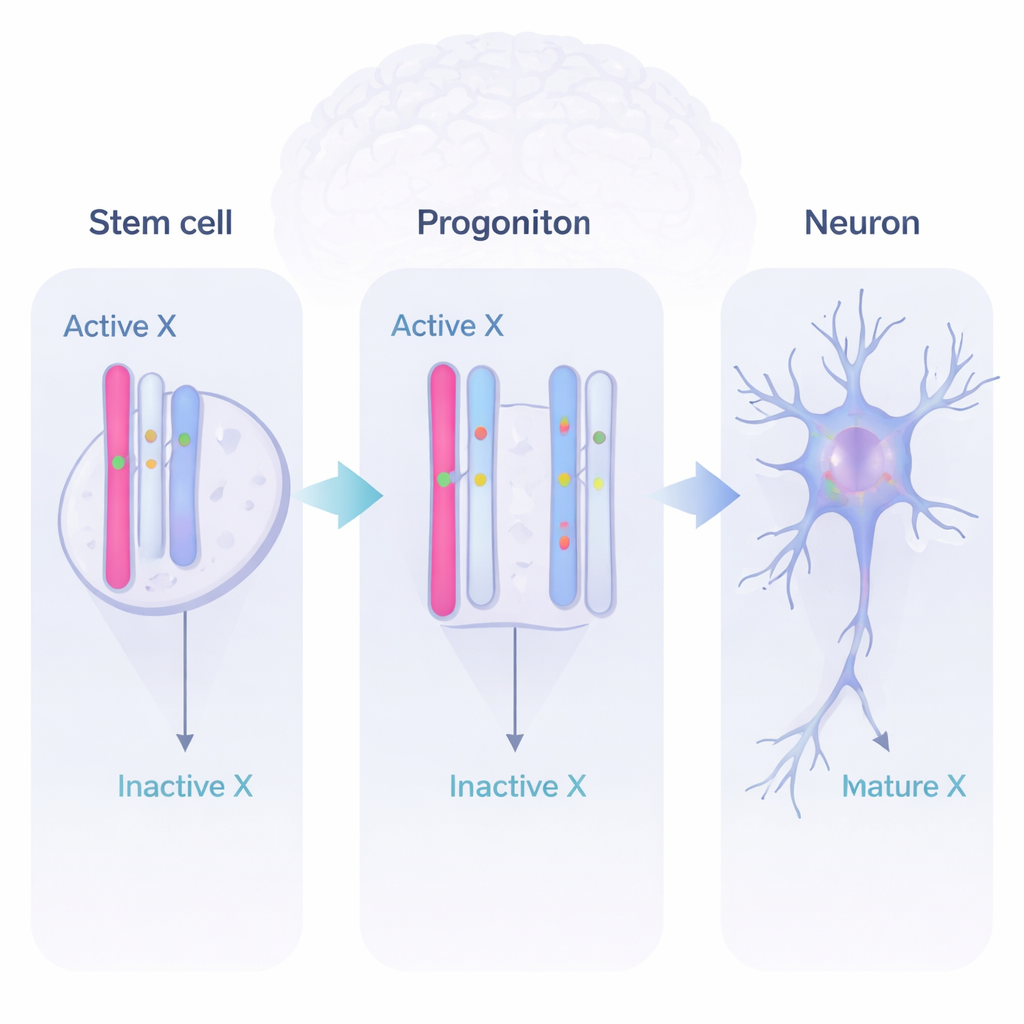
Dynamisch gengebruik tijdens hersenontwikkeling
Door RNA af te lezen (de boodschappen die van genen worden gemaakt) en onderscheid te maken tussen de twee ouderlijke kopieën, ontdekte het team drie hoofdgedragingen. Sommige genen bleven, zoals verwacht, grotendeels uitgeschakeld op het inactieve X. Andere waren “volledige ontsnappers”, actief vanaf beide X-kopieën in alle stadia. Het meest intrigerend was een aanzienlijke groep dynamische genen. Deze genen waren stil op het inactieve X in stamcellen, schakelden aan vanaf beide X-chromosomen in neurale progenitorcellen en vroege neuronen, en schakelden later weer gedeeltelijk uit. Dit laat zien dat het inactieve X geen statische grafkelder van genen is, maar een flexibel reservoir waar de ontwikkelende hersenen op kunnen terugvallen wanneer extra genactiviteit nuttig is.
Behouden patronen en verbanden met hersenaandoeningen
Toen de onderzoekers hun menselijke gegevens vergeleken met muisstudies en met chemische markers op DNA uit foetaal hersenweefsel, vonden ze dat dit dynamische ontsnappen aan X-inactivatie ook bij andere zoogdieren voorkomt en samenhangt met chromatine-statussen—kenmerken van de DNA-verpakking die bepalen hoe gemakkelijk genen kunnen worden aangezet. De heractiverende genen hadden de neiging te clusteren in bepaalde regio’s van het X-chromosoom en droegen epigenetische signalen van actief DNA specifiek in vrouwelijk hersenweefsel. Belangrijk voor de geneeskunde is dat deze dynamisch heractiveerde genen opvallend rijk waren aan bekende risicogenen voor neuro-ontwikkelingsstoornissen zoals verstandelijke beperking en autisme-spectrumstoornissen, wat suggereert dat deze flexibiliteit zich heeft ontwikkeld als een beschermend mechanisme.
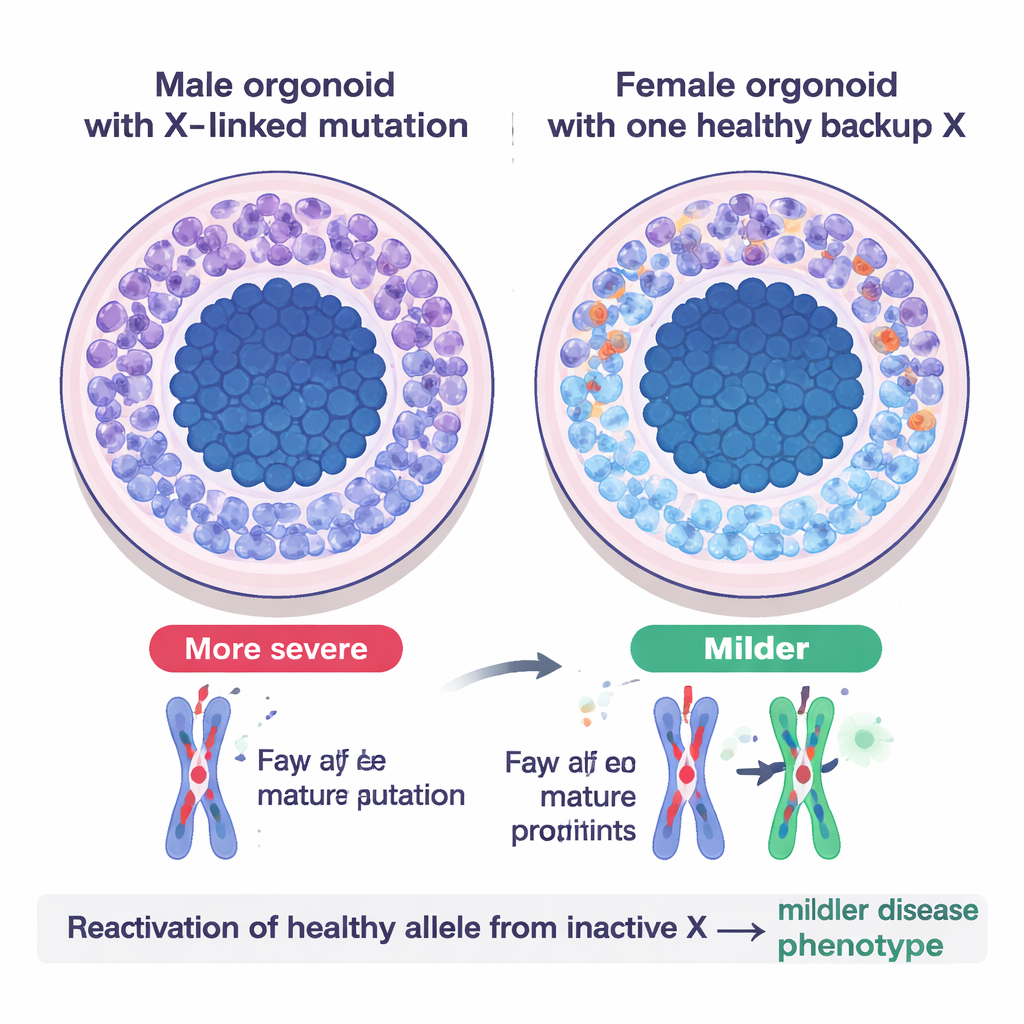
Een praktijktest: Opitz BBB/G-syndroom
Om te zien hoe dit backupsysteem zich in ziekte uitwerkt, modelleerde het team het Opitz BBB/G-syndroom, een zeldzame X-gebonden aandoening die middenlijnstructuren van de hersenen aantast en vaak ontwikkelingsachterstand veroorzaakt. De aandoening wordt veroorzaakt door schadelijke mutaties in een gen genaamd MID1 op het X-chromosoom. In hersenorganoïden gekweekt uit cellen van mannelijke patiënten—waar slechts één X-kopie aanwezig is—waren neuronen schaars en bleven neurale stamcellen te lang in een delende toestand, hetgeen echoot van de onderontwikkeling van de hersenen die bij patiënten wordt gezien. Vrouwelijke organoïden met dezelfde mutatie op hun actieve X, maar een gezonde kopie op het inactieve X, zagen er merkbaar gezonder uit: ze produceerden meer neuronen en hadden mildere defecten. Toen wetenschappers vrouwelijke lijnen zo manipuleerden dat beide X-kopieën de mutatie droegen, ontwikkelden de organoïden ernstige, mannelijke-achtige problemen, wat bevestigt dat het eerder inactieve gezonde allel was heractiverend en hielp compenseren.
Wat dit betekent voor geslachtsverschillen bij hersenziekten
De studie toont aan dat het tweede, “stille” X-chromosoom bij vrouwen niet louter genetische ballast is. Tijdens cruciale vensters van hersenontwikkeling schakelen geselecteerde genen op dit inactieve X aan in specifieke celtypen, waardoor het aantal functionele genkopieën toeneemt. Voor genen zoals MID1, die essentieel zijn voor de bouw van de hersenen, kan deze dynamische heractivering de impact van schadelijke mutaties verzachten en mildere, meer variabele symptomen bij vrouwen veroorzaken. Met andere woorden: vrouwelijke hersenen beschikken over een intern backupsysteem dat in de loop van de tijd kan worden op- of bijgesteld, wat helpt verklaren waarom veel X-gebonden neuro-ontwikkelingsstoornissen minder vaak voorkomen of minder ernstig zijn bij meisjes dan bij jongens.
Bronvermelding: Bertin, M., Todorov, H., Frank, S. et al. Dynamic allele usage of X-linked genes ameliorates neurodevelopmental disease phenotypes in brain organoids. Nat Commun 17, 599 (2026). https://doi.org/10.1038/s41467-026-68428-x
Trefwoorden: inactivering van het X-chromosoom, hersenorganoïden, neuro-ontwikkelingsstoornissen, gen-dosering, geslachtsverschillen in ziekte