Clear Sky Science · nl
Shigella flexneri ontloopt septine-gemedieerde cel-autonome immuniteit via eiwit-ADP-riboxanatie
Hoe sommige darmbacteriën ons interne beveiligingssysteem passeren
Ernstige diarree door Shigella-bacteriën blijft wereldwijd een groot probleem, vooral bij jonge kinderen. Onze cellen zijn niet weerloos: ze beschikken over ingebouwde middelen die binnendringende microben kunnen vangen en vernietigen. Deze studie onthult hoe Shigella flexneri, een belangrijke veroorzaker van dysenterie, slimme moleculaire trucs gebruikt om één van deze middelen te ontmantelen, waardoor de bacterie zich van cel naar cel in de darm kan verspreiden.
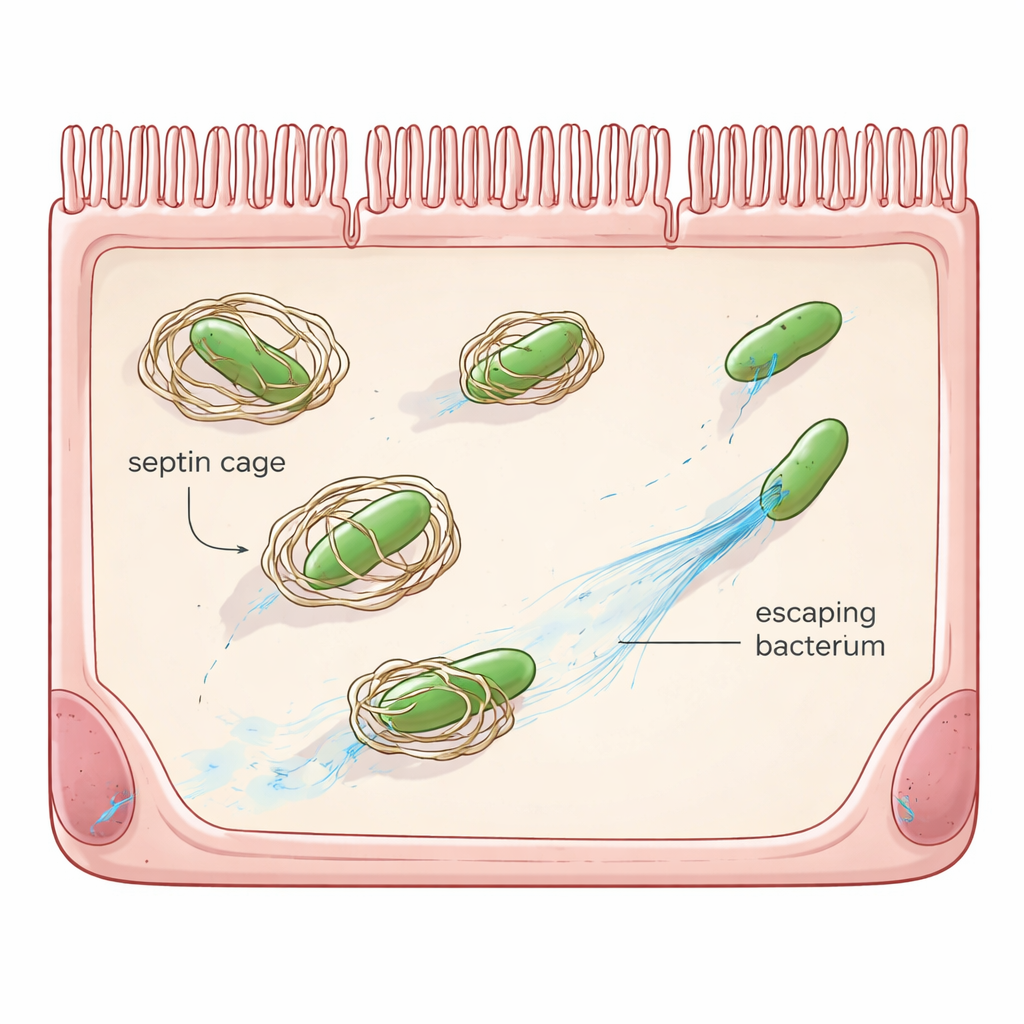
De "doe-het-zelf" verdediging van de cel
Naast witte bloedcellen en antilichamen hebben veel gewone cellen hun eigen noodbeveiligingssystemen, bekend als cel-autonome immuniteit. Eén zo’n systeem berust op septinen, een familie van scaffold-eiwitten die ringen en kooi-achtige structuren vormen. Wanneer Shigella een cel binnendringt en ontsnapt in het gelei-achtige cytoplasma, kunnen septinen zich rond de bacterie assembleren, waardoor haar beweeglijkheid wordt geblokkeerd en de bacterie wordt gemarkeerd voor vernietiging via cellulaire recyclemechanismen. Eerder werk toonde aan dat Shigella al over één tegengif beschikt, een eiwit genaamd OspG, dat septinen voor afbraak markeert. Toch vermijden de meeste bacteriën kooivorming zelfs als OspG ontbreekt, wat suggereert dat Shigella extra trucs heeft.
Een tweede bacteriële saboteur ontmaskerd
De auteurs richtten hun aandacht op een andere groep Shigella-eiwitten, bekend als de OspC-familie. Met een wereldwijde eiwitkaartenbenadering in humane cellen zochten ze naar gastheer-eiwitten die chemisch werden gemodificeerd in aanwezigheid van OspC-eiwitten. Naast bekende doelen die betrokken zijn bij eiwitsynthese vonden ze dat meerdere septinen, met name één genaamd SEPT9, consequent waren gemarkeerd. Gedetailleerde biochemische tests toonden aan dat drie OspC-eiwitten rechtstreeks een klein energie-rijk label, afgeleid van het molecuul NAD, op meerdere plaatsen van septinen kunnen aanhechten. Deze chemische wijziging, ADP-riboxanatie genoemd, is een bijzondere, onomkeerbare variant van een meer gebruikelijke eiwitmodificatie.
Het eiwitskelet van binnenuit breken
Om te begrijpen hoe dit chemische label de verdediging van de cel verzwakt, zochten de onderzoekers het in detail uit bij SEPT9. Septinen vormen normaal gesproken ordelijke ketens van acht eenheden, die zich vervolgens organiseren tot filamenten en uiteindelijk tot volledige kooien rond bacteriën. De onderzoekers ontdekten dat één specifieke positie in SEPT9, het aminozuur arginine 561, de belangrijkste plaats is voor ADP-riboxanatie tijdens infectie. Structureel werk en reconstitutie-experimenten met gezuiverde eiwitten lieten zien dat deze positie ligt op een kritisch contactoppervlak waar twee SEPT9-eenheden in elkaar grijpen. Wanneer dat arginine chemisch wordt gemodificeerd — of wordt vervangen door een residu dat de toegevoegde negatieve lading nabootst — vallen de octamere ketens uiteen in kleinere stukken en kunnen ze geen stabiele filamenten meer vormen.
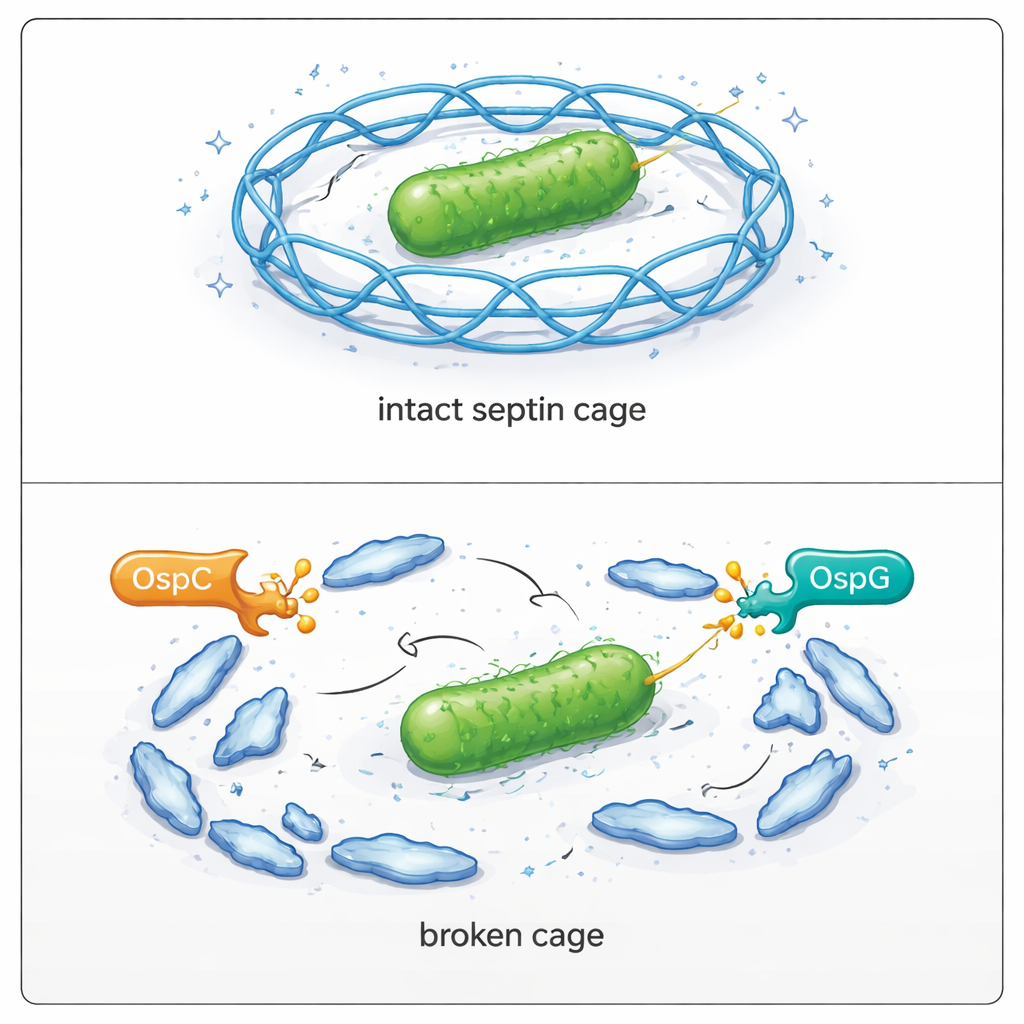
Toekijken hoe kooien falen in geïnfecteerde cellen
Het team keerde vervolgens terug naar levende cellen om de gevolgen te bekijken. In humane cellen geïnfecteerd met gewone Shigella belandde slechts een minderheid van de bacteriën in septinekooien. Wanneer alle OspC-eiwitten genetisch werden verwijderd, verdubbelde het aandeel gekooide bacteriën bijna. Het verwijderen van OspG had een vergelijkbaar effect, en het samen verwijderen van zowel OspC als OspG verhoogde de kooivorming nog verder en schaadde het vermogen van de bacteriën om zich over een cellaag te verspreiden sterk. Het opnieuw inbrengen van actieve OspC-eiwitten in de mutante stammen herstelde hun ontsnapping uit kooien en hun capaciteit om te repliceren en grote plaques te vormen. Microscopen bevestigden dat wanneer SEPT9 niet kan worden gemodificeerd op arginine 561, het efficiënt aan kooien deelneemt; wanneer het door OspC wordt gewijzigd, daalt de kooivorming rond bacteriën scherp.
Wat dit betekent voor de bestrijding van Shigella
Vrij toegankelijk verwoord, toont dit werk aan dat Shigella een bij elkaar passend paar moleculaire gereedschappen draagt, ontworpen om de tralies van een intracellulaire "gevangenis" open te breken. OspC verzwakt rechtstreeks de eiwitbouwstenen die nodig zijn voor de constructie van septinekooien, terwijl OspG hun afbraak via een ander chemisch pad bevordert. Samen laten deze strategieën de bacteriën vrij slippen, zich binnen cellen verplaatsen en buurcellen binnendringen. Het begrijpen van deze precieze ontsnappingmechanismen verdiept niet alleen ons beeld van hoe cel-intrinsieke immuniteit werkt, maar wijst ook op nieuwe therapeutische invalshoeken: middelen die OspC blokkeren of kritieke septinecontacten beschermen, zouden de natuurlijke capaciteit van de cel om deze gevaarlijke pathogeen te vangen en te verwijderen kunnen herstellen.
Bronvermelding: Tang, Z., Xian, W., Özbaykal Güler, G. et al. Shigella flexneri evades septin-mediated cell-autonomous immunity via protein ADP-riboxanation. Nat Commun 17, 1727 (2026). https://doi.org/10.1038/s41467-026-68425-0
Trefwoorden: Shigella, septinekooien, cel-autonome immuniteit, bacteriële virulentiefactoren, ADP-ribosylatie