Clear Sky Science · nl
Peptide-natuurproducten die op ClpC1 gericht zijn verstoren het proteoom van Mycobacterium tuberculosis verschillend
Waarom het verstoren van bacteriële opruimploegen ertoe doet
Tuberculose blijft een van de dodelijkste infectieziekten ter wereld, en geneesmiddelresistente stammen van Mycobacterium tuberculosis maken de behandeling moeilijker. De meeste bestaande antibiotica richten zich op de celwand van de bacterie of op haar vermogen om energie te produceren en genetisch materiaal te kopiëren. Deze studie onderzoekt een heel andere zwakke plek: het interne "opruimteam" van de cel dat de gezondheid van eiwitten bewaakt. Door te begrijpen hoe nieuwe op natuurlijke producten gebaseerde moleculen dit opruimsysteem verstoren, hopen wetenschappers toekomstige geneesmiddelen te ontwerpen die tuberkelbacteriën op nieuwe en duurzamere manieren kunnen doden.
Het eiwit-huishoudpunt van de cel
Net als alle levende cellen bouwt, vouwt, repareert en recyclet de tuberkelbacterie voortdurend zijn eiwitten. Een centrale speler in dit netwerk van eiwit-huishouding is een groot molecular machinecomplex genaamd ClpC1–ClpP1P2. Een deel (ClpC1) fungeert als chaperonne en herkent en trekt beschadigde of overbodige eiwitten aan, terwijl het andere deel (ClpP1P2) ze in stukjes hakt voor recycling. Dit systeem is essentieel voor het overleven van de bacterie, vooral onder stress zoals hitte of antibiotische aanval. Verschillende natuurlijke peptideverbindingen — ecumicine, ilamycines (rufomycines) en cyclomarins — binden al bekend aan ClpC1 en tonen sterke tuberkeldodende activiteit, wat suggereert dat dit complex een krachtig doelwit voor geneesmiddelen kan zijn. 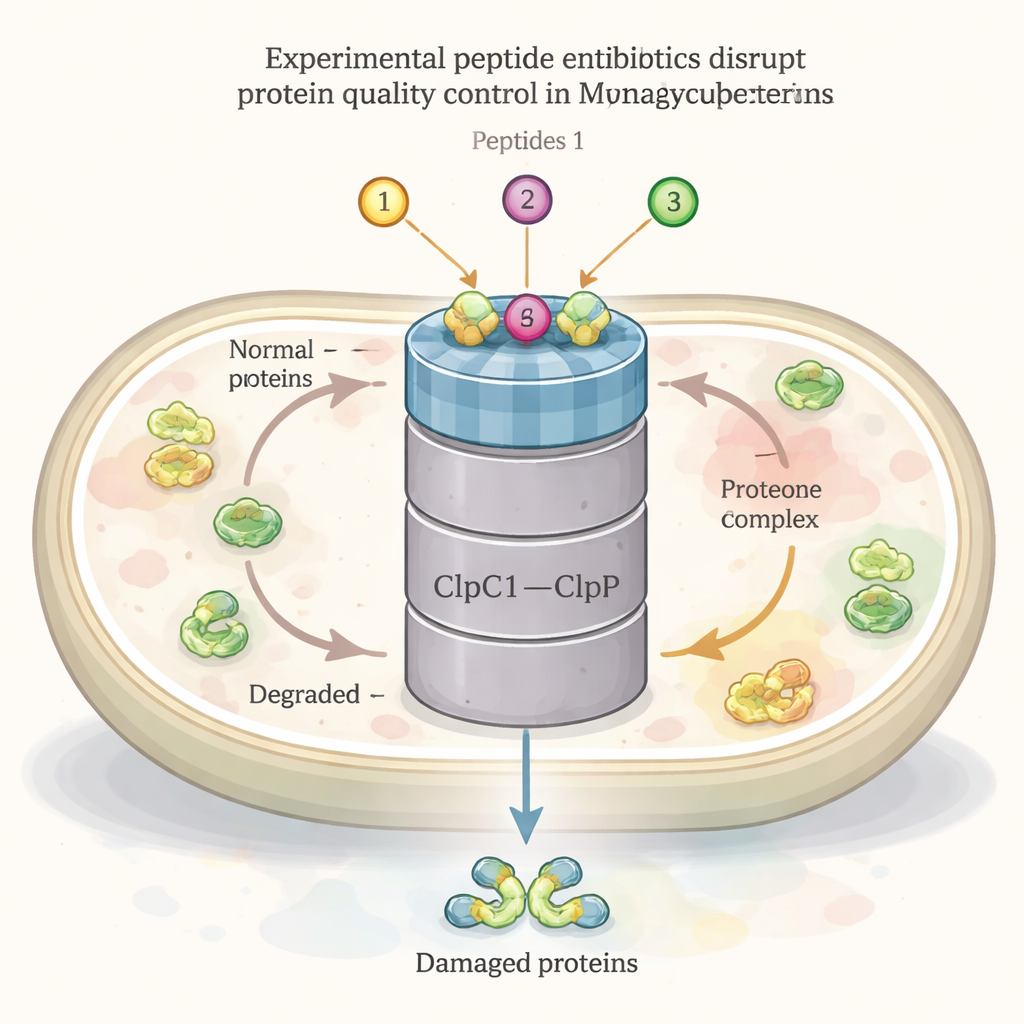
Drie verwante middelen, drie verschillende effecten
De onderzoekers bestudeerden één representant van elk van de drie peptidefamilies: een ecumicine-analoog (Ecu*), ilamycin E (IlaE) en een cyclomarin-derivaat (desoxycyclomarin, dCym). Hoewel alle drie zich binden aan hetzelfde gebied van ClpC1, gedragen ze zich niet hetzelfde in de cel. Met behulp van kwantitatieve proteomics — een benadering die duizenden eiwitten tegelijk meet — vonden ze dat Ecu* de breedste verstoring veroorzaakte en significant de niveaus van bijna 17% van alle bacteriële eiwitten veranderde. IlaE veranderde ongeveer 12% en dCym ongeveer 7%. Slechts 72 eiwitten werden consequent door alle drie de verbindingen beïnvloed, en de meeste daarvan namen in hoeveelheid af. Dit laat zien dat elk molecuul de ClpC1-machine in een andere richting duwt en zo het eiwitlandschap van de cel op verschillende manieren herschikt in plaats van de machine simpelweg "uit te schakelen".
De versnipperaar verstoppen versus de stroom uitschakelen
Om deze effecten in context te plaatsen, vergeleek het team de peptiden met bortezomib, een kankertherapiemiddel dat proteïne-afbrekende enzymen breed blokkeert. In tuberkelbacteriën veroorzaakte bortezomib een algemene ophoping van veel eiwitten, zoals verwacht wanneer de versnipperaars worden uitgeschakeld. Daarentegen produceerden de peptiden selectieve patronen: sommige bekende ClpC1-doelen stapelden zich op, andere werden uitgeput, en een globale remming van alle eiwitafbraak werd niet waargenomen. Gedetailleerde laboratoriumtesten met gezuiverde componenten toonden aan dat elk peptide veranderde hoe specifieke substraten werden behandeld. Zo interfereerden alle drie met de vernietiging van één regulerend eiwit (PanD), maar alleen Ecu* blokkeerde de afbraak van een modelongevouwen eiwit, en alleen dCym verstoorde de degradatie van het stress-beschermende eiwit Hsp20. Deze verschillen suggereren dat de algemene vorm en flexibiliteit van elk doelwit-eiwit mede bepalen hoe het wordt beïnvloed wanneer ClpC1 door een bepaalde verbinding "misgestemd" raakt. 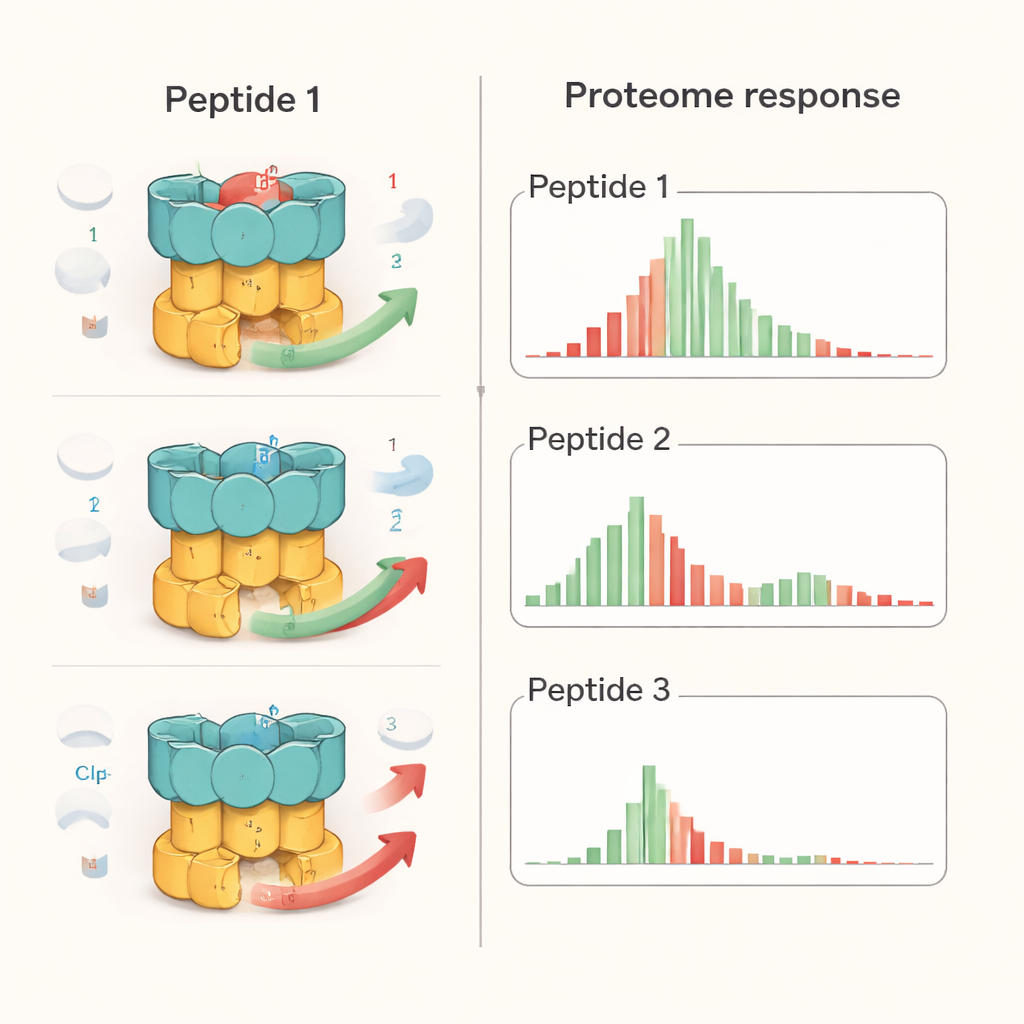
Stressreactoren en bacteriële zelfredding
De tuberkelbacterie heeft back-uproutes om om te gaan wanneer eiwitschade het hoofdopruimsysteem overweldigt. Een zulk systeem omvat een andere chaperonne, ClpC2, die cyclomarin-achtige moleculen kan binden en hun effect op ClpC1 kan verminderen. Deze studie vond dat hoewel alle drie de peptiden ClpC2 in het buisje kunnen binden, alleen het cyclomarin-derivaat (dCym) daadwerkelijk hogere ClpC2-niveaus in levende bacteriën veroorzaakte en krachtiger werd wanneer ClpC2 experimenteel werd verminderd. In contrast bleven Ecu* en IlaE effectief zelfs wanneer ClpC2 werd teruggedrongen, wat suggereert dat zij deze zelfreddingsroute grotendeels omzeilen. Het team ontdekte ook een sterke, verbinding-specifieke relatie met Hsp20, een klein eiwit dat helpt schadelijke ophopingen te voorkomen: Ecu* (en in mindere mate IlaE) veroorzaakten dramatische verhogingen in Hsp20-niveaus en Ecu* bond rechtstreeks aan Hsp20, wat een nieuwe koppeling onthult tussen deze kandidaat-geneesmiddelen en het stressresponssysteem van de cel.
Stress in een therapeutisch voordeel veranderen
Omdat het ClpC1-systeem vooral belangrijk is onder zware omstandigheden, testten de onderzoekers de geneesmiddelen terwijl de bacteriën mild aan hitte-stress werden blootgesteld, wat de hoeveelheid misgevouwen eiwitten verhoogt. Onder deze omstandigheden werden zowel Ecu* als dCym veel dodelijker en bereikten ze een toxiciteit vergelijkbaar met die van bortezomib, ondanks dat ze selectiever werken. Dit toont aan dat het gericht beïnvloeden van het eiwitkwaliteit-controlesysteem even effectief kan zijn als het uitschakelen van alle grote proteasen, maar met mogelijk fijnere controle. Het werk toonde ook aan dat veel van de door Ecu* veroorzaakte veranderingen in eiwitniveaus niet eenvoudigweg de veranderingen in genactiviteit weerspiegelen, wat onderstreept dat het verstoren van ClpC1 vooral de regulatie na eiwitsynthese verstoort.
Wat dit betekent voor toekomstige tuberculosebehandelingen
Voor niet-specialisten is de kernboodschap dat tuberkelbacteriën vertrouwen op een fijn afgewogen intern opruim- en stress-responssysteem om te overleven. De drie hier geteste uit natuurlijke producten afgeleide peptiden grijpen allemaal hetzelfde centrale complex, maar duwen het in verschillende modi, wat leidt tot uiteenlopende en zeer specifieke vervormingen van de eiwitsamenstelling van de bacterie. Belangrijk is dat ecumicine-achtige en ilamycin-achtige verbindingen een ingebouwd bacterieel reddingsmechanisme vermijden dat het effect van cyclomarin kan dempen, en toch de ziekteverwekker onder stress verlammen. Deze eigenschappen maken ze veelbelovend als bouwstenen voor toekomstige tuberculosegeneesmiddelen, inclusief ontworpen moleculen die tuberkelcellen ertoe kunnen brengen selectief hun eigen essentiële eiwitten te vernietigen of die kunnen worden verwerkt in "eiwit-targeting chimeren" om bacteriële zelfafbraak nauwkeurig te richten.
Bronvermelding: Barter, I.K., Bedding, M.J., Leodolter, J. et al. ClpC1-targeting peptide natural products differentially dysregulate the proteome of Mycobacterium tuberculosis. Nat Commun 17, 1725 (2026). https://doi.org/10.1038/s41467-026-68423-2
Trefwoorden: tuberculose, eiwitkwaliteitcontrole, ClpC1, antibioticaresistentie, natuurlijke productantibiotica