Clear Sky Science · nl
Gelijktijdige epigenomische profilering en meting van regulatorische activiteit met e2MPRA
De verborgen schakelaars van de cel lezen
Elke cel in je lichaam draagt in wezen hetzelfde DNA, maar een hersencel en een levercel gedragen zich heel verschillend. Het geheim zit in korte DNA-stukjes die als dimmers voor genen werken en die ze harder, zachter of uit zetten. Deze studie introduceert een krachtig nieuw instrument, e2MPRA, waarmee wetenschappers duizenden van deze schakelaars tegelijk kunnen testen terwijl ze ook bekijken hoe het DNA in de cel wordt verpakt en gemarkeerd — cruciale stappen om ontwikkeling, ziektegevoeligheid en waarom sommige genetische varianten belangrijk zijn terwijl anderen dat niet zijn te begrijpen.
Van DNA-kaarten naar DNA-functie
In het afgelopen decennium hebben onderzoekers enorme kaarten gemaakt van "kandidaat" regulatorische schakelaars, bekend als cis-regulatoire elementen. Ze gebruiken methoden die laten zien waar DNA losjes is verpakt (open chromatine), welke eiwitten gebonden zijn en welke histonmerken het omliggende DNA versieren. Die kaarten zijn indrukwekkend, maar ze zijn grotendeels beschrijvend: alleen omdat een eiwit bindt of een merk verschijnt, bewijst dat nog niet dat een sequentie daadwerkelijk genactiviteit aanstuurt. Traditionele massaal parallelle reporterassays (MPRAs) kunnen testen of duizenden DNA-fragmenten een reporter-gen versterken of dempen, maar ze vertellen ons niet welke eiwitten daar binden of welke epigenetische veranderingen die activiteit vergezellen.
Een tweevoudige assay voor activiteit en epigenetische merken
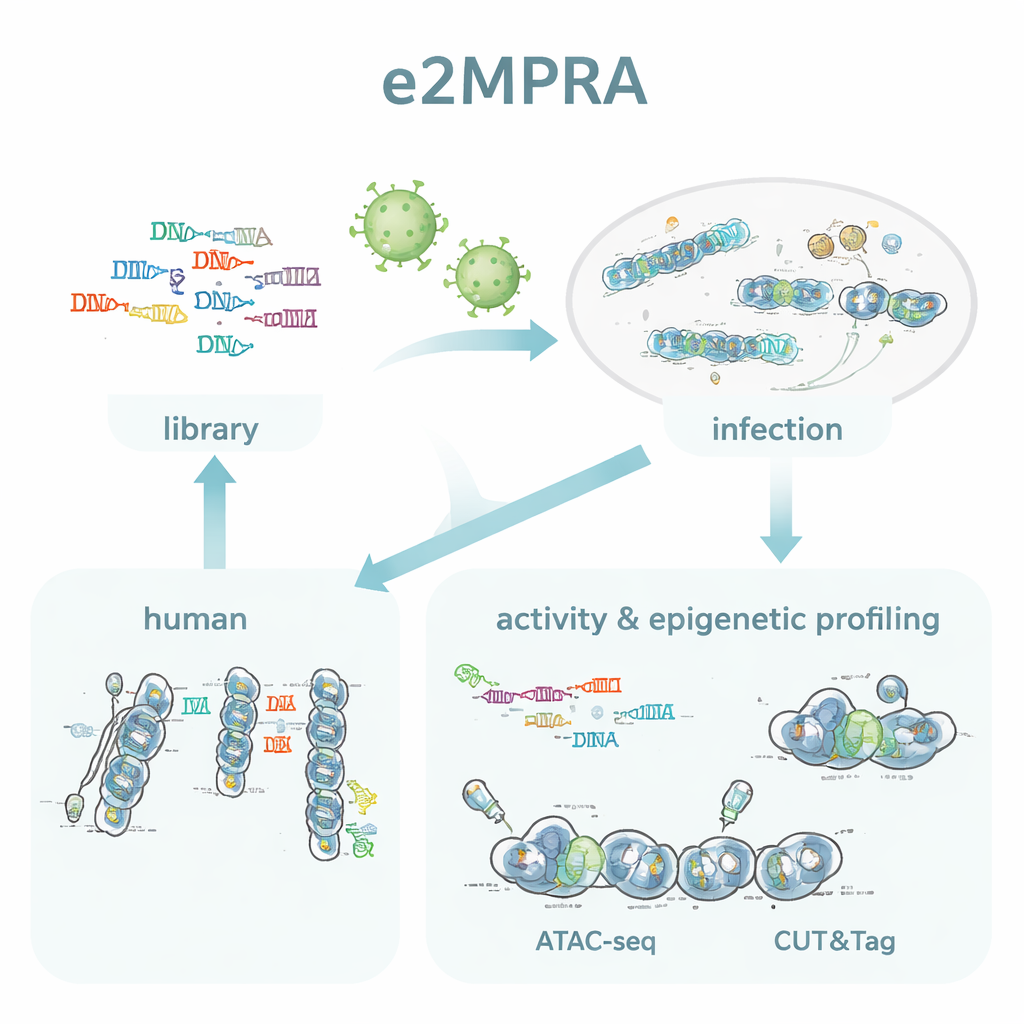
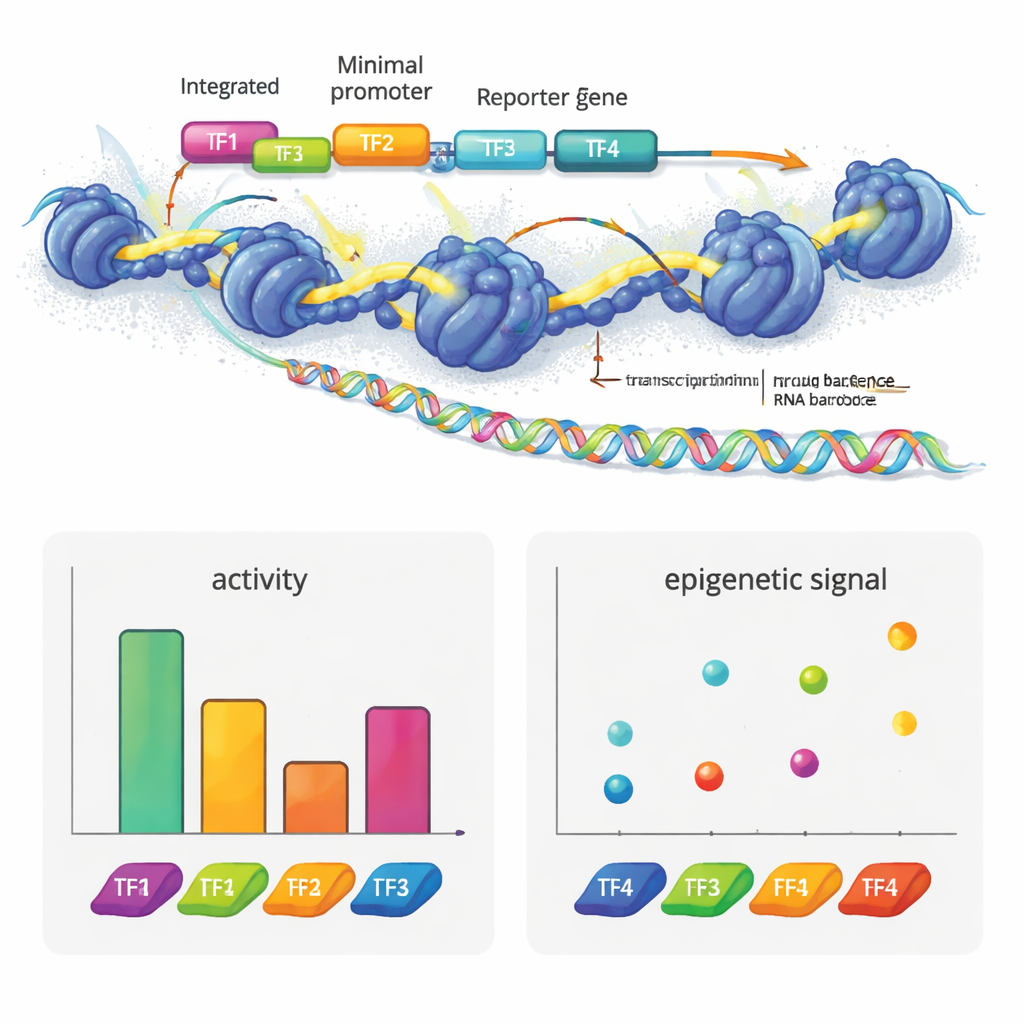
De auteurs creëerden e2MPRA door een lentivirale MPRA te combineren met twee epigenomische technieken, ATAC-seq en CUT&Tag. Eerst bouwen ze een DNA-bibliotheek waarin elke kandidaat-regulatorische sequentie gekoppeld is aan een korte barcode en naast een minimaal promotor- en reporter-gen wordt geplaatst. Deze bibliotheek wordt vervolgens verpakt in lentivirussen en vele keren geïntegreerd in de genomen van gekweekte menselijke cellen. Vanuit dezelfde celpool lezen ze barcodes in RNA om regulatorische activiteit te meten, en gebruiken ze ATAC-seq en CUT&Tag om chromatine-openheid en een belangrijk histonmerk (H3K27ac) specifiek bij de ingevoegde sequenties te meten. Door deze signalen te normaliseren op hoe vaak elke sequentie daadwerkelijk integreert, verkrijgen ze zij-aan-zij metingen van de "aan/uit-sterkte" en de epigenetische toestand voor duizenden elementen in één experiment.
Ontcijferen hoe transcriptiefactormotieven samenwerken
Om te zien wat deze technologie kan onthullen, bouwde het team synthetische enhancers uit bekende transcriptiefactormotieven die in levercellen worden gebruikt. Ze plaatsten deze motieven in verschillende aantallen en volgordes op neutrale DNA-templates. Sommige factoren, zoals HNF1A en XBP1, gedroegen zich als klassieke activatoren: meer kopieën verhoogden de reporter-output. Andere factoren, zoals HNF1A en ONECUT1, verhoogden vooral de chromatine-toegankelijkheid, wat past bij hun rol als "pioniers" die gesloten DNA openen. PPARA vertoonde een ander patroon: het veranderde sterk chromatine en histonmerken maar niet zelfstandig de transcriptie, en werkte wel samen met andere factoren om genactiviteit te verhogen. REST, een bekende repressor, dempte de activiteit wanneer deze naast activatoren werd geplaatst. Opvallend was dat het simpelweg herschikken van vier motieven de enhancer-sterkte substantieel kon veranderen, en dat activatoren doorgaans het beste werkten wanneer ze dichter bij de promotor stonden, wat een soort grammatica onthult in hoe deze motieven gerangschikt zijn.
Precies gevoelige basen in pluripotentie-enhancers aanwijzen
Vervolgens richtten de onderzoekers zich op enhancers die belangrijk zijn voor de identiteit van stamcellen, met de nadruk op regio's die worden gebonden door de pluripotentiefactoren POU5F1 (ook OCT4 genoemd) en SOX2. Ze creëerden dichte mutatiebibliotheken waarbij elke base van 100 basenparen lange enhancers systematisch werd gewijzigd, samen met kleine ramen van zes basen die willekeurig werden herschikt. Met e2MPRA in geïnduceerde pluripotente stamcellen konden ze zien welke mutaties reporter-activiteit verzwakten of versterkten en hoe ze chromatine-openheid en acetylatie beïnvloedden. Het verstoren van het POU5F1::SOX2-bindmotief verminderde vaak zowel genactiviteit als epigenetische merken, wat hun centrale rol bevestigt. In een goed bestudeerde enhancer nabij het POU5F1-gen vonden ze ook dat het veranderen van een YY1-motief de transcriptie verhoogde maar de chromatine-opening verminderde, wat suggereert dat sommige factoren een open toestand kunnen bevorderen terwijl ze de expressie toch beperken.
Wat dit betekent voor genen en ziekte
e2MPRA geeft niet perfect elke nuance van het natuurlijke 3D-bedrading van het genoom weer, maar het biedt een praktische manier om duizenden regulatorische sequenties en varianten onder gelijke omstandigheden te vergelijken. Door een functionele aflezing (hoe sterk een DNA-segment een gen aandrijft) te koppelen aan epigenetische aflezingen (hoe dat DNA is verpakt en gemarkeerd), helpt deze methode te onthullen waarom bepaalde transcriptiefactormotieven, combinaties en posities zo cruciaal zijn. Op langere termijn kunnen hulpmiddelen zoals e2MPRA het eenvoudiger maken om niet-coderende genetische varianten die aan ziekte gekoppeld zijn te interpreteren, synthetische enhancers voor gentherapie te ontwerpen en een vollediger "regulatiecode" op te bouwen die DNA-sequentie verbindt met celdynamiek.
Bronvermelding: Zhang, Z., Georgakopoulos-Soares, I., Bourque, G. et al. Simultaneous epigenomic profiling and regulatory activity measurement using e2MPRA. Nat Commun 17, 1724 (2026). https://doi.org/10.1038/s41467-026-68422-3
Trefwoorden: genregulatie, enhancers, epigenetica, transcriptiefactoren, functionele genomica