Clear Sky Science · nl
Guardian ubiquitine E3-ligases richten zich op kankergerelateerde APOBEC3-deaminases voor afbraak om de integriteit van het menselijk genoom te bevorderen
Ons DNA beschermen tegen ‘vijandig vuur’ van binnenuit
Onze cellen zetten krachtige enzymen in om viraal DNA te beschadigen en ons zo tegen infecties te beschermen. Maar sommige van diezelfde enzymen kunnen, als ze niet goed worden gecontroleerd, per ongeluk ons eigen genoom beschadigen en bijdragen aan kanker. Deze studie onthult hoe menselijke cellen deze risicovolle enzymen in toom houden en beschrijft een ingebouwd “kwaliteitscontrolesysteem” dat gevaarlijke varianten markeert voor vernietiging voordat ze ons DNA kunnen herschrijven.
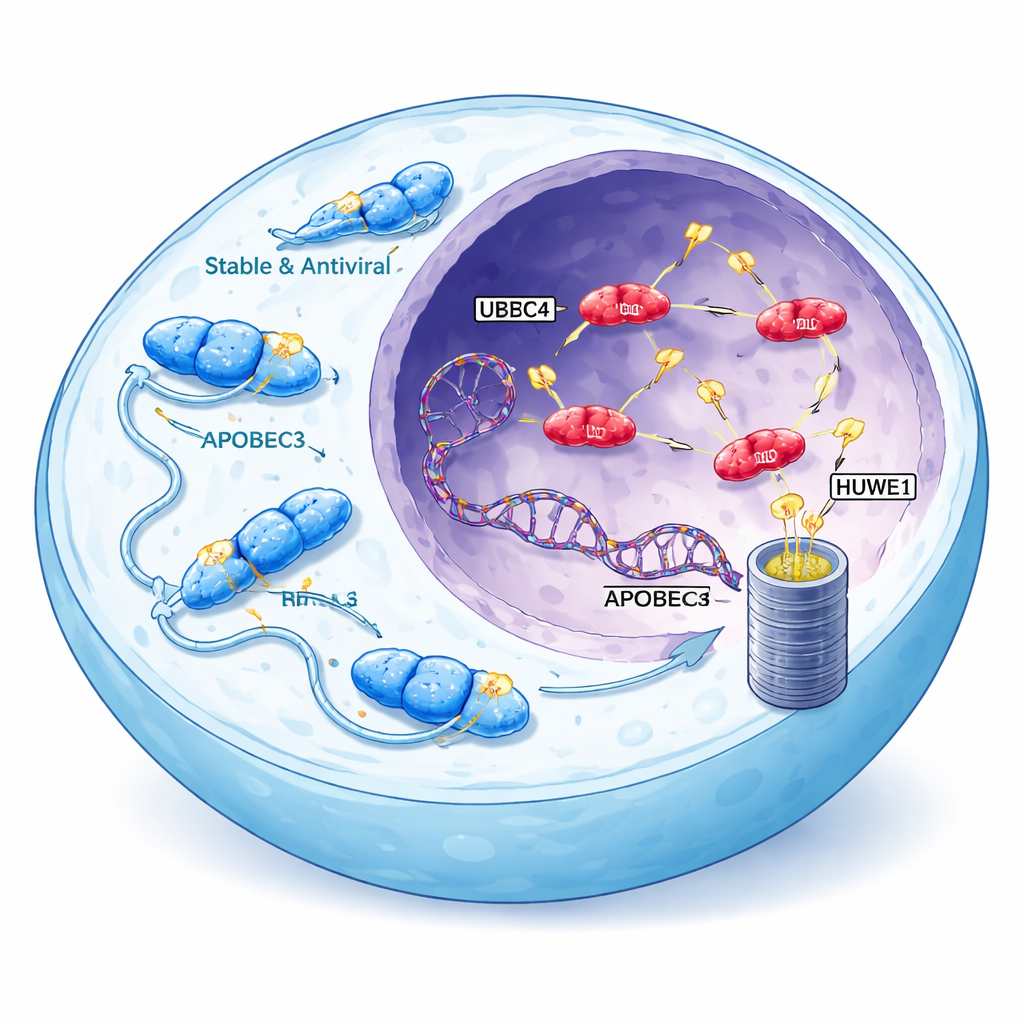
Virusbestrijders die zich tegen ons kunnen keren
De APOBEC3-familie van enzymen helpt normaal gesproken bij de verdediging tegen virussen zoals HIV door viraal DNA chemisch te wijzigen en zo dodelijke fouten te veroorzaken. Mensen hebben zeven APOBEC3-varianten, en drie daarvan—A3A, A3B en een vorm van A3H genaamd haplotype I (A3H-I)—worden sterk geassocieerd met mutatiepatronen die in veel vormen van kanker worden gezien. Deze specifieke enzymen kunnen het celkern binnendringen, waar onze chromosomen zich bevinden, en kenmerkende clusters van mutaties in het genoom introduceren. Dergelijke APOBEC-gekoppelde signaturen komen voor in meer dan de helft van alle menselijke kankers, vooral bij borst-, long- en blaastumoren, waar ze de voorraad genetische veranderingen vergroten waarop tumoren kunnen terugvallen om zich aan te passen en behandeling te weerstaan.
Waarom de gevaarlijkste vormen merkwaardig onstabiel zijn
Opmerkelijk genoeg zijn de APOBEC3-enzymen die het sterkst met kanker worden geassocieerd ook het minst stabiel. In tegenstelling tot hun cytoplasmatische verwanten, die zich ophopen tot hoge niveaus en virussen efficiënt blokkeren, worden A3A, A3B en A3H-I snel afgebroken en zijn ze meestal in lage concentraties in de kern aanwezig. De onderzoekers stelden dat deze instabiliteit mogelijk doelbewust is: als cellen actief de niveaus van kern-APOBEC3-eiwitten beperken, kan elke verstoring van die controle uitbarstingen van mutagenese ontketenen. Met A3H-I als model lieten ze zien dat kankergerelateerde APOBEC3’s voornamelijk door het proteasoom, de eiwitversnipperaar van de cel, worden vernietigd nadat ze op meerdere aminozuurplaatsen met kleine moleculaire ‘vlaggen’ genaamd ubiquitine zijn gemarkeerd.
De cellulaire bewakers vinden
Om de machinerie die A3H-I en A3B markeert te identificeren, combineerde het team CRISPR-screening met eiwit-nabijheidsmapping. Ze maakten cellen die verschillend oplichten afhankelijk van hoe stabiel A3H-I en de onschadelijke variant A3H-II zijn, en schakelden systematisch genen uit die betrokken zijn bij eiwitafbraak. Drie ubiquitine-ligases—UBR4, UBR5 en HUWE1—staken er bovenuit. Het uitschakelen van een van deze ligases verhoogde selectief de niveaus van de onstabiele, nucleaire A3H-I zonder de stabiele, cytoplasmatische A3H-II te beïnvloeden. Dezelfde ligases verhoogden onafhankelijk de niveaus van endogene A3B in colon- en immuuncellijnen, en het verwijderen van alle drie tegelijk veroorzaakte een optellende toename van A3B-abundantie. Biochemische experimenten toonden verder aan dat UBR5 en HUWE1 fysiek aan A3B en A3H-I binden en rechtstreeks ubiquitineketens aanhechten, terwijl UBR4 lijkt te specialiseren in het verlengen van deze ketens om de eiwitten efficiënter afbreekbaar te maken.
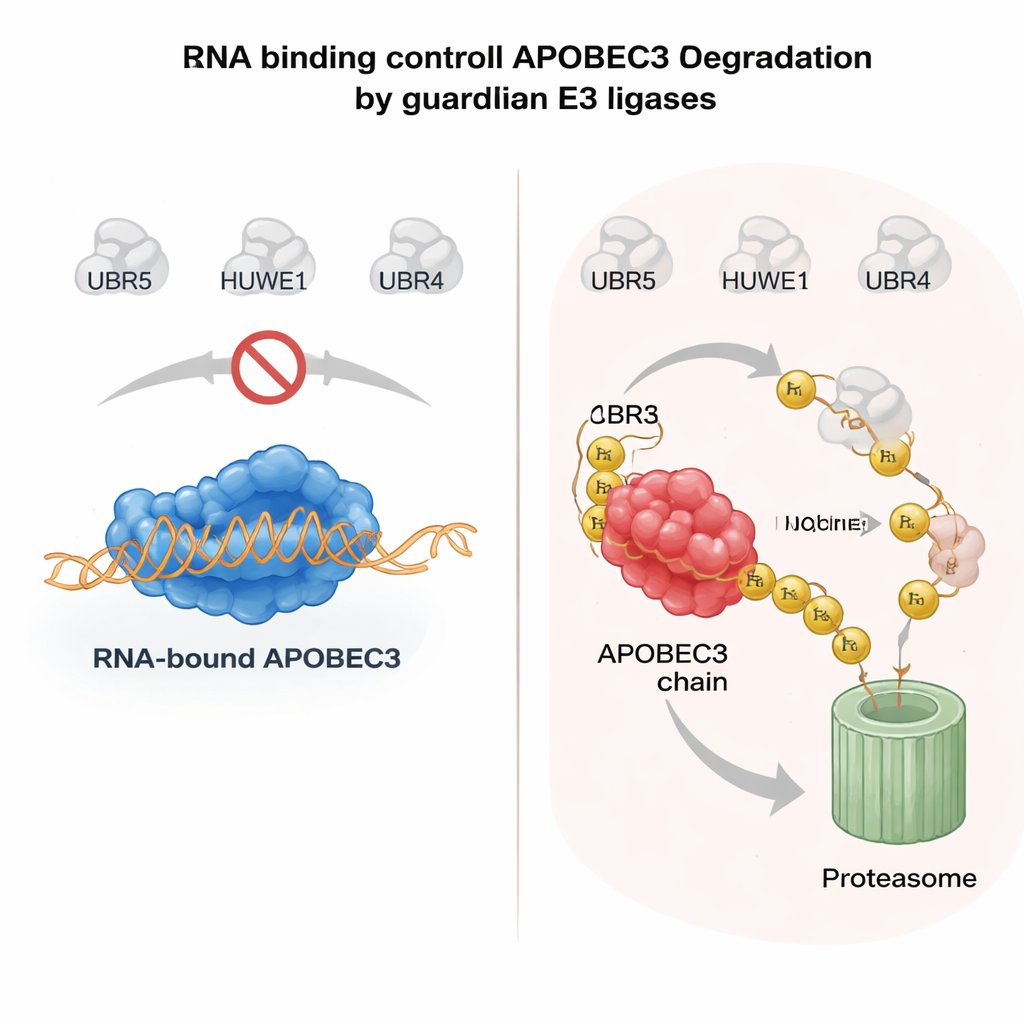
RNA als veiligheidsgordel voor risicovolle enzymen
Wat bepaalt of een APOBEC3-enzym gespaard blijft of wordt vernietigd? Een belangrijke aanwijzing kwam uit de manier waarop APOBEC3-eiwitten aan RNA-moleculen in het cytoplasma binden. Wanneer A3H of een ander familielid, A3G, RNA bindt, blijft het vaak in grote complexen in het cytosol en is het relatief stabiel. Mutaties die de RNA-binding verzwakken, zorgen ervoor dat deze enzymen naar de kern verschuiven, hun beschermende partners verliezen en zeer onstabiel worden. De auteurs toonden aan dat wanneer APOBEC3-eiwitten niet aan RNA gebonden zijn, UBR5 en HUWE1 blootliggende oppervlakken van het enzym herkennen, ze met ubiquitine versieren en gericht afbreken in de kern. In gezuiverde systemen versterkte het toevoegen van RNase om RNA te verwijderen sterk het vermogen van deze ligases om aan APOBEC3 te binden en het te ubiquitineren, wat bevestigt dat RNA-binding fungeert als een moleculair schild. Dit mechanisme stelt cellen in staat antivirale APOBEC3’s actief te houden in het cytoplasma terwijl elke niet-gebonden, genoombedreigende pool in de kern snel wordt opgeruimd.
Wanneer de bewakers falen: verbanden met kankermutaties
Als UBR4, UBR5 en HUWE1 als bewakers fungeren, zou hun verlies de mutatieniveaus moeten verhogen. De onderzoekers toetsten dit door elke ligase uit te schakelen in colonkankercellen en DNA-veranderingen in de loop van de tijd te volgen met een gevoelige sequencingmethode die mutatie-’signaturen’ leest. Het verwijderen van deze ligases, vooral in cellen die A3H-I tot expressie brachten, versterkte APOBEC-specifieke mutatiepatronen—precies het soort dat in menselijke tumoren wordt aangetroffen. Bij uitbreiding naar patiëntengegevens analyseerden ze duizenden kankergenomen en vonden dat tumoren met mutaties in UBR5 of HUWE1 een significant hoger aandeel APOBEC-gekoppelde mutatiesignaturen hadden dan tumoren met intacte ligases, zelfs na correctie voor de totale mutatielast. Dit suggereert dat defecte bewaker-ligases bij patiënten kankergerelateerde APOBEC3-enzymen kunnen laten ontsporen en het tumorgenoom kunnen herschikken.
Betekenis voor toekomstige kankerzorg
Voor niet-specialisten is de conclusie dat onze cellen een verfijnd controlesysteem bezitten om te voorkomen dat nuttige antivirale enzymen per ongeluk ons eigen DNA saboteren. UBR4, UBR5 en HUWE1 fungeren als bewakers die signaleren wanneer APOBEC3-enzymen niet langer veilig aan RNA vastzitten en, vooral in de kern, ze naar de cellulair versnipperaar sturen. Wanneer dit controlesysteem verzwakt is—door mutaties in de ligases of door geneesmiddelen die eiwitafbraak blokkeren—kan APOBEC3-activiteit de genetische chaos aanwakkeren die kankerevolutie en behandelingsresistentie drijft. Inzicht in dit bewakernetwerk opent wegen naar nieuwe diagnostische markers, zoals ligasemutaties of APOBEC-eiwitniveaus, en suggereert dat het zorgvuldig bijsturen van deze route mogelijk ooit kan helpen schadelijke uitbarstingen van mutaties in tumoren te beperken zonder onze antivirale verdediging te ondermijnen.
Bronvermelding: Schwartz, I., Budroni, V., Meyenberg, M. et al. Guardian ubiquitin E3 ligases target cancer-associated APOBEC3 deaminases for degradation to promote human genome integrity. Nat Commun 17, 1723 (2026). https://doi.org/10.1038/s41467-026-68420-5
Trefwoorden: APOBEC3, genoomstabiliteit, ubiquitine-ligase, kanker-mutagenese, eiwitafbraak