Clear Sky Science · nl
Ruimtelijke profilering van contractiliteit door een zelfgeorganiseerde mechanogeen-activiteitsgradiënt ligt ten grondslag aan Drosophila-gastrulatie
Hoe weefsels zichzelf vormen
Vroege embryo's veranderen op de een of andere manier eenvoudige cellagen in ingewikkelde driedimensionale vormen. Deze studie behandelt een fundamentele vraag achter die toverkunst: hoe coördineren cellen waar ze moeten samentrekken en buigen zodat een weefsel op de juiste plek en in de juiste richting vouwt? Door vliegenembryo's op hoge resolutie te volgen, ontdekken de auteurs een chemisch signaal dat zich gedraagt als een “mechanische morfogen” en rechtstreeks bepaalt waar cellen aan zichzelf trekken om een cruciale vouwing in de ontwikkeling aan te sturen.
Een golf die het embryo vouwt
Bij de fruitvlieg Drosophila is gastrulatie een belangrijke stap in de vroege ontwikkeling, waarbij een vlakke cellaag naar binnen buigt om de aanleg van de darm te beginnen. Aan de achterzijde van het embryo start een groep cellen, het posterior endoderm primordium, dit proces door samentrekking aan hun bovenste (apicale) zijde. Deze initiële buiging zet een voortbewegende golf van weefselinvaginatie in gang die zich over aangrenzende cellen voortplant. De auteurs tonen aan dat deze golf afhangt van een signaal genaamd Fog, een uitgescheiden molecule die een familie receptoren activeert die bekendstaan als GPCR's, en die op hun beurt het contractiele apparaat van de cel inschakelen dat is opgebouwd uit het motorproteïne Myosin-II.
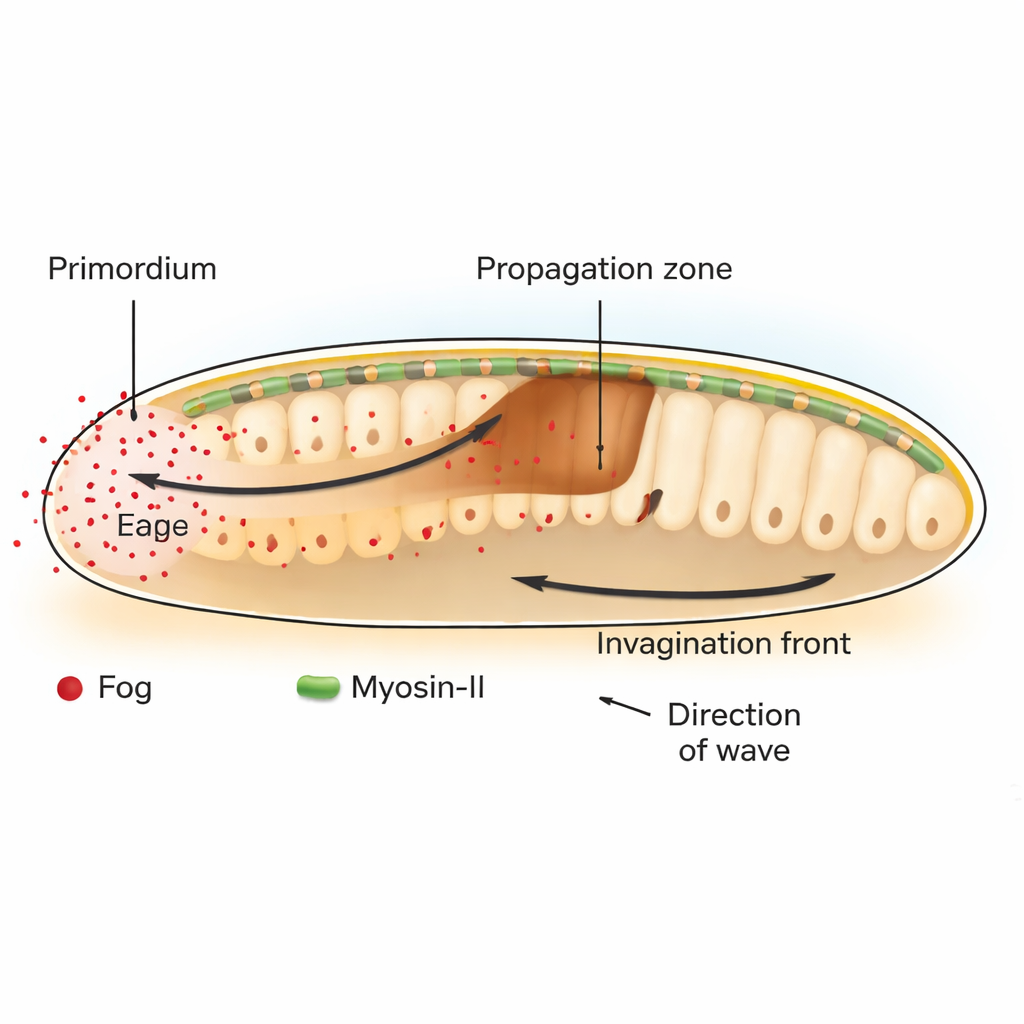
Een chemische stof die kracht patroon in plaats van lot bepaalt
Klassiek hebben ontwikkelingsbiologen zich gericht op “morfogenen”, diffusieve moleculen waarvan concentratiegradiënten cellen vertellen welke identiteit ze moeten aannemen. Hier gedraagt Fog zich anders. In plaats van te veranderen welk celtype een gebied zal worden, past Fog rechtstreeks aan hoe sterk cellen samentrekken. Door Fog en zijn downstream boodschapper Gα selectief te herstellen of te blokkeren in bepaalde regio's, laten de onderzoekers zien dat Fog geproduceerd in het primordium zowel noodzakelijk als voldoende is om Myosin-II-activatie en weefselvouwing op afstand in de aangrenzende propagatiezone te veroorzaken. Wanneer Fog wordt verankerd zodat het zich niet kan verspreiden, trekken alleen de producerende cellen samen en stokt de invaginatiegolf na slechts één of twee cellenrijen.
Een verborgen gradiënt op het celoppervlak
Een voor de hand liggend idee is dat Fog een klassieke concentratiegradiënt buiten de cellen zou vormen. Met een fluorescente versie van Fog en gevoelige fluorescentiemetingen komt het team echter tot de tegenovergestelde bevinding: in de dunne vloeistoflaag tussen het weefsel en de omhullende membraan (de vitelliene membraan) is Fog opmerkelijk uniform verdeeld. Toch vormt Myosin-II-activiteit duidelijk een steile, voortbewegende gradiënt, het sterkst direct voor de oprukkende vouw en afnemend over een paar celafstanden. Het ontbrekende stuk is dat Fog niet fungeert als eenvoudige bulkconcentratie-indicator; in plaats daarvan raakt een klein deel van Fog tijdelijk vast aan het celoppervlak, bindt het aan zijn GPCR-receptoren en vormt zo een oppervlakgebonden activiteitsgradiënt, terwijl de vrije Fog-moleculen in de vloeistof gelijkmatig blijven verdeeld.
Receptoren, endocytose en adhesie vormen de golf
De auteurs tonen aan dat dit oppervlakgebonden Fog, samen met zijn receptoren, zichzelf organiseert tot een patroon. Waar Fog herhaaldelijk op receptoren botst, bevordert het receptorclustering en -activatie, wat meer Myosin-II aantrekt. Een cellulair “opruimproces” — GPCR-endocytose — verwijdert vervolgens actieve complexen, voorkomt ongecontroleerde activatie en helpt af te stellen hoe ver het signaal zich verspreidt. Wanneer deze endocytose genetisch vertraagd is, wordt de Myosin-II-gradiënt hoger en wijder. Een tweede belangrijke speler is een klasse adhesiemoleculen die integrines worden genoemd. Terwijl het weefsel buigt, drukken cellen vóór de vouw tegen de vitelliene membraan; dit contact activeert lokaal integrines, die op hun beurt de effectiviteit van Fog–GPCR-signaleringsroutes versterken. Het gebied met sterke integrinebetrokkenheid komt overeen met de reikwijdte van de Myosin-II-gradiënt, en zonder integrines wordt de golf zwak en korter van bereik, ook als Fog-signalisatie anderszins versterkt is.
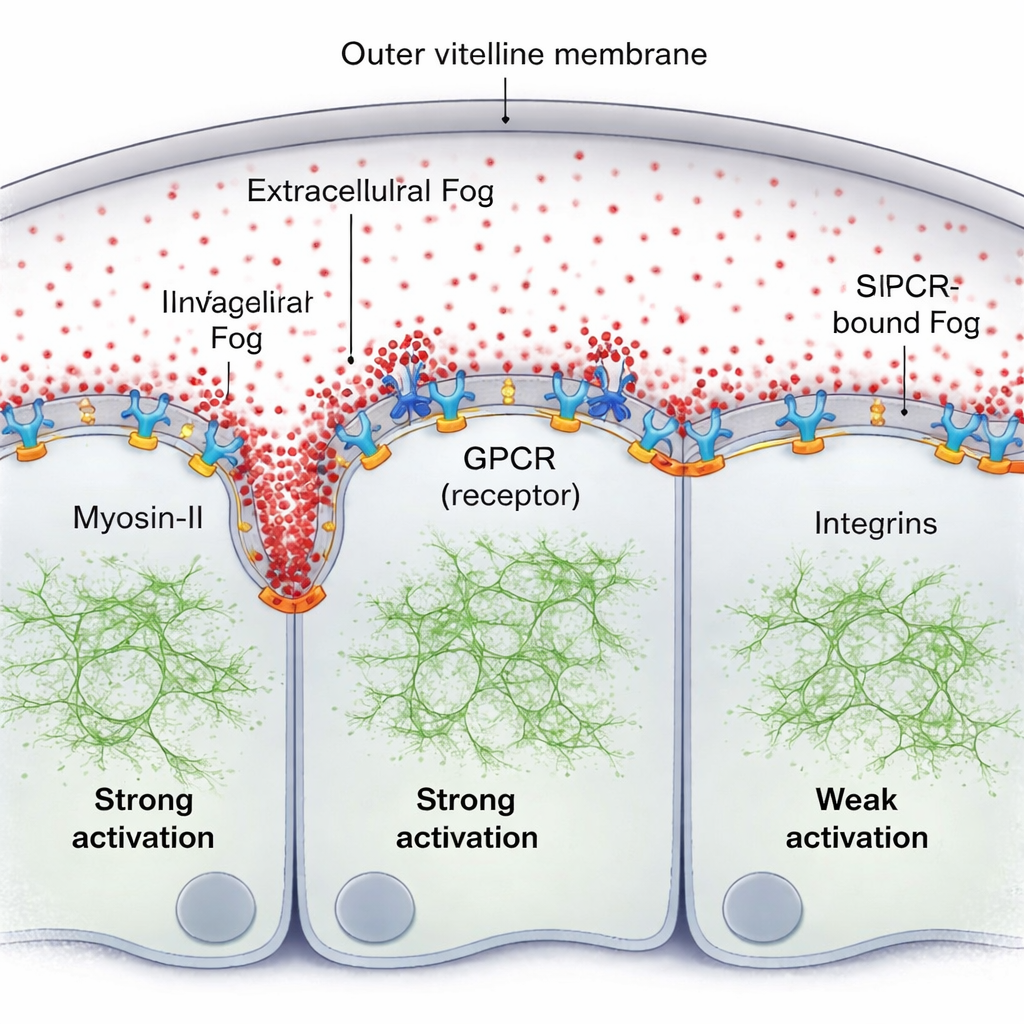
Een zelfvernieuwend mechanisch patroon
Voor niet-specialisten is de kernboodschap dat het embryo zich niet uitsluitend baseert op vooraf getekende chemische kaarten om te beslissen waar het moet vouwen. In plaats daarvan bouwt het een bewegend patroon van mechanische activiteit terwijl het zich ontwikkelt. Fog verspreidt zich uniform, maar zijn effectieve werking wordt op het celoppervlak gebeeldhouwd door receptorclustering, receptorverwijdering en veranderende weefselgeometrie naarmate cellen tegen hun omgeving drukken. Dit creëert een zelfgeorganiseerde, voortbewegende gradiënt van contractiele kracht die het weefsel gecoördineerd naar binnen trekt in een golf. Het werk biedt een concreet voorbeeld van een lang-theoretiseerde “mechanogeen”: een diffunderend molecuul dat rechtstreeks de fysieke krachten in een weefsel patroongeeft en helpt verklaren hoe levende vormen zich tijdens de ontwikkeling zo betrouwbaar vormen.
Bronvermelding: Mundhe, G., Dunsing-Eichenauer, V., Philippe, JM. et al. Spatial patterning of contractility by a self-organized mechanogen activity gradient underlies Drosophila gastrulation. Nat Commun 17, 1721 (2026). https://doi.org/10.1038/s41467-026-68418-z
Trefwoorden: gastrulatie, mechanogeen, Drosophila-embryo, weefselmechanica, Fog-signaleringspad