Clear Sky Science · nl
Configuraties van DNA-einden bepalen de vorming van synaptische complexen tijdens NHEJ-gemedieerde eindoverbrugging
Als DNA breekt, moeten cellen snel handelen
Dagelijks wordt het DNA in onze cellen geknipt, beschadigd en aangetast door normale stofwisseling en omgevingsstress. Een van de gevaarlijkste verwondingen zijn dubbele strengbreuken, waarbij beide strengen van de DNA-helix breken. Als deze breuken niet snel en nauwkeurig worden hersteld, kunnen cellen sterven of, erger nog, ontsporen richting kanker. Deze studie onderzoekt hoe de exacte vorm en chemie van gebroken DNA-einden bepalen of een belangrijke herstelroute, non-homologe end-joining (NHEJ), die uiteinden efficiënt en met zo min mogelijk fouten bij elkaar brengt.
Twee manieren om gebroken DNA samen te brengen
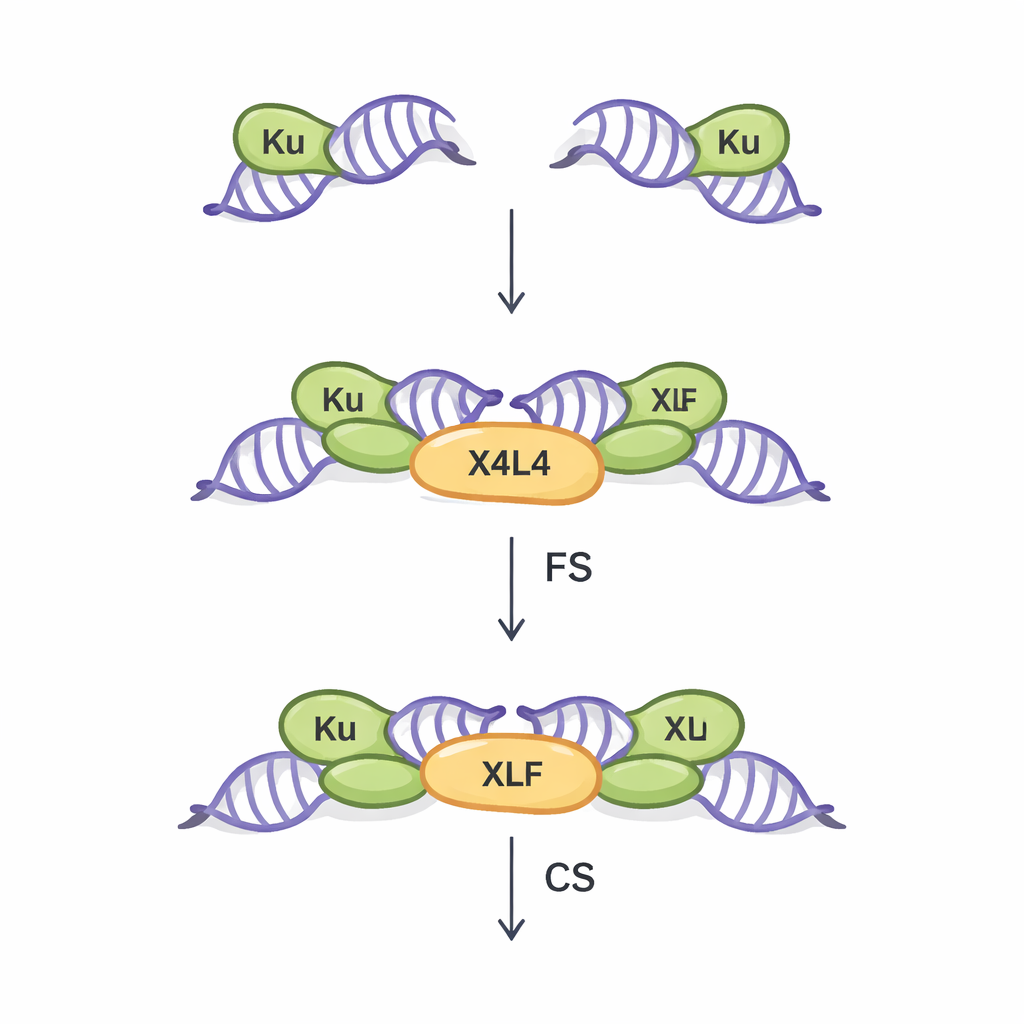
NHEJ is de belangrijkste reparatieroute voor dubbele strengbreuken in de meeste lichaamscellen. Het werkt zonder een overeenkomstig DNA-sjabloon, wat het snel maakt maar enigszins foutgevoelig. De eerste cruciale stap in deze route wordt synapsis genoemd: het fysiek overbruggen van de twee gebroken DNA-einden zodat ze later kunnen worden samengevoegd. Eerder werk, grotendeels met ideale blinde (blunt) DNA-einden, toonde twee soorten synaptische assemblages. In de "flexibele synaptische" (FS) toestand worden de einden dicht bij elkaar gehouden en kunnen ze bewegen en zoeken naar manieren om te paarsen. In de "dichte synaptische" (CS) toestand liggen de einden uitgelijnd end-to-end en zijn ze klaar om verzegeld te worden door een ligase-enzym. Drie kernproteïnen — Ku, XRCC4–Ligase IV (samen X4L4 genoemd) en XLF — blijken dit proces te coördineren, maar hoe reële, onregelmatige DNA-einden beïnvloeden welke synaptische toestand ontstaat, was tot nog toe slecht begrepen.
Vorm van het eind en korte overeenkomsten sturen de herstelroute
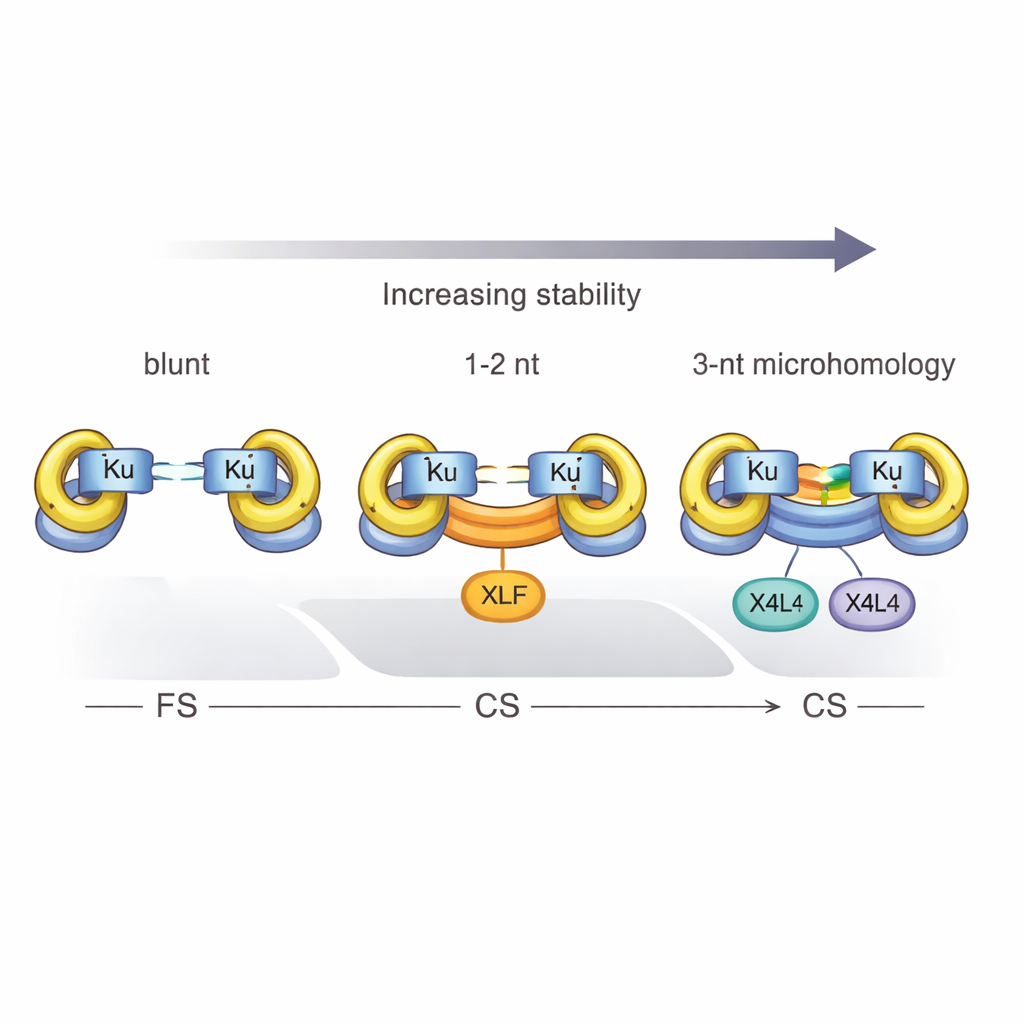
De onderzoekers gebruikten single-molecule FRET, een fluorescentietechniek die afstanden op nanometerschaal volgt, om individuele DNA-moleculen te observeren terwijl ze door NHEJ-eiwitten bij elkaar werden gebracht. Ze vergeleken eenvoudige blinde einden met realistischere einden die korte overhangs dragen — kleine enkelstrengige staarten die mogelijk met elkaar kunnen paaren. Ze ontdekten dat wanneer overhangs complementair zijn, zelfs met slechts een paar basen, dat de kans op het vormen van een dicht synaptisch complex dramatisch vergroot. Drie overeenkomende basen van "microhomologie" bij de breuk waren zelfs voldoende voor Ku en X4L4 om alleen een stabiel CS-complex te vormen, zonder XLF. Dit laat zien dat het DNA zelf een deel van de energie en richtvoering kan leveren die normaal door helper-eiwitten wordt aangedragen.
Hoe kleine DNA-flappen de brug stabiliseren
Door onderscheidbare FRET-handtekeningen te analyseren, onthulde het team ten minste twee structurele varianten van de dichte synaptische toestand voor overhangende einden. In de ene paaren de uiteinden van de overhangs direct met elkaar, waardoor een genikte of gegriefde verbinding ontstaat. In de andere drukken de juncties waar dubbelstrengs DNA de enkelstrengige overhangs ontmoeten in elkaars verlengde, terwijl de overhangs naar buiten klappen als kleine flapjes. Deze flapjes laten nog steeds basenparing toe en houden de einden zeer dicht bij elkaar, wat waarschijnlijk het complex stabiliseert en enzymen ruimte geeft om het DNA bij te knippen of te verlengen voordat het definitief wordt verzegeld. Intrigerend genoeg beïnvloedde veelvoorkomende oxidatieve schade in de overhangs, zoals 8-oxoguanine, dit proces slechts bescheiden, wat de robuustheid van NHEJ tegen bepaalde vormen van schade benadrukt.
Proteïnen, fosfaten en de kracht van drie
De studie definieerde ook een harde drempel: ten minste drie complementaire baseparen zijn vereist zodat Ku en X4L4 betrouwbaar een flexibel complex in een dicht complex kunnen omzetten. Met slechts één of twee overeenkomsten blijft het systeem meestal in de flexibele toestand steken, tenzij XLF meedoet om de einden samen te klemmen. Chemische details zijn ook belangrijk. Wanneer het gebroken DNA een 5′-fosfaatgroep draagt — een normale eigenschap van veel fysiologische breuken — wordt synapsis efficiënter en is het waarschijnlijker dat dichte complexen daadwerkelijk worden geligeerd, waardoor een tijdelijke brug verandert in een permanente reparatie. Deze fosfaatboost kan echter niet volledig het stabiliserende effect van basenparing bij de breuk vervangen.
Waarom dit belangrijk is voor gezondheid en genbewerking
Eenvoudig gezegd laat dit werk zien dat gebroken DNA-einden geen passieve slachtoffers zijn die wachten om gerepareerd te worden. Hun exacte vormen, kleine stukjes overeenkomende sequentie en chemische labels sturen actief hoe herstelproteïnen ze grijpen, uitlijnen en weer verbinden. Wanneer drie of meer overeenkomstige basen aanwezig zijn, helpen de DNA-einden zelf de breuk in een reparatieklare configuratie te vergrendelen, waardoor sommige hulp-eiwitten soms optioneel worden. Wanneer zulke overeenkomsten schaars zijn, worden extra proteïnefactoren essentieel. Deze inzichten helpen verklaren waarom sommige breuken netjes worden gerepareerd terwijl andere leiden tot kleine mutaties of herordelingen. Ze bieden ook aanwijzingen om genbewerkingstools zoals CRISPR te verbeteren, waarbij opzettelijk aangebrachte DNA-breuken door hetzelfde NHEJ-machinerie worden hersteld. Door de einden van die breuken bij te stellen, kunnen wetenschappers mogelijk beter sturen hoe het genoom wordt hervormd.
Bronvermelding: Zhang, C., Jin, W., Jiang, Y. et al. DNA end configurations dictate synaptic complex formation during NHEJ-mediated end bridging. Nat Commun 17, 1720 (2026). https://doi.org/10.1038/s41467-026-68417-0
Trefwoorden: herstel van dubbele strengbreuken in DNA, non-homologe end-joining, DNA-synapsis, microhomologie, genoomstabiliteit