Clear Sky Science · nl
Een enkele switch van valine naar leucine verstoort de DNA-binding van Plasmodium falciparum AP2-G en onthult GDV1’s rol bij ap2-g-activatie
Hoe malariaparasieten een cruciale leven-of-dood-keuze maken
Malariaparasieten die in ons bloed leven staan voortdurend voor een ingrijpende beslissing: doorgaan met zich binnen één persoon te vermenigvuldigen, of overschakelen naar een vorm die via een mug naar de volgende gastheer kan springen. Deze studie onthult hoe een enkele kleine wijziging in een parasietproteïne die besmettelijke, mugklare fase volledig kan uitschakelen, en biedt daarmee nieuwe aanknopingspunten om malariatransmissie te blokkeren.
Het keuzevorkje van de parasiet
In de bloedbaan richten Plasmodium falciparum-parasieten zich meestal op snelle groei, wat ziekte veroorzaakt. Maar een klein deel transformeert tot seksuele vormen, gametocyten genoemd, de enige stadia die muggen kunnen opnemen en doorgeven. Hoe slechts sommige parasieten in een populatie deze omschakeling maken, is lange tijd een raadsel geweest. Eerder werk toonde aan dat twee parasietproteïnen, GDV1 en een DNA-bindend eiwit genaamd AP2-G, centraal staan in deze beslissing. GDV1 helpt het normaal stilgelegde ap2-g-gen te wekken, en AP2-G zet op zijn beurt een reeks genen aan die seksuele ontwikkeling aandrijven. De huidige studie wilde een andere proteïne onderzoeken, een kinase genaamd STK2, maar stuitte in plaats daarvan op een veel ingrijpendere vondst in AP2-G zelf.
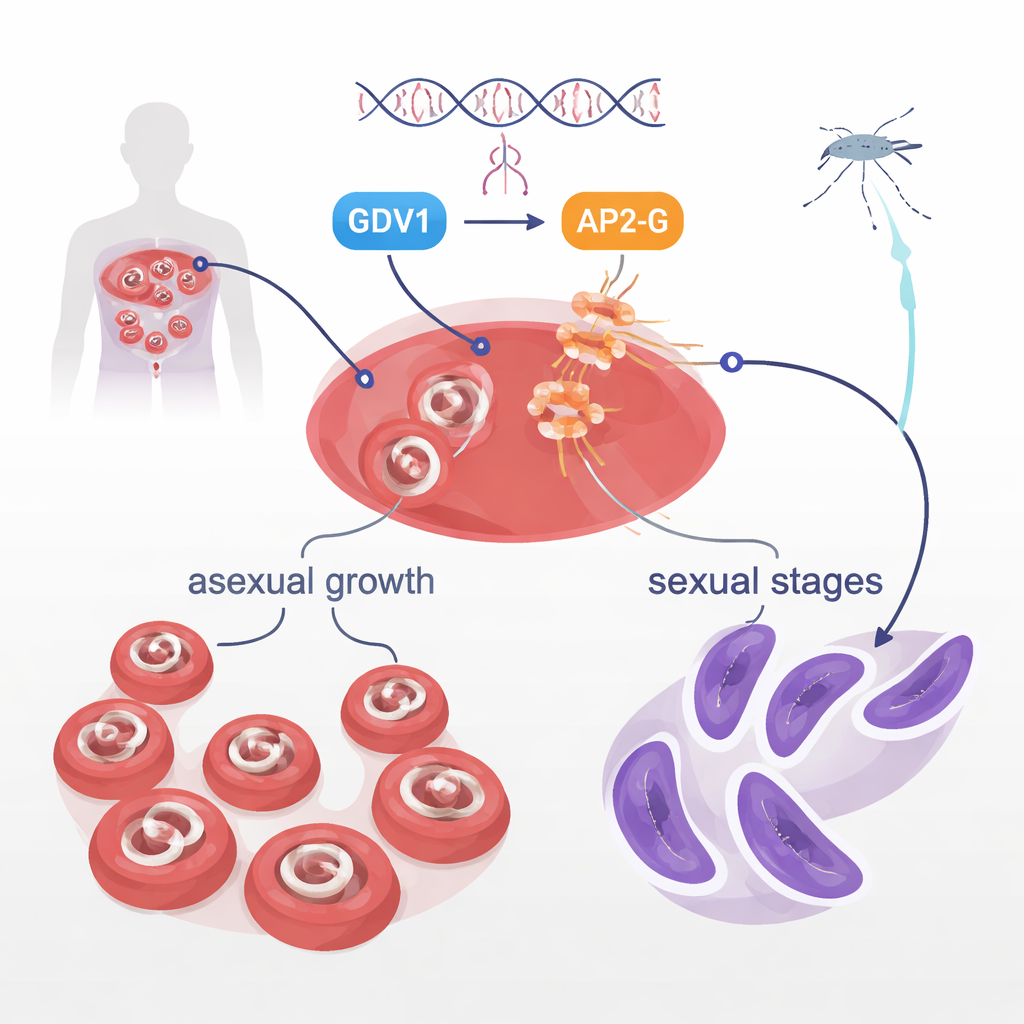
Een enkel aminozuur dat transmissie stopt
Toen de onderzoekers het stk2-gen verwijderden in één laboratoriumstam, merkten ze dat deze parasieten volledig hun vermogen om gametocyten te produceren verloren, terwijl ze aseksueel nog gewoon groeiden. Verrassend genoeg vormden gametocyten normaal toen vergelijkbare bewerkingen in een andere stam werden herhaald. Volledig-genoomsequencing onthulde de verborgen dader: één enkele “letter”wijziging in het ap2-g-gen, waarbij één aminozuur, valine, werd vervangen door een zeer vergelijkbaar aminozuur, leucine, op positie 2163. Deze positie ligt aan het begin van het DNA-bindende gebied van AP2-G, het deel dat fysiek specifieke DNA-motieven vastgrijpt om genen aan te zetten. Deze kleine valine-naar-leucinewisseling alleen was voldoende om de vorming van gametocyten te aboleren. Toen wetenschappers deze mutatie in normale parasieten integreerden, verdwenen gametocyten; wanneer ze het weer terugzetten naar valine, werd de seksuele ontwikkeling volledig hersteld.
Hoe de switch het moleculaire slot breekt
Om te begrijpen waarom deze subtiele verandering zo verwoestend is, combineerde het team computermodellering met laboratoriumexperimenten. Structuurvoorspellingen suggereerden dat het vervangen van valine door leucine de precieze vorm van het AP2-DNA-bindingsdomein verschuift en destabiliseert. In proefbuisassays met gezuiverde eiwitten bond normaal AP2-G sterk aan zijn voorkeurs-DNA-sequentie, een korte code met het motief “GnGTAC.” De mutant AP2-G met leucine op positie 2163 bindde deze sequentie daarentegen helemaal niet. Zonder stabiele DNA-binding kon AP2-G zijn eigen gen niet meer inschakelen (een positieve terugkoppelingslus die autoregulatie wordt genoemd) of tientallen downstream-genen activeren die nodig zijn om parasieten op het seksuele traject te brengen. Functioneel werden de mutante parasieten “steriel”: ze konden de vormen die muggen infecteren niet produceren, hoewel ze in rode bloedcellen bleven floreren.
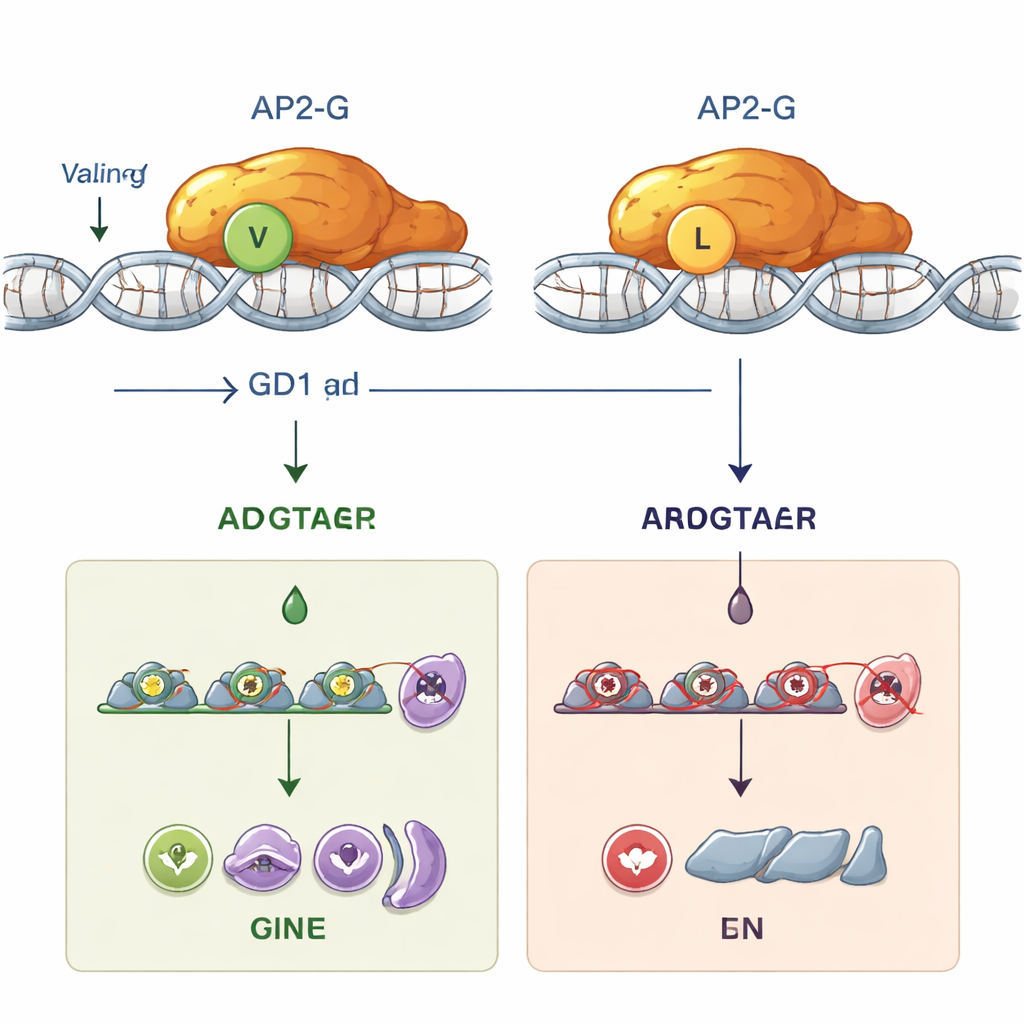
GDV1’s verborgen rol voordat AP2-G het overneemt
De mutatie gaf onderzoekers ook een uniek instrument: parasieten waarin het ap2-g-gen kan worden aangezet, maar AP2-G geen DNA kan binden. Met behulp van oplichtende reporters volgden ze wanneer verschillende spelers handelen tijdens de 48-uurscyclus van de parasiet in rode bloedcellen. Ze vonden dat het GDV1-eiwit als eerste verschijnt, vroeg in een stadium dat schizogonie wordt genoemd, en essentieel is om ap2-g uit zijn gesilenceerde staat te doen ontwaken. Deze vroege activatie trad op ongeacht of ap2-g normaal AP2-G of de gemuteerde versie codeerde. Pas later, zodra voldoende normaal AP2-G was opgebouwd, trad de sterke zelfversterkende lus in werking en werden andere “seksuele” genen geactiveerd. Een belangrijke marker, een eiwit genaamd MSRP1, lichtte alleen op in parasieten met functioneel AP2-G, wat een handig middel biedt om vroege en late seksueel gecommitteerde parasieten te onderscheiden. In gemuteerde lijnen met de leucine-wissel kon GDV1 ap2-g nog steeds wekken, maar het gebrekkige AP2-G-eiwit kon het proces niet voortdrijven, waardoor de seksuele ontwikkeling stagneerde.
Gevolgen voor het stoppen van malariaverspreiding
Voor de algemene lezer is de conclusie eenvoudig: malariaparasieten vertrouwen op een uiterst gevoelig moleculair slot om te beslissen of ze overdraagbaar zullen zijn. Deze studie toont aan dat het veranderen van slechts één “tand” in dat slot—een enkele valine in AP2-Gs DNA-grijpende regio—voorkomt dat de parasiet ooit mug-infectieuze stadia vormt. Tegelijkertijd maakt het duidelijk dat een ander eiwit, GDV1, eerder optreedt als de sleutel om eerst het stille ap2-g-gen te ontgrendelen, voordat AP2-G zijn eigen productie versterkt en een breder seksueel programma activeert. Door deze opeenvolging van gebeurtenissen in kaart te brengen en reporter-parasietlijnen te creëren die oplichten wanneer elke stap plaatsvindt, levert dit werk krachtige hulpmiddelen om geneesmiddelen of menselijke factoren te screenen die seksuele commitment verstoren. Op de lange termijn zou het richten op AP2-Gs DNA-bindende regio of de GDV1-gedreven activatiestap de basis kunnen vormen van nieuwe strategieën die niet alleen malaria bij één patiënt genezen, maar de keten van transmissie geheel doorbreken.
Bronvermelding: Prajapati, S.K., Dong, J.X., Morahan, B.J. et al. A single valine to leucine switch disrupts Plasmodium falciparum AP2-G DNA binding and reveals GDV1’s role in ap2-g activation. Nat Commun 17, 1719 (2026). https://doi.org/10.1038/s41467-026-68416-1
Trefwoorden: malariatransmissie, Plasmodium falciparum, ontwikkeling van gametocyten, AP2-G, GDV1