Clear Sky Science · nl
Multimodale AI voor opportunistische screening, stadiering en risico‑stratificatie van progressie bij steatotische leverziekte
Waarom levervet en littekenvorming iedereen aangaan
Vettige leverziekte is niet langer zeldzaam of een nicheprobleem: ongeveer één op de drie volwassenen wereldwijd heeft extra vet in de lever, en dat aantal stijgt. Bij veel mensen blijft het stil, maar bij anderen leidt het tot gevaarlijke littekenvorming (fibrose), cirrose, leverkanker en hartproblemen. Tegelijkertijd krijgen miljoenen mensen al CT‑scans om andere redenen—pijn op de borst, controle na kanker of routinematige onderzoeken—zonder dat er specifiek naar de lever wordt gekeken. Deze studie stelt een eenvoudige maar krachtige vraag: kan kunstmatige intelligentie (AI) die bestaande beelden onopgemerkt scannen, verborgen leverziekte signaleren en artsen helpen ingrijpen voordat ernstige schade optreedt?
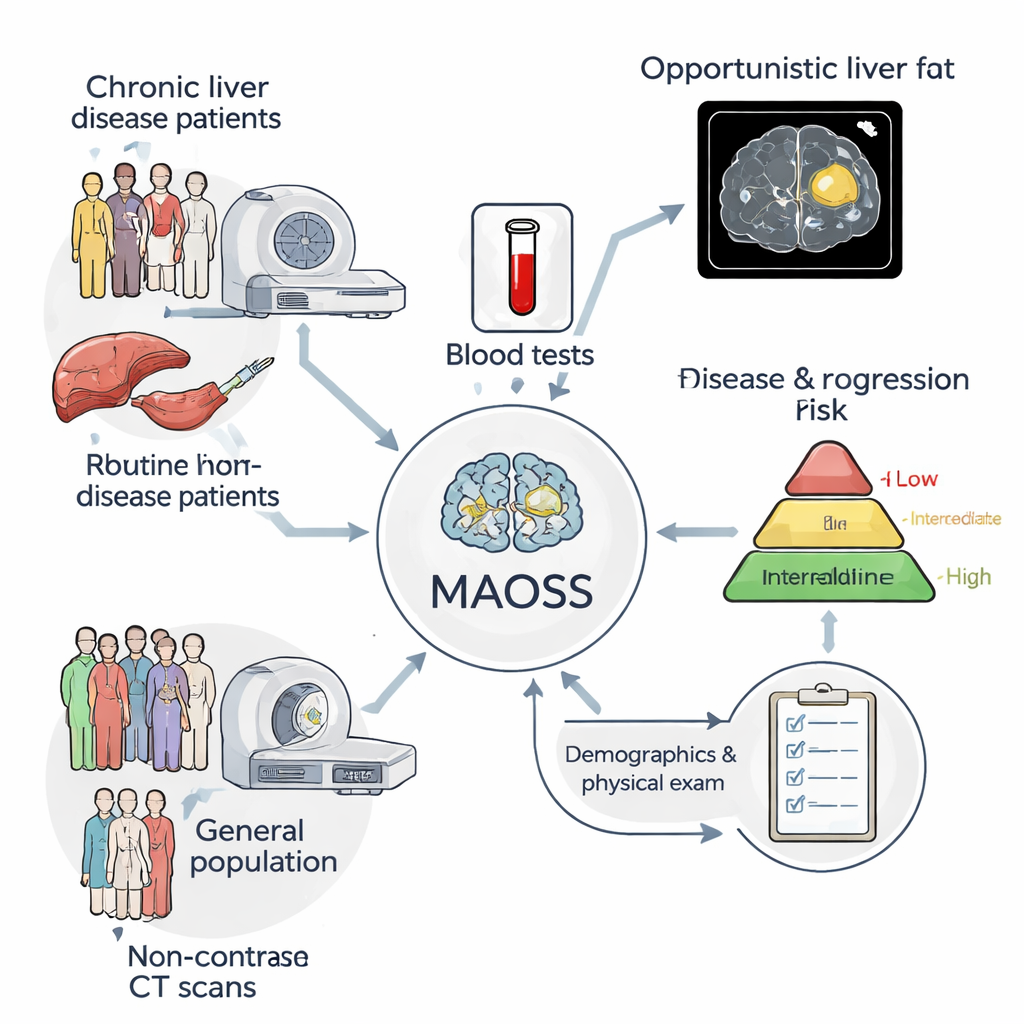
Een nieuwe AI‑hulp gebouwd op real‑world ziekenhuisdata
De onderzoekers ontwikkelden een multimodaal AI‑systeem genaamd MAOSS (Multi‑modal AI for Opportunistic hepatic Steatosis Screening). In plaats van te vertrouwen op één type informatie combineert MAOSS er drie: 3D niet‑geconstraste CT‑beelden van de lever, standaard bloedwaarden en basisgegevens zoals leeftijd en lichaamsgrootte. Het team trainde het systeem op meer dan 2.000 patiënten uit een groot Chinees ziekenhuis, waaronder bijna 1.000 van wie leverschilfers onder de microscoop waren onderzocht (de gouden standaard) en meer dan 1.100 met gedetailleerde radiologierapporten bij scans. Deze mix liet de AI leren van zowel de meest precieze labels (biopsieën) als de bredere, gemakkelijker te verzamelen rapporten die in de dagelijkse praktijk worden gebruikt.
De AI leren zowel vet als littekenweefsel te lezen
MAOSS is ontworpen om twee kernvragen van elke CT‑scan te beantwoorden: hoeveel vet zit er in de lever (steatose) en hoe gevorderd is eventuele littekenvorming (fibrose). Daartoe behandelt het model ziektestadia als een geordelde ladder—van geen, via mild en matig, naar ernstig—en leert het elke patiënt op de juiste sport te plaatsen. Een speciale “multimodale” opzet stelt het systeem in staat flexibel om te gaan met ontbrekende informatie; bijvoorbeeld, het kan nog steeds functioneren wanneer enkele bloedtesten ontbreken en dan meer vertrouwen op beeldvorming. De onderzoekers voegden ook een verklaringshulpmiddel toe gebaseerd op "integrated gradients", dat de specifieke regio’s en dichtheden binnen het leverbeeld benadrukt die de AI‑beslissing het sterkst beïnvloeden, waardoor clinici een warmtemap krijgen van vermoedelijke vetveranderingen.
Hoe goed MAOSS presteert vergeleken met huidige hulpmiddelen
Getest op afzonderlijke patiëntengroepen uit meerdere ziekenhuizen—including een externe cohorte en een groep met MRI‑gebaseerde metingen van levervet—toonde MAOSS hoge nauwkeurigheid bij het detecteren van zelfs milde leververvetting, met AUC‑waarden rond 0,90–0,93. Het presteerde ook sterk bij het identificeren van klinisch relevante fibrose, met AUC’s rond 0,82–0,89. Deze scores waren consequent beter dan modellen die alleen beelden, alleen klinische gegevens of standaard echografiegebaseerde maten zoals transient elastografie gebruikten. In een leessessie met 11 radiologen fungeerde MAOSS als assistent: toen artsen de AI‑score naast de CT kregen te zien, verbeterde hun vermogen om vroege stadia van vettige lever op te sporen merkbaar, vooral bij het onderscheiden van normale levers van die met subtiele ziekte.
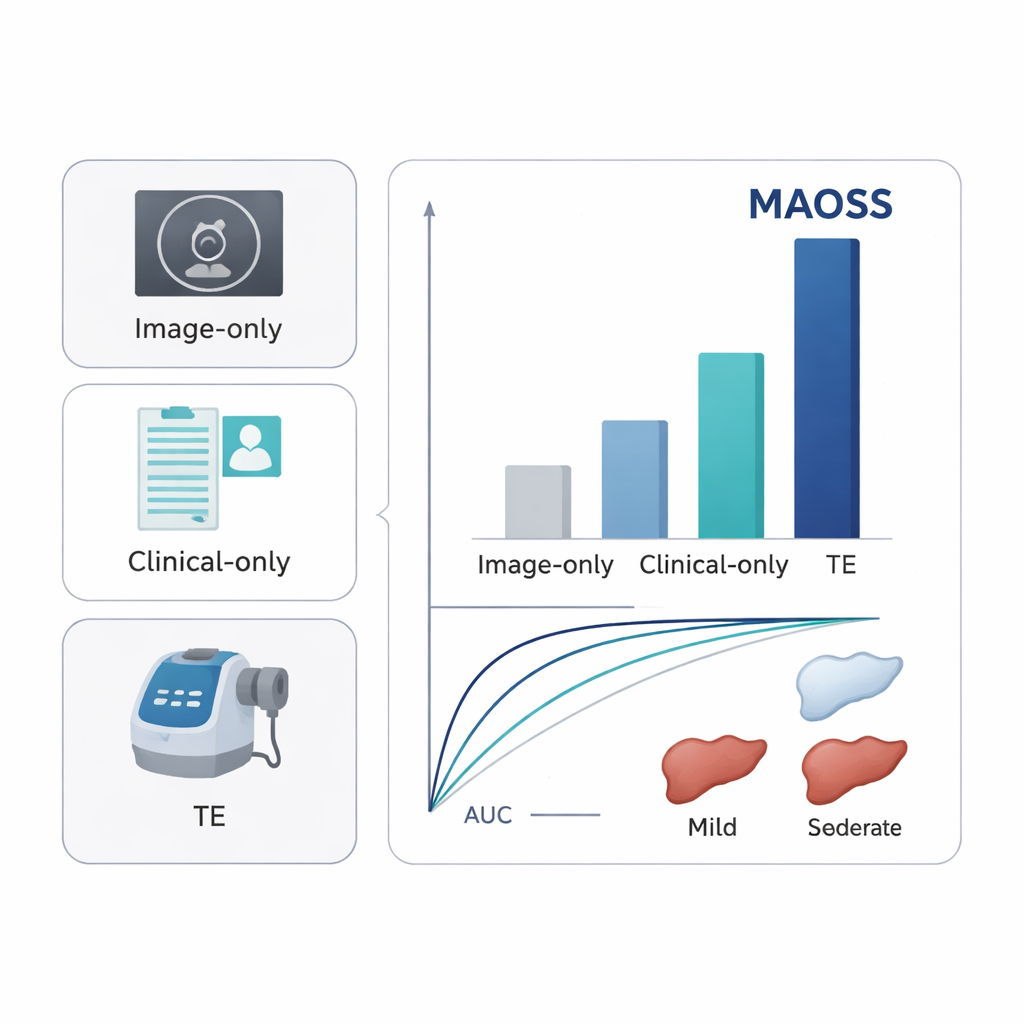
Routine‑scans omvormen tot een vroegwaarschuwingssysteem
Het team vroeg zich vervolgens af hoe MAOSS zou werken in de rommelige realiteit van de dagelijkse geneeskunde. Ze pasten het systeem toe op meer dan 18.000 real‑world CT‑scans uit spoedeisende hulp, opgenomen patiënten, poliklinieken en gezondheidsonderzoekcentra, waarvan de meeste oorspronkelijk waren aangevraagd om redenen die niets met de lever te maken hadden. MAOSS’ inschattingen van “vettige lever” versus “geen vettige lever” kwamen goed overeen met radiologierapporten, vooral in grote cohorten van lichamelijke onderzoeken. Vervolgens koppelden ze MAOSS aan een gevestigde klinische richtlijn die bepaalt welke patiënten met een vettige lever naar specialistische zorg moeten worden verwezen. In een biopt‑geïnformeerde groep van 1.192 mensen identificeerde het MAOSS‑verrijkte traject ongeveer een derde meer patiënten met risico op progressie naar steatohepatitis of gevorderde fibrose dan de standaardaanpak die alleen op echografiematen is gebaseerd, terwijl het nog steeds veilig laag‑risico individuen uitsloot.
Wat dit betekent voor patiënten en toekomstige zorg
Voor de leek is de kernboodschap dat dezelfde CT‑scans die al worden gemaakt voor andere gezondheidsproblemen stilletjes kunnen fungeren als een screeningsysteem voor leverziekte, zonder extra afspraken of invasieve procedures. Door CT‑beelden automatisch te lezen naast routinematige bloedtesten kan MAOSS vettige lever en verontrustende littekenvorming eerder opsporen dan traditionele methoden, radiologen helpen subtiele ziekte te zien die ze anders zouden missen, en patiënten nauwkeuriger indelen in laag, intermediair en hoog risico op progressie naar cirrose. Hoewel de auteurs opmerken dat grotere, langer lopende studies nodig zijn en de AI niet perfect is, suggereren hun resultaten dat multimodale AI een belangrijk onderdeel kan worden van het voorkomen van ernstige leverziekte voordat die ongemerkt voortschrijdt.
Bronvermelding: Gao, Y., Li, C., Chang, W. et al. Multi-modal AI for opportunistic screening, staging and progression risk stratification of steatotic liver disease. Nat Commun 17, 1562 (2026). https://doi.org/10.1038/s41467-026-68414-3
Trefwoorden: vettige leverziekte, medische AI, CT‑beeldvorming, leverfibrose, opportunistische screening