Clear Sky Science · nl
Hiërarchische mechanismen regelen de verwijdering van DNA-schade–gestopte RNA-polymerase II
Wanneer genkopieermachines een blokkade tegenkomen
Elke seconde reizen miljoenen kleine moleculaire machines, RNA-polymerase II genoemd, langs ons DNA om genen naar RNA te kopiëren. Maar wanneer het DNA beschadigd is — bijvoorbeeld door ultraviolette (UV) straling van de zon — kunnen deze machines vastlopen. Als vastgelopen polymerasen zich ophopen, kunnen cellen hun genen niet goed meer aflezen, wat vooral gevaarlijk is voor hersencellen en kan leiden tot zeldzame aandoeningen zoals het Cockayne-syndroom. Deze studie onthult in detail hoe onze cellen deze geblokkeerde machines detecteren en ofwel herstarten of verwijderen voordat ze blijvende schade veroorzaken.
Een nieuwe manier om cellulaire verkeersopstoppingen te observeren
Om te begrijpen hoe cellen geblokkeerde polymerasen opruimen, bouwden de onderzoekers een tijdsafhankelijke "verkeerscamera" voor transcriptie. Ze gebruikten een medicijn dat bestaande RNA-polymerase II-moleculen laat doorbewegen maar voorkomt dat nieuwe starten, en creëerden vervolgens een klein plekje UV-schade in elke celkern. Door een specifiek chemisch label op de actieve vorm van de polymerase te volgen, konden ze zien hoe snel die verdween uit de beschadigde zone in vergelijking met de rest van het genoom. Parallel ontwikkelden ze een aanvullende test die de totale hoeveelheid actieve polymerase in celextracten bekeek, wat niet alleen onthulde wanneer polymerasen het DNA verlieten, maar ook wanneer ze door het afbraaksysteem van de cel werden afgebroken.
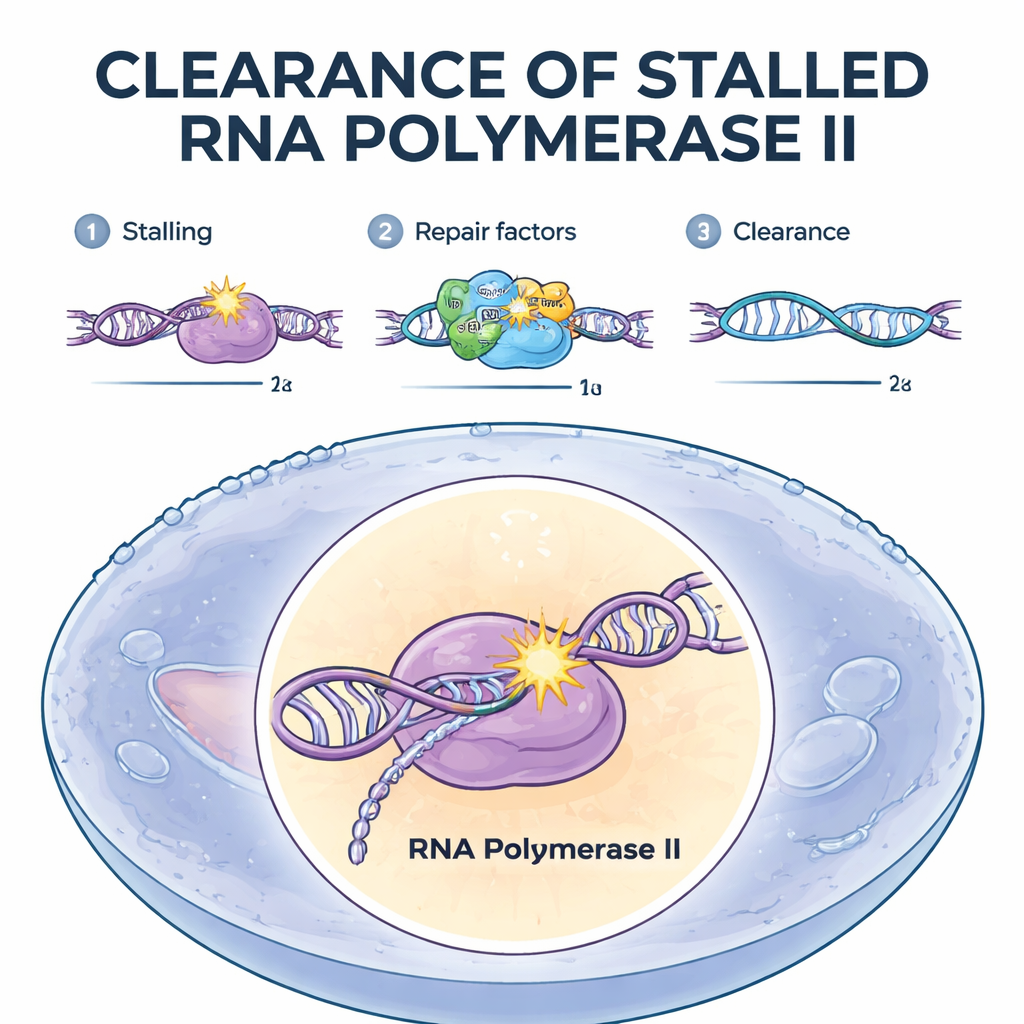
De vastgelopen machines markeren voor verwijdering
Het team richtte zich op transcription-coupled repair, een gespecialiseerd herstelmechanisme dat beschadigingen in actief afgelezen genen repareert. Ze gebruikten een bij elkaar passende reeks humane cellijnen, waarvan elke cellijn één verschillend reparatiefactor miste. Twee eiwitten, CSB en CSA, bleken beslissende poortwachters. Wanneer één van beide ontbrak, stapelde polymerase II zich op en bleef hardnekkig op de beschadigingsplaatsen zitten, en de cel faalde in de afbraak ervan. Biochemisch misten deze cellen ook het vermogen om kleine ubiquitine-tags aan een sleutelplaats op de polymerase te bevestigen. Daarentegen maakten cellen zonder latere reparatie-eiwitten — degenen die het beschadigde DNA wegsnijden en vervangen — de polymerase nog steeds normaal vrij. Dit toonde aan dat de initiële ubiquitinering van de vastgelopen polymerase de kritieke trigger is voor het bepalen van het lot ervan.
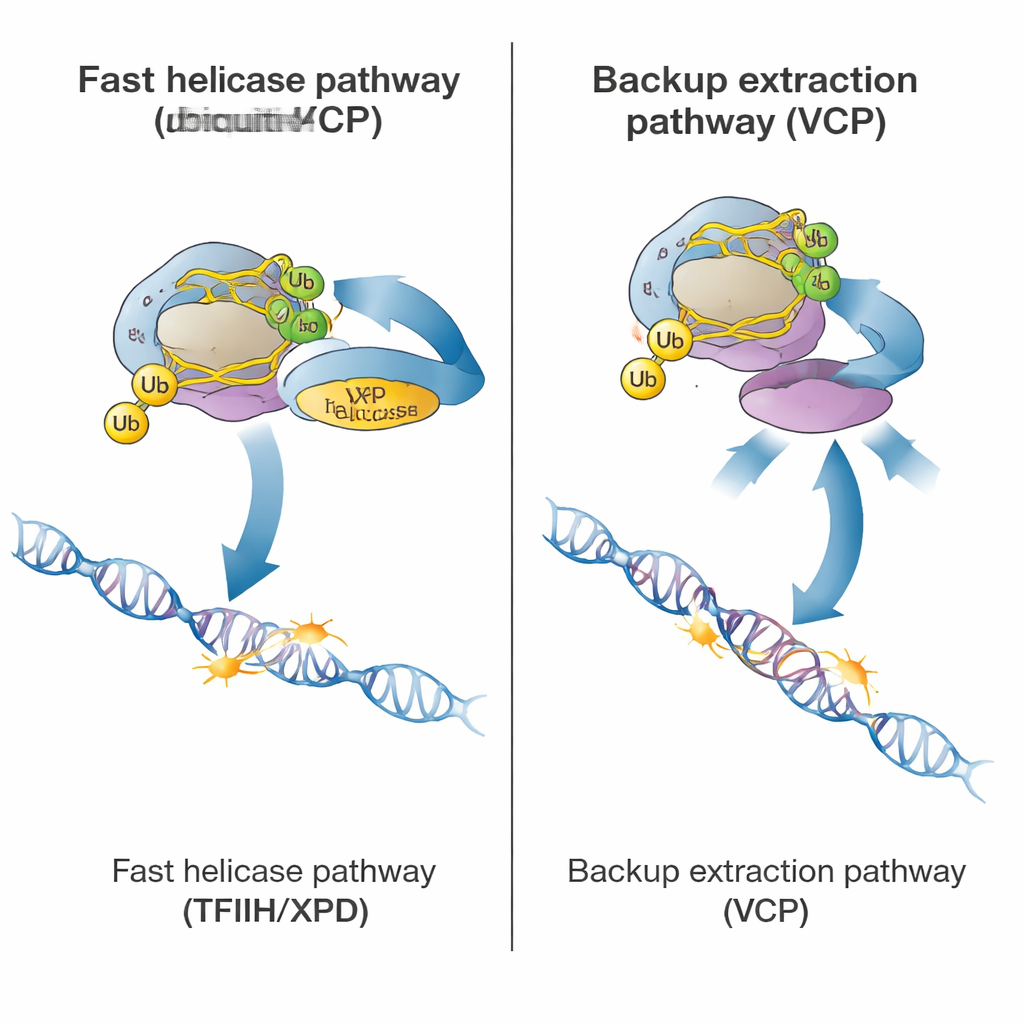
Twee opruimploegen: één snel, één als back-up
Zodra de polymerase is gemarkeerd, kan de cel kiezen tussen twee manieren om hem te verwijderen. De primaire, snelle route berust op een groot reparatiecomplex genaamd TFIIH, en in het bijzonder zijn XPD-helicase-subunit, dat energie gebruikt om DNA te ontwinden. Hulp-eiwitten, waaronder ELOF1, UVSSA en STK19, brengen TFIIH naar de vastgelopen polymerase en positioneren XPD op het DNA net voor de polymerase. Met nieuwe tests in patiëntencellen die een helicase-dode XPD-mutatie dragen, lieten de auteurs zien dat wanneer XPD het DNA niet kan ontwinden, het vrijmaken van de polymerase dramatisch vertraagt, ook al is de rest van het reparatiemechanisme aanwezig. Dit geeft aan dat de mechanische trekkracht van XPD normaal gesproken de polymerase losrukt van de beschadiging zodat reparatie-enzymen de plek kunnen bereiken.
Een trage maar essentiële plan B
De studie onthulde ook een langzamere, noodroute voor het vrijmaken van vastgelopen polymerase. Deze route is afhankelijk van VCP (ook bekend als p97), een eiwit dat ubiquitine-tags herkent en eiwitten krachtig uit chromatine kan verwijderen. In gezonde cellen met volledig functioneel TFIIH had blokkering van VCP slechts een klein effect. Maar in cellen waarin TFIIH ontbrak, verkeerd gepositioneerd was of helicase-dood was, werd de vrijmaking van polymerase bijna volledig afhankelijk van VCP. In deze situaties kon VCP nog steeds de gemarkeerde polymerase van het DNA trekken, zelfs wanneer normale reparatie niet kon doorgaan. Cruciaal is dat deze back-uproute nog steeds enige ubiquitinering vereiste, wat verklaart waarom cellen zonder CSB of CSA — en dus zonder ubiquitine-merken — in zowel de primaire als de back-uproutes faalden.
Waarom dit belangrijk is voor gezondheid en ziekte
Samengevoegd schetst het werk een hiërarchisch veiligheidsprogramma dat cellen gebruiken telkens wanneer RNA-polymerase II op DNA-schade stuit. Eerst markeren CSB en CSA de vastgelopen machine met ubiquitine. Als alles naar behoren werkt, rukken TFIIH en zijn XPD-helicase vervolgens snel de polymerase los zodat de beschadiging kan worden weggesneden en hersteld. Als TFIIH zijn werk niet kan doen, treedt VCP in om de polymerase te extraheren en naar afbraak te sturen, waardoor wordt voorkomen dat hij de genexpressie verstopt, ook al blijft de DNA-schade zelf bestaan. Dit kader helpt verklaren waarom erfelijke defecten in CSB of CSA bijzonder ernstige neurologische problemen veroorzaken: zonder ubiquitine-markering verliezen cellen zowel de primaire reparatiegestuurde route als de back-upextractieroute, waardoor vastgelopen polymerasen op beschadigde genen blijven kleven en transcriptie chronisch geblokkeerd raakt.
Bronvermelding: van der Meer, P.J., Yakoub, G., Tsukada, K. et al. Hierarchical mechanisms control the clearance of DNA lesion–stalled RNA polymerase II. Nat Commun 17, 1647 (2026). https://doi.org/10.1038/s41467-026-68413-4
Trefwoorden: transcription-coupled DNA-reparatie, RNA-polymerase II, UV-geïnduceerde DNA-schade, eiwit-ubiquitylatie, Cockayne-syndroom