Clear Sky Science · nl
In situ-visualisatie van fenotypische heterogeniteit en enkelvoudige celmorfologie van Clostridioides difficile tijdens darminfectie
Waarom darmbacteriën zich niet allemaal hetzelfde gedragen
Clostridioides difficile, vaak C. diff genoemd, is een beruchte ziekenhuisbacterie die ernstige, soms levensbedreigende diarree kan veroorzaken nadat antibiotica de normale darmflora hebben verstoord. Toch kunnen individuele cellen heel verschillend gedrag vertonen, zelfs als ze genetisch identiek zijn en in dezelfde omgeving verkeren. Deze studie laat, met ongekende detailrijkdom, zien hoe enkele C. diff-cellen toxineproductie in- of uitschakelen en zelfs van vorm veranderen tijdens infectie van de darm van muizen, wat aanwijzingen geeft waarom de ziekte zo hardnekkig en moeilijk te behandelen kan zijn.
Een gevaarlijke darmindringer in realtime volgen
Om te begrijpen hoe individuele C. diff-cellen zich in het lichaam gedragen, moesten de onderzoekers een manier vinden om ze duidelijk te zien temidden van de dichte en diverse gemeenschap van darmmicroben. Ze ontwikkelden C. diff-stammen die continu helder opgloeien onder de microscoop, met speciale fluorescente eiwitten die de groeivoorwaarden of ziekmakend vermogen van de bacteriën niet verstoren. Door antibiotica-behandelde muizen te infecteren met deze oplichtende stammen en vervolgens de dikke darm in plakjes te snijden en te kleuren, konden ze de exacte locaties en het gedrag van duizenden individuele bacteriecellen binnen intact darmweefsel vastleggen. 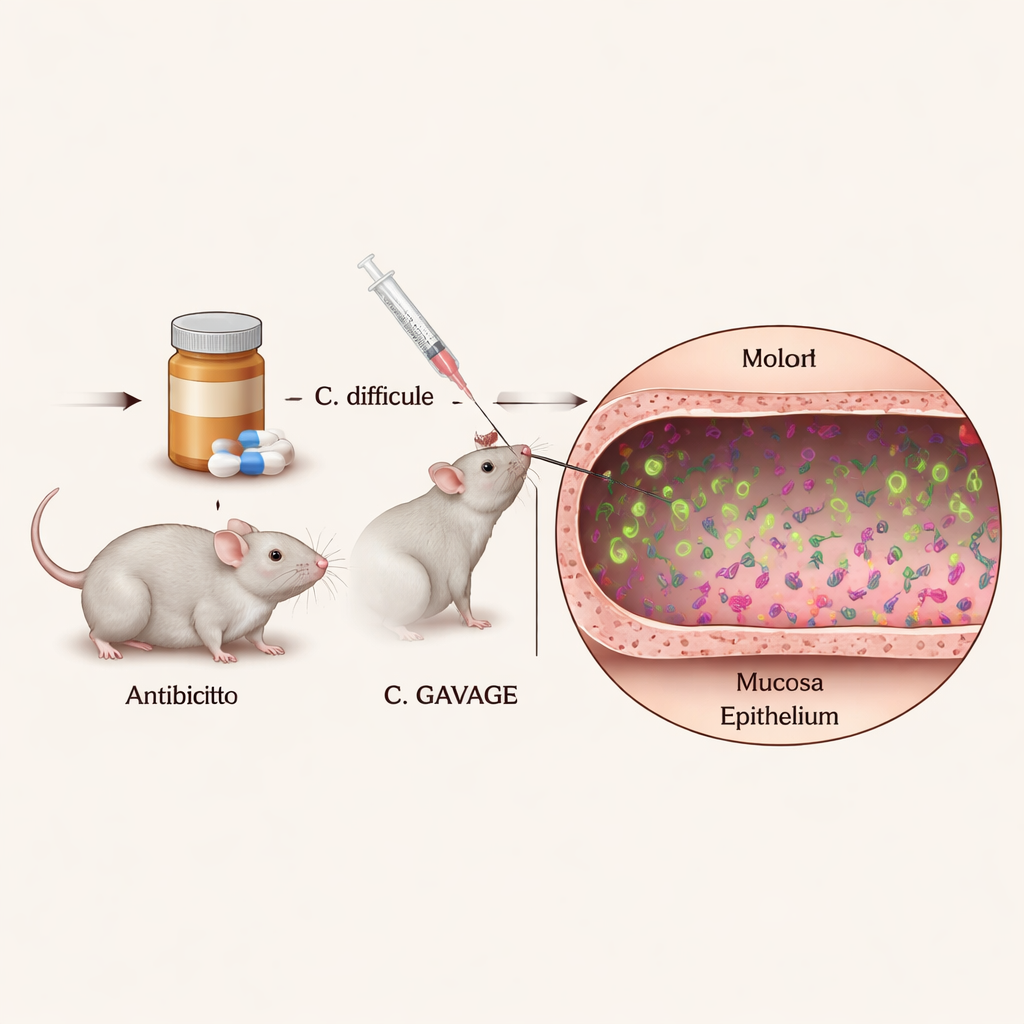
Waar de bacteriën in de dikke darm leven
De beelden toonden dat de meeste C. diff-cellen zich in het midden van de darminhoud bevinden, het lumen genaamd, wat bevestigt dat de soort voornamelijk een vrij drijvende “luminale” pathogeen is. Een opvallende minderheid van cellen verscheen echter consequent dicht bij de slijmlaag en direct naast het epitheliale oppervlak — de dunne cellaag die de darm bekleedt en als barrière naar de buitenwereld fungeert. Deze dichtbij-contact subpopulatie was in conventionele muizen met een normaal immuunsysteem eerder niet duidelijk waargenomen. Belangrijk is dat de ingebouwde fluorescente labels de bacteriën in de dieren niet merkbaar verzwakten, wat betekent dat de beelden waarschijnlijk weergeven hoe C. diff zich in een realistische infectie gedraagt.
Wie maakt toxine, en waar?
Vervolgens voegden de onderzoekers een tweede fluorescente signaal toe dat alleen aan gaat wanneer C. diff zijn toxinegenen activeert. Toxines zijn de schadelijke eiwitten die de darmwand beschadigen en de ziektesymptomen veroorzaken; ze worden ook door artsen in ontlastingstesten gemeten om infectie vast te stellen. Verrassend genoeg produceerden de bacteriën niet allemaal tegelijkertijd toxines. In plaats daarvan lichtte altijd maar een fractie van de cellen op als “toxine-ON”, zowel vroeg als laat in de infectie. Deze fractie was groter in een mutante stam die genetisch was ingesteld op overproductie van toxine, maar zelfs daar deed niet elke cel mee. Even opvallend was dat de positie van een cel — rondzwemmend in het lumen, gelegen in slijm, of in aanraking met het epitheel — niet sterk beïnvloedde hoe vaak toxine werd geproduceerd of hoe sterk die genen werden ingeschakeld. 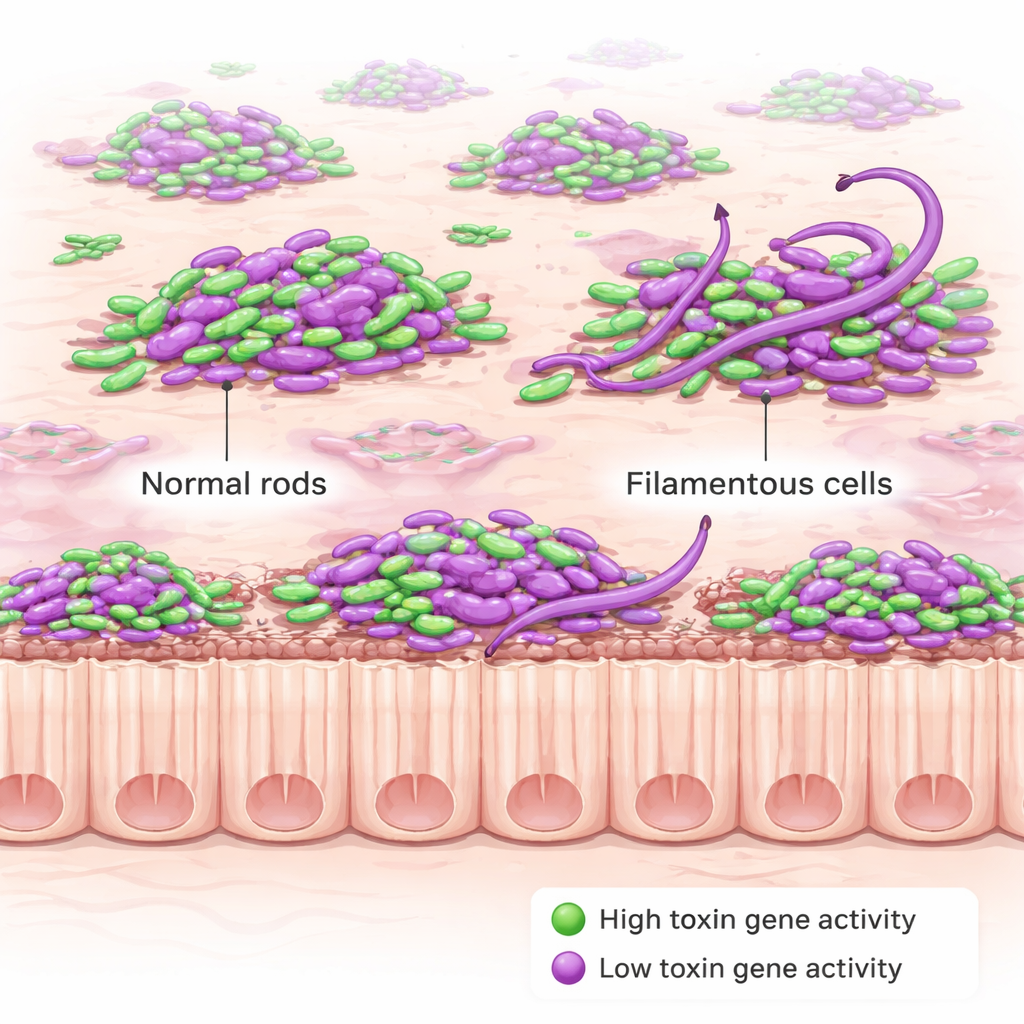
Vormveranderende cellen onder stress
Terwijl ze de toxineproductie in kaart brachten, stuitten de onderzoekers op een verrassend nieuw gedrag. In muizen geïnfecteerd met de toxine-overproducerende mutant werden veel C. diff-cellen tijdens de acute ziektefase uitzonderlijk lang, gebogen filamenten, sommige meer dan tien keer zo lang als normale korte staafjes. Deze “snoerachtige” morfologie trad vooral op tijdens vroege, ernstige infectie en nam later af; ze trad niet op wanneer dezelfde stam in laboratoriumbouillon werd gekweekt. Dat wijst erop dat de stressvolle omstandigheden in de ontstoken darm — en niet alleen de genetische verandering — deze dramatische vormverandering uitlokken. vervolgexperimenten toonden aan dat het verlies van een regulatoir eiwit genaamd RstA, dat zowel toxinegenen als andere stressreacties reguleert, bijdraagt aan de vorming van deze filamenten.
Wat dit betekent voor C. diff-ziekte
Voor niet-specialisten is de kernboodschap dat zelfs één stam van C. diff zich gedraagt als een verdeeld arbeidskorps. Sommige cellen betalen de energiekosten om toxine te produceren en de darm te beschadigen, en stellen zo voedingsstoffen vrij die hun toxinevrije buren kunnen benutten. Deze gedeelde “arbeidsdeling” kan helpen verklaren waarom de infectie kan aanhouden en terugkeren, omdat niet elke cel even kwetsbaar is voor behandelingen die zich richten op toxine of snel delende bacteriën. Het nieuw ontwikkelde oplichtende rapportagesysteem geeft wetenschappers een krachtig middel om cel voor cel te volgen hoe C. diff en aanverwante darmmicroben zich in tijd en ruimte binnen het lichaam aanpassen. Dat inzicht kan uiteindelijk therapieën sturen die niet alleen gericht zijn op het doden van bacteriën, maar op het ontregelen van de schadelijke rollen van specifieke subpopulaties die ziekte en terugkeer aanjagen.
Bronvermelding: DiBenedetto, N.V., Donnelly-Morell, M.L., Kumamoto, C.A. et al. In situ visualization of Clostridioides difficile phenotypic heterogeneity and single-cell morphology during gut infection. Nat Commun 17, 1716 (2026). https://doi.org/10.1038/s41467-026-68411-6
Trefwoorden: Clostridioides difficile, darmmicrobioom, bacteriële toxines, fenotypische heterogeniteit, fluorescente beeldvorming