Clear Sky Science · nl
Een nanosysteem dat zich richt op tissue inhibitor of metalloproteinase‑1 voor continue spatiotemporale therapie van idiopathische longfibrose
Waarom hardnekkige littekenvorming in de long ertoe doet
Idiopathische longfibrose (IPF) is een meedogenloze longaandoening waarbij normaal, sponsachtig longweefsel geleidelijk wordt vervangen door stijf littekenweefsel. Mensen met IPF krijgen kortademigheid bij dagelijkse activiteiten en de meeste overleven slechts een paar jaar na de diagnose. De geneesmiddelen van vandaag kunnen bij sommigen het ziekteverloop vertragen, maar herstellen zelden bestaande littekens en veroorzaken vaak bijwerkingen. Deze studie onderzoekt een slimme, inhalatie‑“nano‑therapie” die niet alleen IPF wil vertragen, maar actief littekenweefsel wil opruimen en de long helpt zichzelf te herstellen.
Het probleem: kleverige littekens en chemische stress
Bij IPF vullen de ruimtes waar zuurstof normaal in het bloed overgaat zich met overtollige eiwitten zoals collageen, waardoor flexibele luchtzakjes veranderen in stijve plekken. De auteurs richtten zich op een eiwit genaamd TIMP‑1, dat fungeert als een rem op natuurlijke enzymen die normaal overtollig collageen afbreken. Door longmonsters van patiënten en van muizen met geïnduceerde longfibrose te onderzoeken, vonden ze dat TIMP‑1‑niveaus meerdere malen hoger waren dan in gezonde longen en meestegen met collageenopbouw. Tegelijkertijd lieten beschadigde longen sterke stijgingen zien van reactieve zuurstofsoorten (ROS) — chemische “vonken” die cellen beschadigen — en een verlies van belangrijke merkers van gezonde luchtzakbekledende cellen. Samen wezen deze bevindingen op een vicieuze cirkel: te veel TIMP‑1 vertraagt de afbraak van littekens, terwijl oxidatieve stress de longstructuur verder beschadigt.
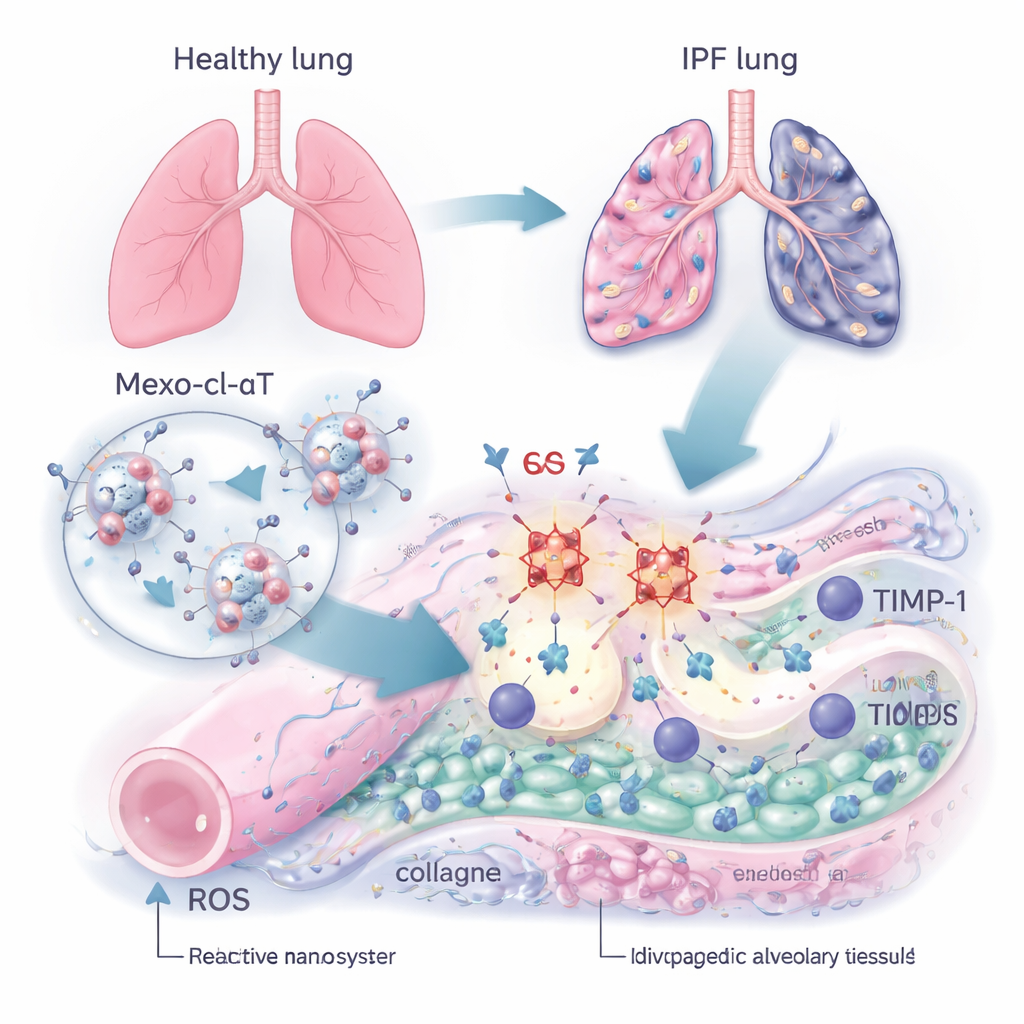
Een slim aflevervoertuig: kleine herstelpakketjes
Om deze cirkel te doorbreken bouwde het team een nanoschaaltherapie genaamd Mexo‑cl‑aT. Ze begonnen met exosomen — natuurlijke, belachtige deeltjes die door stamcellen worden uitgescheiden en die al bekendstaan om zich naar beschadigd weefsel te richten en genezing te ondersteunen. Op het oppervlak van deze exosomen hechtten ze antilichamen die specifiek binden aan TIMP‑1. De verbinding tussen exosoom en antilichaam werd gemaakt met een speciale chemische schakel die door ROS kan worden geknipt. Met andere woorden: de vijandige chemische omgeving van een geschrompelde long wordt als signaal gebruikt: wanneer het exosoom een beschadigd gebied met hoge ROS‑waarden bereikt, breekt de schakel, wordt een deel van de ROS opgeslokt en het antilichaam precies daar vrijgegeven waar TIMP‑1 geconcentreerd is, terwijl het exosoom zelf blijft bijdragen aan weefselherstel.
Hoe het nanosysteem zich gedraagt en werkt
In celonderzoeken lieten de onderzoekers zien dat Mexo‑cl‑aT stabiel blijft in vloeistof maar snel zijn antilichamen loslaat wanneer het wordt blootgesteld aan hoeveelheden waterstofperoxide die vergelijkbaar zijn met die in zieke longen. Tegelijkertijd verlaagt het systeem sterk de hoeveelheid aanwezig peroxide, wat zijn ROS‑opruimende rol bevestigt. In littekenachtige celmodellen verminderden de vrijgegeven antilichamen TIMP‑1‑niveaus en maakten ze enzymen vrij die collageen afbreken, terwijl het exosoomcomponent celsterfte verminderde, celgroei stimuleerde en wondsluiting versnelde in zowel long‑ als bloedvatcellen. In vergelijking met versies waarvan de schakel niet kon worden geknipt, verwijderde het ROS‑responsieve ontwerp meer collageen en verminderde het chemische stress effectiever, wat het belang van gecontroleerde afgifte onderstreept.
Testen in een ernstig model van longlittekenvorming
Het team testte de therapie vervolgens in muizen met gevorderde longfibrose veroorzaakt door het medicijn bleomycine, een model gekozen om laat‑stadium IPF na te bootsen. Een enkele dosis geïnhaleerd Mexo‑cl‑aT bleef dagenlang in de longen aanwezig en behield meer antilichaam dan een simpele mix van de afzonderlijke componenten. Behandelde longen zagen er gezonder uit voor het blote oog en onder de microscoop: luchtruimtes openden zich weer, de dikte van littekens nam af en de totale collageeninhoud keerde bijna naar normaal terug. Merkers van geactiveerde littekenvormende cellen daalden, terwijl eiwitten gekoppeld aan gezonde bekleding van luchtzakjes en bloedvaten stegen. Chemische metingen toonden aan dat de behandeling TIMP‑1‑niveaus scherp verlaagde, de balans van collageen‑opruimende enzymen herstelde en ongeveer driekwart van de overtollige ROS verwijderde. Belangrijker nog, ontstekingsmetingen namen af en bloedonderzoeken en orgaanonderzoeken toonden geen duidelijke toxiciteit.
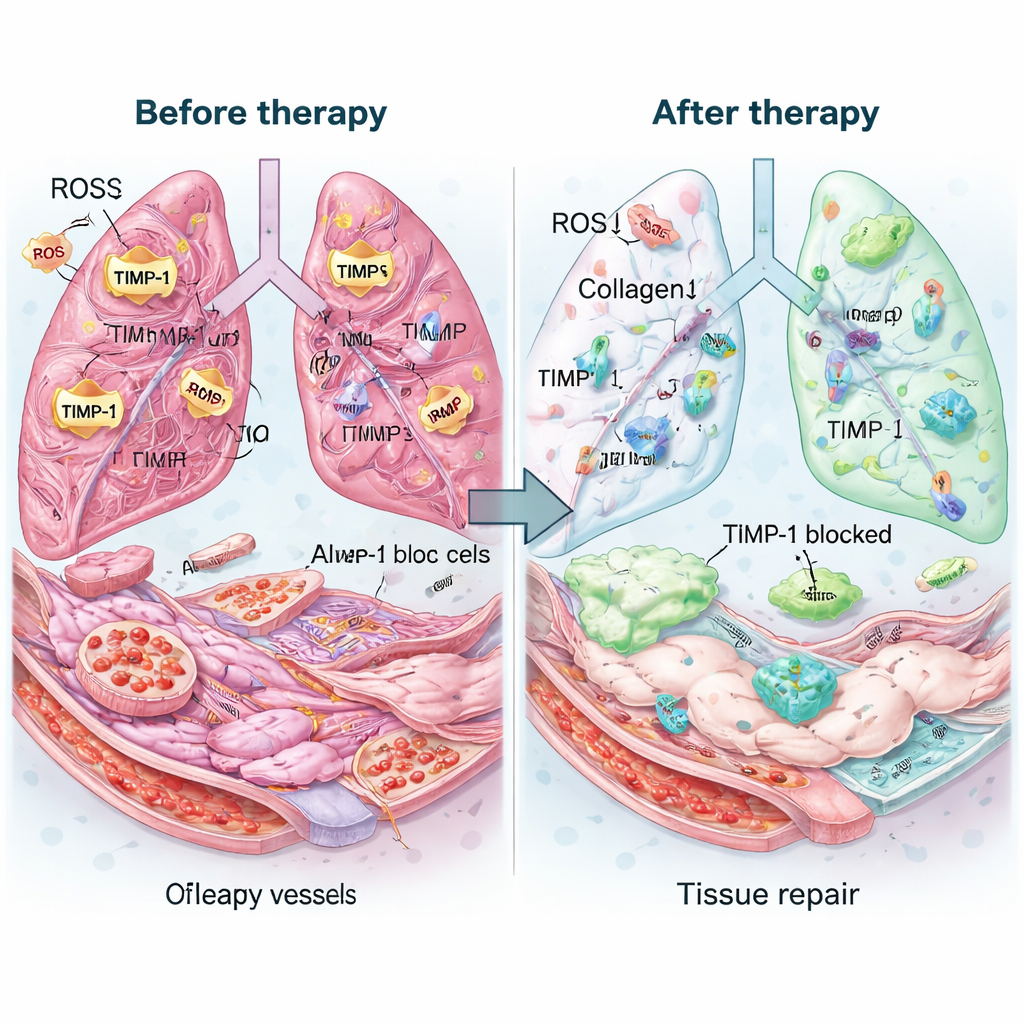
Wat dit voor patiënten zou kunnen betekenen
Voor mensen die met IPF leven biedt dit werk nog geen directe genezing, maar het introduceert een veelbelovende strategie. In plaats van alleen nieuwe schade te vertragen, richt het Mexo‑cl‑aT‑nanosysteem zich op het actief terugdraaien van bestaande littekens, het kalmeren van schadelijke chemische stress en het ondersteunen van het herbouwen van kwetsbaar longweefsel — allemaal in een gerichte, geïnhaleerde vorm die de behandeling concentreert waar die het meest nodig is. Hoewel uitdagingen zoals grootschalige productie van exosomen en testen bij mensen blijven, suggereert de studie dat precieze nano‑therapieën afgestemd op de zieke omgeving op een dag kunnen veranderen hoe hardnekkige longlittekenvorming, en mogelijk andere fibrotische aandoeningen, worden behandeld.
Bronvermelding: Li, C., Lu, G., Chen, H. et al. A nanosystem targeting tissue inhibitor of metalloproteinase-1 for continuous spatiotemporal idiopathic pulmonary fibrosis therapy. Nat Commun 17, 1694 (2026). https://doi.org/10.1038/s41467-026-68398-0
Trefwoorden: idiopathische longfibrose, littekenvorming in de long, nanomedicijn, exosoomtherapie, TIMP‑1