Clear Sky Science · nl
Beschadigde epitheliale celtoestanden beïnvloeden de overleving van niervoorplantaten na T-celgemedieerde afstoting
Waarom dit nieronderzoek belangrijk is voor patiënten
Niertransplantaties kunnen levensreddend zijn, maar veel transplantaten falen jaren na de operatie, zelfs wanneer artsen de immuunreactie die bekendstaat als T‑celgemedieerde afstoting onder controle lijken te hebben. Deze studie stelt een eenvoudige maar cruciale vraag: als de immuunreactie onder de microscoop als “behandeld” lijkt, waarom slijten sommige getransplanteerde nieren dan toch vroegtijdig? Door in getransplanteerde nieren van muizen en mensen tot op het niveau van individuele cellen in te zoomen, onthullen de onderzoekers een verborgen laag van schade in de filterbuisjes van de nier die helpt verklaren welke graften overleven en welke niet.
Voorbij de klassieke tekenen van afstoting kijken
Artsen stellen T‑celgemedieerde afstoting meestal vast door het zien van witte bloedcellen die de nier binnendringen en de kleine buisjes die urine verwerken aanvallen. Krachtige middelen tegen afstoting kunnen deze immuuncellen vaak verdrijven en de bioptie er beter laten uitzien. Toch lopen patiënten met dit type afstoting een hoog risico op verlies van het transplantaat. Eerdere grootschalige genstudies suggereerden dat signalen van weefselschade binnen niercellen de uitkomst beter voorspellen dan simple tellingen van immuuncellen. De auteurs wilden deze schadesignalen op single‑cell resolutie definiëren en testen hoe nauw ze samenhangen met langetermijn‑transplantoverleving.
Afstoting ontleden, cel voor cel
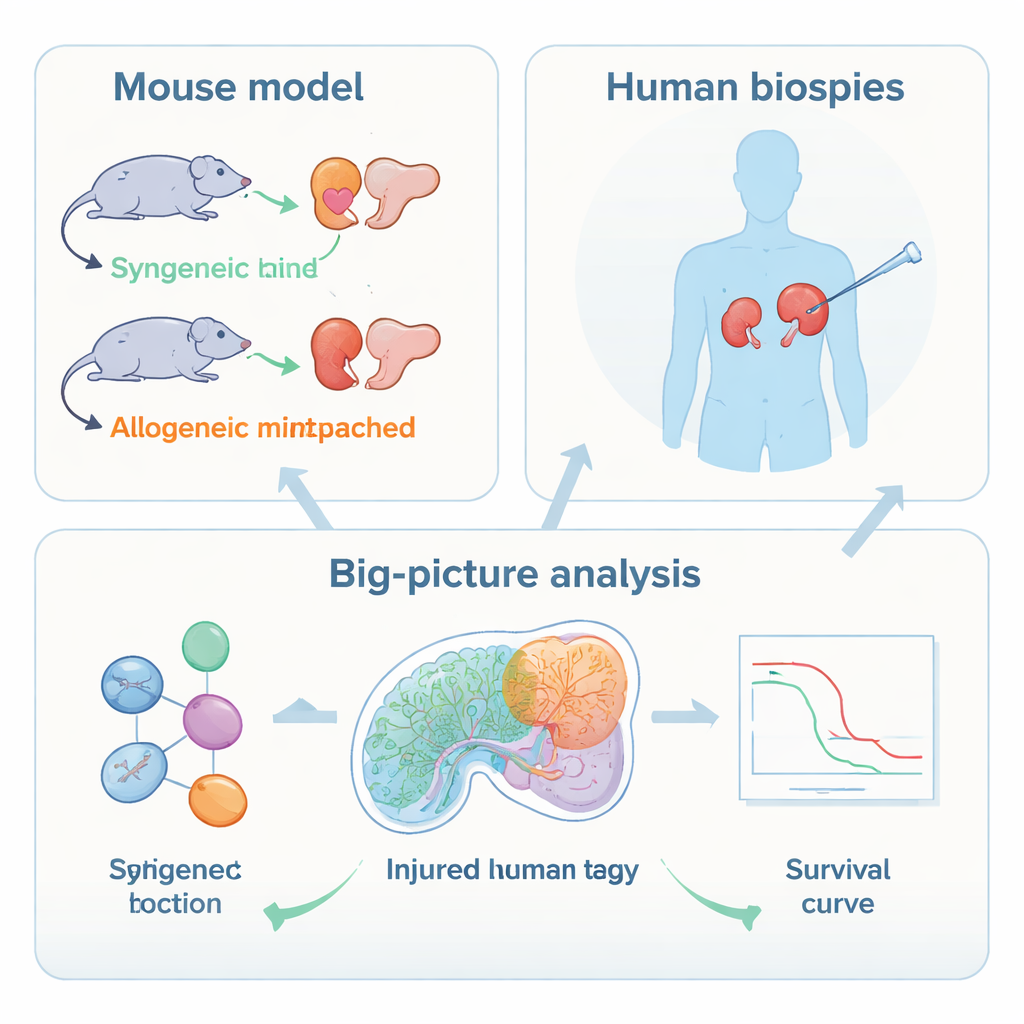
Het team gebruikte eerst een gecontroleerd muismodel, waarbij nieren werden getransplanteerd tussen genetisch identieke muizen of tussen niet‑gelijksoortige stammen om afstoting op te wekken. Vervolgens pasten ze single‑nucleus RNA‑sequencing toe, waarmee de activiteit van duizenden genen in individuele cellen wordt uitgelezen, en spatial transcriptomics, waarmee wordt aangegeven waar die cellen in de weefselsnede liggen. Deze methoden toonden dat tijdens afstoting de sterkste moleculaire veranderingen niet plaatsvonden in immuuncellen, maar in de epitheellaag van de nier zelf — met name in de cellen die de proximale tubuli en een segment dat de dikke opstijgende tak heet, bekleden. In deze gebieden schakelden cellen genen in die duiden op schade en stress, ontstekingssignalen en markers van een meer primitieve, minder gespecialiseerde toestand, terwijl ze transportfuncties terugschroefden die nodig zijn voor gezonde filtratie.
Verborgen pockets van ernstig beschadigde tubuluscellen
Door cellen met vergelijkbare genactiviteit te clusteren, ontdekten de onderzoekers meerdere afzonderlijke “schadetoestanden” binnen tubulaire cellen in de muizennieren. Sommige weerspiegelden vroege stressreacties, terwijl andere ernstig beschadigde, sterk gewijzigde cellen vertegenwoordigden die hun normale identiteit verloren hadden en veel ontstekings‑ en littekenvormingseiwitten produceerden. Ruimtelijke mapping liet zien dat deze celtoestanden zich niet gelijkmatig verspreidden: bepaalde ernstige schadetoestanden vormden vlekkerige pockets door de niercortex en de buitenste merglaag en bevonden zich in complexe buurten met T‑cellen, macrofagen en fibroblasten. Ter vergelijking: sommige beschadigde cellen in diepere regio’s waren verrassend geïsoleerd van immuuncellen, wat hint op verschillende manieren waarop schade kan ontstaan en voortduren.
Muisschadetoestanden koppelen aan menselijke transplantaten
De auteurs vroegen vervolgens of vergelijkbare celtoestanden ook bij mensen voorkomen. Ze analyseerden biopten van menselijke niertransplantaten met actieve T‑celgemedieerde afstoting en van stabiele graften. Single‑cell data toonden opnieuw beschadigde proximale tubuluscellen en cellen van de dikke opstijgende tak waarvan de genpatronen sterk overeenkwamen met de meest ernstig beschadigde muisceltoestanden. Met deze menselijke signaturen “deconvolueerden” de onderzoekers duizenden oudere bulk‑bioptie genexpressieprofielen en vonden dat ernstig beschadigde tubulus‑toestanden vaker voorkwamen bij T‑celgemedieerde en gemengde afstoting dan bij alleen‑antilichaamafstoting of geen afstoting. Belangrijk was dat ze compacte gencollecties opstelden die elk schadetoestand representeerden en die scoreden in een grote cohorte met gedetailleerde follow‑up.
Beschadigde tubuluscellen als voorspellers van graftlot
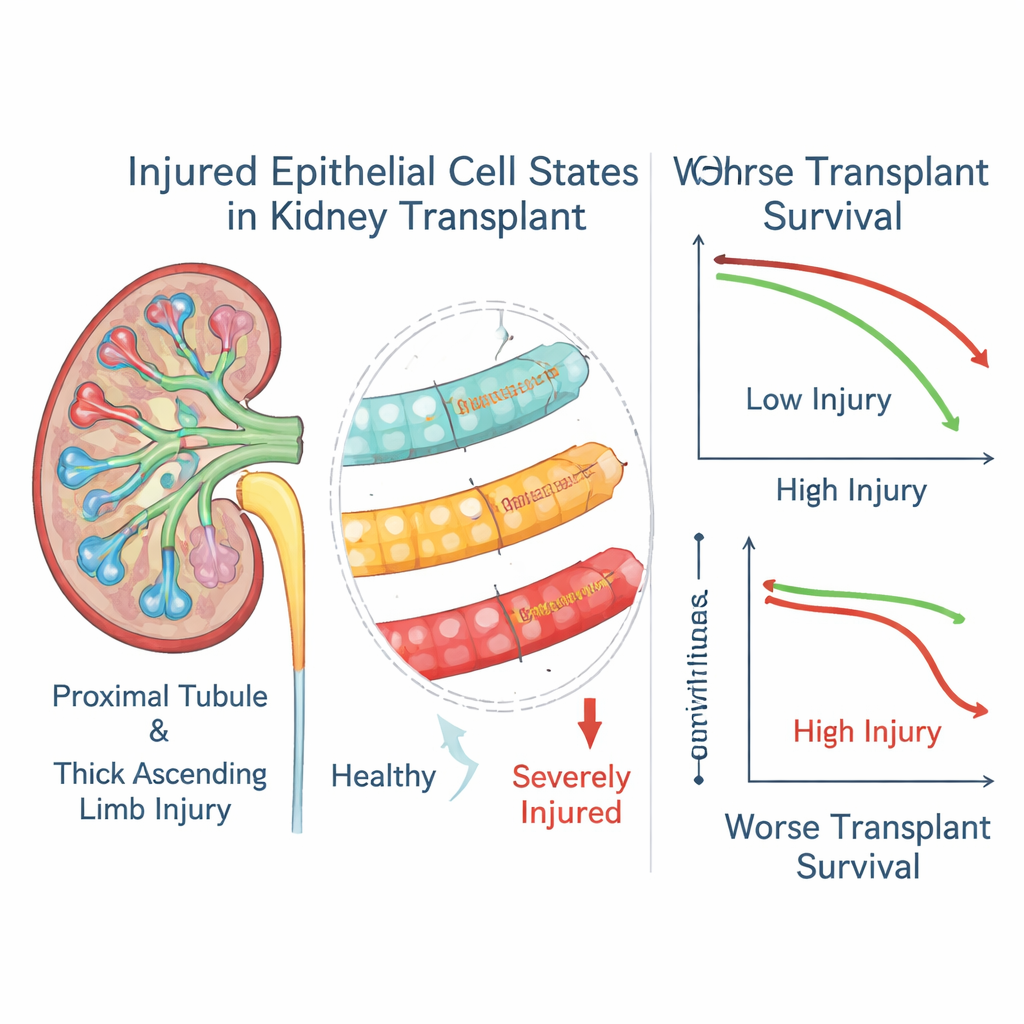
Toen de auteurs deze genschalen koppelden aan driejarenuitkomsten bij meer dan duizend transplantatieontvangers, ontstond een duidelijk patroon. Hoge niveaus van markers voor de meest ernstig beschadigde epitheliale toestanden in zowel proximale tubuli als dikke opstijgende takken waren sterk geassocieerd met een grotere kans op verlies van het transplantaat, zelfs bij patiënten wier biopten elders als behandeld werden geclassificeerd. Een mildere tubulusbeschadigingstoestand liet het omgekeerde zien en hing samen met betere overleving, wat suggereert dat dit een succesvoller herstelprogramma kan vertegenwoordigen. In een subset van patiënten met herhaalde biopsies bleven de “ernstige schade”-scores vaak langdurig hoog, lang nadat de afstotingsperiode kennelijk was opgelost, wat impliceert dat deze veranderde cellen kunnen aanhouden en de ziekte blijven beïnvloeden.
Wat dit betekent voor transplantatiezorg
Voor niet‑specialisten is de kernboodschap dat niet alle schade in een afgestoten nier direct door immuuncellen wordt veroorzaakt, en dat niet alle schade verdwijnt wanneer de immuunaanval tot rust komt. Deze studie toont aan dat hardnekkige pockets van ernstig beschadigde tubuluscellen fungeren als een vroeg waarschuwingssysteem voor toekomstig transplantaatverlies. Op termijn zouden eenvoudige tests gebaseerd op deze schadelijke gentranscripties — mogelijk zelfs met behulp van cellen die in de urine worden uitgeworpen — artsen kunnen helpen hoogrisicopatiënten te identificeren, behandelingen op maat te maken en te monitoren of nieren werkelijk herstellen. Het werk wijst ook op deze beschadigde epitheliale cellen zelf als potentiële doelen voor nieuwe therapieën die getransplanteerde nieren verder beschermen naast de gebruikelijke immuunsuppressie.
Bronvermelding: Pfefferkorn, A.M., Jahn, L., Gauthier, P.T. et al. Injured epithelial cell states impact kidney allograft survival after T-cell-mediated rejection. Nat Commun 17, 1060 (2026). https://doi.org/10.1038/s41467-026-68397-1
Trefwoorden: afstoting bij niertransplantatie, beschadiging van tubuluscellen, single-cell sequencing, transplantatie-overleving, epitheliale celtoestanden