Clear Sky Science · nl
Weergave van weefsel-specifieke Drosophila-stofwisseling identificeert door suikerarm dieet veroorzaakte metabole ontregeling in spier op reactie- en padniveaus
Waarom deze fruitvliegstudie van belang is voor de menselijke gezondheid
Te veel suiker in ons dieet kan het vermogen van het lichaam om brandstof te beheren onder druk zetten en uiteindelijk bijdragen aan type 2-diabetes. Deze studie gebruikt fruitvliegen om tot in opmerkelijke details te onthullen hoe verschillende weefsels met metabolisme omgaan en hoe een suikerrijk dieet de spierfunctie verstoort. Omdat vliegen veel metabolische genen en orgaansystemen met mensen delen, helpen deze inzichten te verklaren wat er in onze eigen spieren mis kan gaan bij langdurige suikeroverschot.
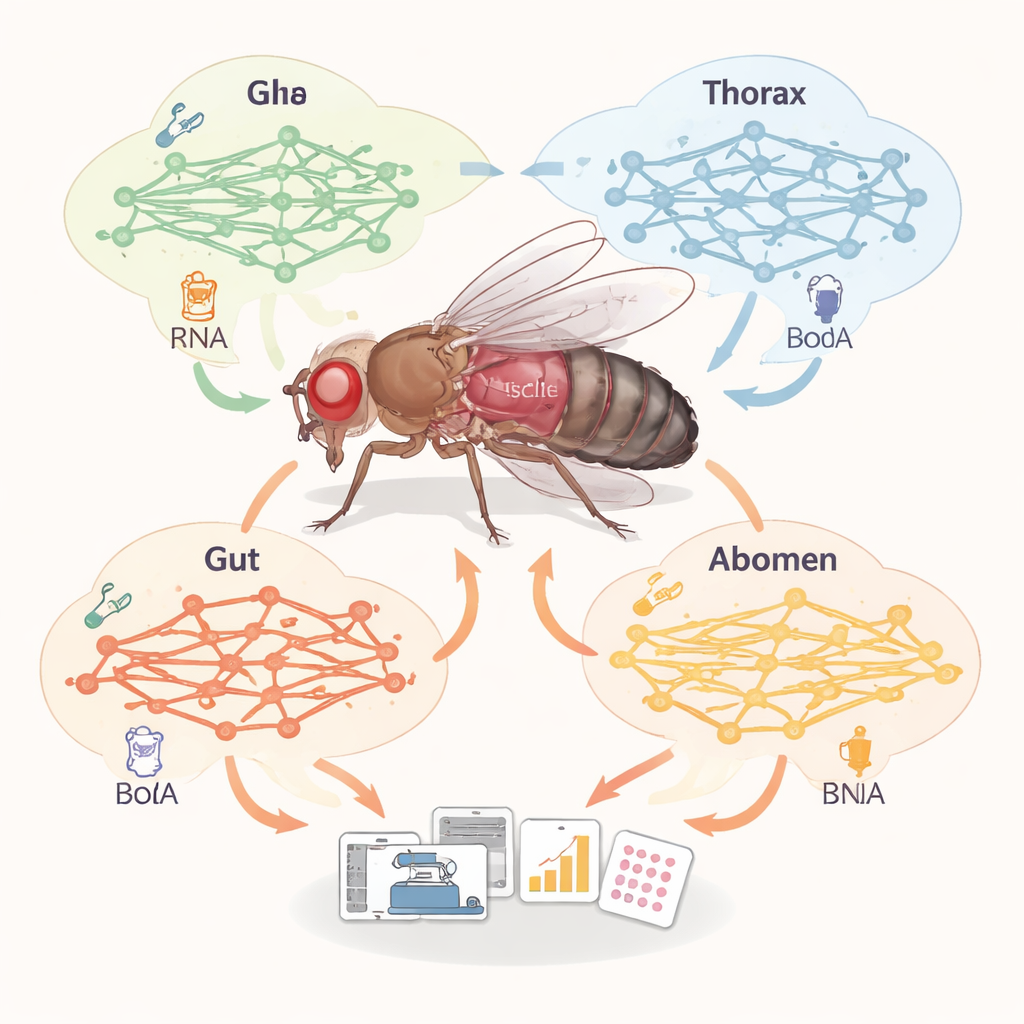
Metabolisme weefsel voor weefsel in kaart brengen
Ons lichaam, net als dat van fruitvliegen, bestaat uit weefsels die heel verschillende metabole rollen vervullen: spier verbrandt brandstof, vet slaat het op, de darm verwerkt voedsel, enzovoort. In plaats van elke enzymactiviteit rechtstreeks te meten, bouwden de onderzoekers grootschalige "kaarten" van het metabolisme — zogenaamde genoom-schaal metabole modellen — voor 32 verschillende vliegweefsels. Ze combineerden een bestaand, gecureerd netwerk van chemische reacties met single-cell genexpressiegegevens die aangeven welke metabolische genen in elk weefsel aanstaan. Zo konden ze vergelijken hoeveel reacties, metabolieten en genen actief zijn in elk weefsel-specifiek netwerk en zien welke paden in spier, vetlichaam, darm en verschillende zenuwcellen worden benadrukt.
Verschillende brandstoftaken voor verschillende organen
De vergelijking onthulde duidelijke metabole "persoonlijkheden" tussen weefsels. Het vetlichaam en oenocyten — vliegaanpakken van menselijk vet en lever — bevatten de rijkste set reacties, vooral die welke vetten verbranden via beta-oxidatie. Spier had daarentegen niet het grootste netwerk, maar wel het hoogste aandeel reacties die stoffen in- en uit de cellen verplaatsen, wat suggereert dat spier een belangrijk knooppunt is voor de uitwisseling van brandstoffen en bouwstenen met de rest van het lichaam. De wetenschappers controleerden ook of de voorspelde paden overeenkwamen met echte metabolietpatronen die in verschillende lichaamsregio's werden gemeten. Met gerichte metabolomica analyseerden zij honderden kleine moleculen uit vliegkoppen, thoraxen, darmen en abdomen en keken vervolgens of paden die in de gegevens verrijkt waren overlappen met die voorspeld door de modellen. In spier en vetlichaam was de overeenkomst sterk, wat vertrouwen geeft dat de weefsel-specifieke modellen de werkelijke biologische processen beter vastleggen dan genexpressie alleen.
Wat een suikerrijk dieet doet met de brandstofstroom in spier
Met een gevalideerd spiermodel simuleerde het team wat er gebeurt wanneer vliegen langdurig een suikerrijk dieet krijgen, een goed ingeburgerd model voor type 2-diabetes. Ze beperkten het model met bekende kenmerken van diabetische spier, zoals verminderde glucoseopname en vertraagde activiteit in de centrale energieketen in mitochondriën. Computationele "flux"-analyses — berekeningen van hoe snel reacties kunnen verlopen — toonden brede verminderingen in reacties die afhankelijk zijn van het redoxpaar NAD en NADH, moleculen die elektronen transporteren en essentieel zijn voor energieproductie. Met name reacties in het centrale suikerverbrandingspad, glycolyse, vertraagden, inclusief die gekatalyseerd door het enzym GAPDH. Het model voorspelde ook een ongeveer kwart daling in het vermogen van de spier om NADH te produceren, wat wijst op een belast redoxevenwicht. Rechtstreekse metingen in thoracale spier van vliegen bevestigden dat de verhouding NAD tot NADH inderdaad daalde onder een suikerrijk dieet.
Gevolgd gemarkeerde suiker en geoxideerde eiwitten
Om te zien of deze voorspelde knelpunten daadwerkelijk in levende dieren voorkwamen, voerden de onderzoekers vliegen met een suikerrijk dieet dat uniform gemarkeerde koolstof-13 glucose bevatte en volgden vervolgens waar de gemarkeerde koolstof terechtkwam. Ze vonden dat vroege glycolytische tussenproducten stroomopwaarts van GAPDH zich ophoopten, terwijl downstream producten en hun gemarkeerde fracties daalden, wat wijst op een echte vertraging bij en onder deze stap. Evenzo werden bijdragen van glucosekoolstof aan de centrale energieketen verminderd. Tegelijkertijd toonde redox-proteomica — een methode die oxidatieve veranderingen aan specifieke aminozuren in eiwitten detecteert — toegenomen oxidatie van veel glycolytische enzymen, inclusief meerdere sites op GAPDH. Gedurende de glycolyse hadden enzymen met meer oxidatieve modificaties de neiging grotere dalingen in voorspelde flux te vertonen, ook al bleven hun totale eiwitniveaus grotendeels ongewijzigd. Dit suggereert dat chemische schade door oxidatieve stress, in plaats van verlies van enzymhoeveelheid, een belangrijke oorzaak is van verminderde suikerverwerking in spier.
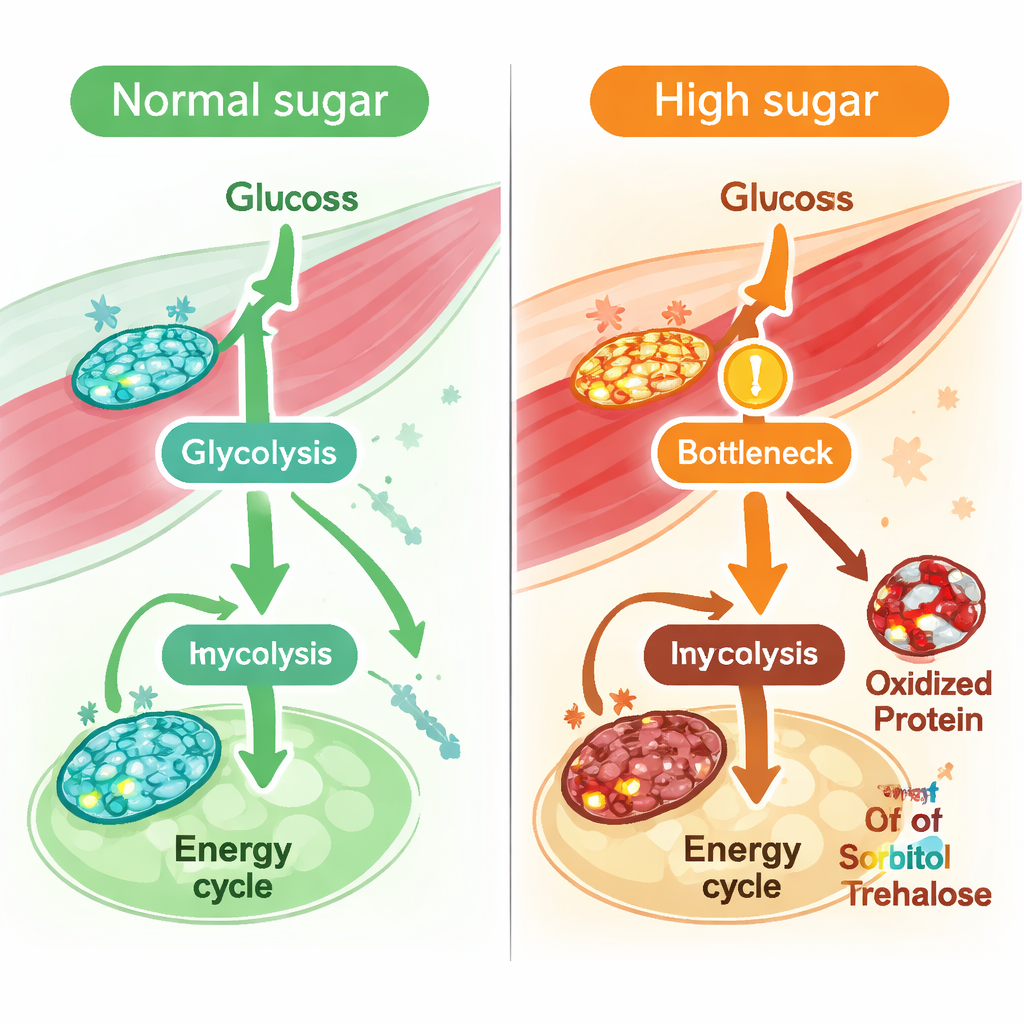
Verborgen problemen in de verwerking van fructose en sucrose
Kijkend voorbij individuele reacties, gemiddelden de onderzoekers fluxen over hele paden om te zien welke het meest verstoord werden door veel suiker. Glycolyse, de energieketen en oxidatieve fosforylering lieten allemaal dalingen zien, maar een van de sterkste voorspelde afnames betrof fructosemetabolisme. Metabolietprofilering van spier ondersteunde dit idee: sorbitol- en trehalose/sucrose-niveaus stegen, en een sleutelenzym dat trehalose in glucose omzet, trehalase, vertoonde zowel verminderde voorspelde activiteit als verhoogde oxidatie op een gevoelige methionineresidu. Samen wijzen deze bevindingen op een bredere verstoring in hoe spier dieet-suikers verwerkt — vooral fructose-achtige en sucrose-afgeleide brandstoffen — bij chronische suikerbelasting.
Wat dit betekent voor het begrip van diabetes
Kort gezegd toont dit werk aan dat te veel suiker niet alleen het bloed overstroomt; het vervormt ook geruisloos hoe spiercellen brandstof routeren en verbranden. Door gedetailleerde, weefsel-specifieke metabole kaarten voor de fruitvlieg te bouwen en deze te controleren met metabolomica, isotopen-tracing en redox-proteomica, laten de onderzoekers zien dat veel suiker redoxstress aanstuurt, sleutel-glycolytische enzymen zoals GAPDH oxideert, de suikerafbraak vertraagt en fructose-gerelateerde paden verstoort. Deze inzichten, verkregen in een goed hanteerbaar modelorganisme, bieden een krachtig kader om te bepalen welke reacties en paden het belangrijkst zijn om te beschermen of te herstellen in menselijke spier om type 2-diabetes te voorkomen of te behandelen.
Bronvermelding: Moon, S.J., Hu, Y., Dzieciatkowska, M. et al. Modeling tissue-specific Drosophila metabolism identifies high sugar diet-induced metabolic dysregulation in muscle at reaction and pathway levels. Nat Commun 17, 1692 (2026). https://doi.org/10.1038/s41467-026-68395-3
Trefwoorden: Drosophila-stofwisseling, weefsel-specifieke metabole modellen, hoge-suiker dieet, spierglycolyse, redoxregulatie