Clear Sky Science · nl
Mechanische verjonging van verouderde stamcellen en oud bot door chromatine‑remodellering
Waarom het belangrijk is botten jong te houden
Naarmate we ouder worden verliezen onze botten geleidelijk aan sterkte: ze worden dunner en brozer. Dat vergroot het risico op breuken, verlies van zelfstandigheid en chronische pijn. De meeste bestaande behandelingen richten zich op medicijnen die botafbraak vertragen of mineralen aanvullen, maar repareren niet rechtstreeks de veroudering van de stamcellen die bot opbouwen. Deze studie onderzoekt een ander perspectief: het gebruik van zorgvuldig gecontroleerde fysieke krachten — in plaats van geneesmiddelen — om verouderende botvormende stamcellen te „verjongen” en de botgezondheid en algemene fitheid bij oudere muizen te verbeteren.
Als de bouwers van het bot verouderen
Diep in ons bot bevinden zich beenmergmesenchymale stamcellen, de meesterbouwers die kunnen uitgroeien tot botvormende cellen. Met de leeftijd delen deze stamcellen minder vaak, vormen ze minder bot en vertonen ze klassieke kenmerken van cellulaire veroudering, zoals DNA‑schade en ontstekingssignalen. De onderzoekers vergeleken cellen van jongere en oudere menselijke donoren en vonden dat verouderde stamcellen niet alleen biochemisch anders waren — ze waren ook mechanisch zwakker. Ze genereerden minder interne trekkracht, hadden lossere interne steigers en toonden slechtere overdracht van mechanische signalen naar de celkern. In botweefsel van oude muizen verscheen een vergelijkbare achteruitgang: het sponsachtige botnetwerk was uitgekleed, belangrijke mechanische signaalproteïnen waren verminderd en verouderingsmarkers waren verhoogd.
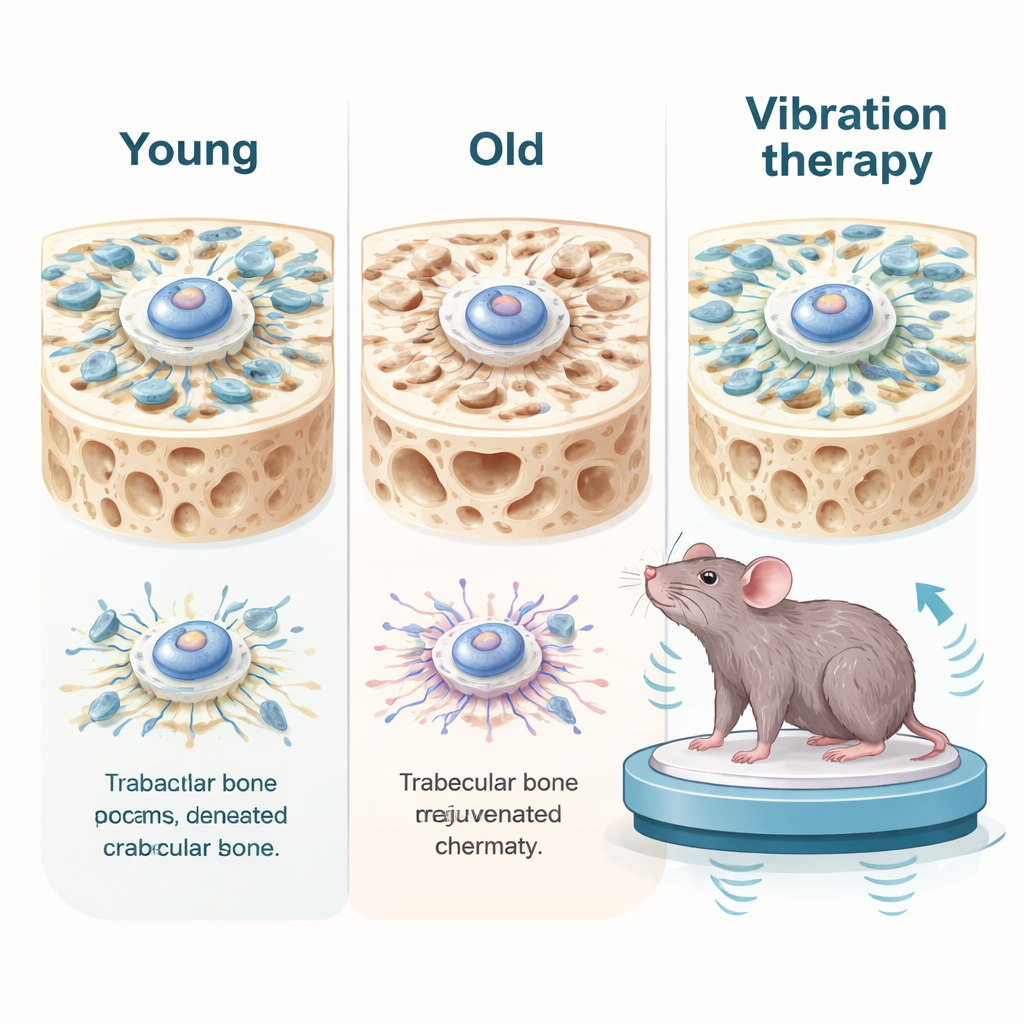
Cellen voorzichtig terugtrekken naar jeugd
Het team vroeg zich vervolgens af of het herstellen van mechanische kracht deze verouderingskenmerken kon omkeren. In petrischaaltjes brachten ze milde rek aan op senescente stamcellen of gebruikten ze een middel dat de activiteit van moleculaire motoren verhoogt. Deze behandelingen versterkten de cellulaire trekkrachten en verbeterden de organisatie van het interne skelet. Opvallend genoeg begonnen verouderde cellen er jonger uit te zien en te handelen: senescencemarkers daalden, DNA‑schade nam af en de cellen deelden zich weer gemakkelijker. Het omgekeerde bleek ook waar — wanneer ze de omgeving onder jonge cellen verzachtten of hun contractiele machinerie chemisch verzwakten, raakten de cellen in een verouderingsachtige toestand, vertraagden en zetten verouderingsmarkers aan, zelfs in een botnabootsend 3D‑gel.
Hoe kracht met genen praat
Om te begrijpen hoe fysieke krachten het celgedrag zo diepgaand konden veranderen, richtten de onderzoekers zich op chromatine — de verpakte vorm van DNA in de kern. In oude stamcellen was chromatine compacter en minder toegankelijk, waardoor het moeilijker werd voor nuttige genen om aan te gaan. Het herstellen van mechanische kracht zorgde ervoor dat het chromatine lokaal ontspande en de chemische merktekens die geassocieerd zijn met open, actieve DNA toenamen. Met een genoomwijde test voor chromatine‑toegankelijkheid vonden ze dat zachte mechanische stimulatie regio’s opende nabij genen die bij verouderingscontrole betrokken zijn. Eén gen, genoemd FOXO1, stak eruit als bijzonder gevoelig voor kracht. Bij toegenomen kracht werd het DNA‑gebied van FOXO1 opener, nam de activiteit toe en werden cellen minder senescent. Het blokkeren van FOXO1 maakte de voordelen van mechanische stimulatie ongedaan, waarmee het gen fungeert als een belangrijke schakel die fysieke belasting verbindt met genetische programma’s voor veerkracht en herstel.
De gouden balans van mechanische therapie vinden
Vervolgens testten de onderzoekers mechanische stimulatie in levende muizen. Oudere dieren werden geplaatst op een platform met laagintensieve trillingen voor korte dagelijkse sessies gedurende een maand, terwijl anderen hun achterpoten werden ontlast via staartopspanning, wat extreme inactiviteit nabootst. Bij oudere muizen versterkten zachte trillingen de mechanische signalering in het bot, verminderden ze verouderings‑ en ontstekingsmarkers en bouwden ze het sponsachtige botnetwerk deels opnieuw op. Het verbeterde ook gripkracht, uithoudingsvermogen bij inspanning, geheugengerelateerde taken en verlaagde ontsteking in bloed, lever en nieren. Wanneer trillingen echter continu werden toegepast zonder rustdagen, verdwenen de voordelen en keerde het effect zelfs om: de botstructuur verslechterde, DNA‑schade nam toe en ontsteking steeg. In celstudies veroorzaakten extreem sterke of te frequente rekken DNA‑breuken en duwden cellen terug in senescentie, wat aantoont dat mechanische kracht afhankelijk van de dosis kan genezen of schaden.
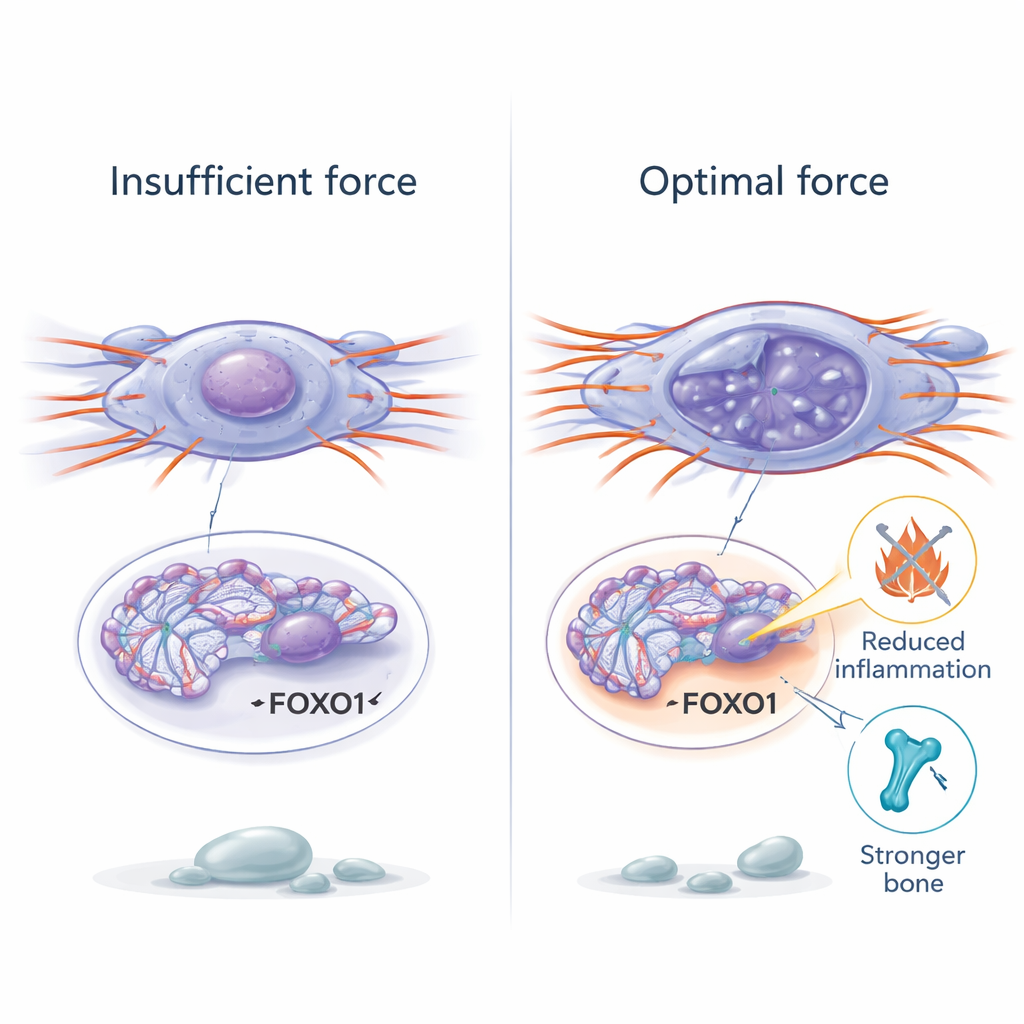
Van oefenimitaties naar toekomstige behandelingen
Voor de leek is de kernboodschap dat onze cellen niet alleen reageren op hormonen en chemicaliën — ze “luisteren” ook nauwgezet naar fysieke krachten. In dit werk tonen de auteurs aan dat matige, goed afgestelde mechanische stimulatie verouderende botstamcellen kan heractiveren, beschermende genprogramma’s zoals FOXO1 kan openen, verzwakt bot kan herbouwen en chronische ontsteking bij oudere muizen kan kalmeren. Tegelijkertijd versnelt te weinig of te veel kracht de cellulaire slijtage. Deze bevindingen suggereren dat zorgvuldig ontworpen mechanische therapieën — mogelijk specifieke bewegingsregimes of veilige trillingsapparaten — op een dag geneesmiddelen zouden kunnen aanvullen om botten, en mogelijk andere weefsels, langer gezonder te houden.
Bronvermelding: Liu, X., Ye, Y., Li, Z. et al. Mechanical rejuvenation of senescent stem cells and aged bone via chromatin remodeling. Nat Commun 17, 1684 (2026). https://doi.org/10.1038/s41467-026-68387-3
Trefwoorden: botveroudering, mechanische stimulatie, stamcelverjonging, chromatine‑remodellering, FOXO1