Clear Sky Science · nl
Precieze verwijdering van uitgebreide GGC-herhalingen in NOTCH2NLC met CRISPR/Cas9 voor de behandeling van neuronale intranucleaire inclusieziekte
DNA bewerken om een mysterieuze hersenaandoening aan te pakken
Neuronale intranucleaire inclusieziekte (NIID) is een zeldzame maar verwoestende hersenaandoening die dementie, bewegingsproblemen en zelfs vroegtijdig overlijden kan veroorzaken. Er is momenteel geen genezing. Deze studie onderzoekt of een krachtig genbewerkinstrument, CRISPR, kan worden gebruikt om een klein maar toxisch DNA-stukje dat NIID veroorzaakt uit te knippen, en biedt daarmee een vooruitblik op hoe toekomstige behandelingen onze genen zouden kunnen herschrijven om hersenziekten te bestrijden. 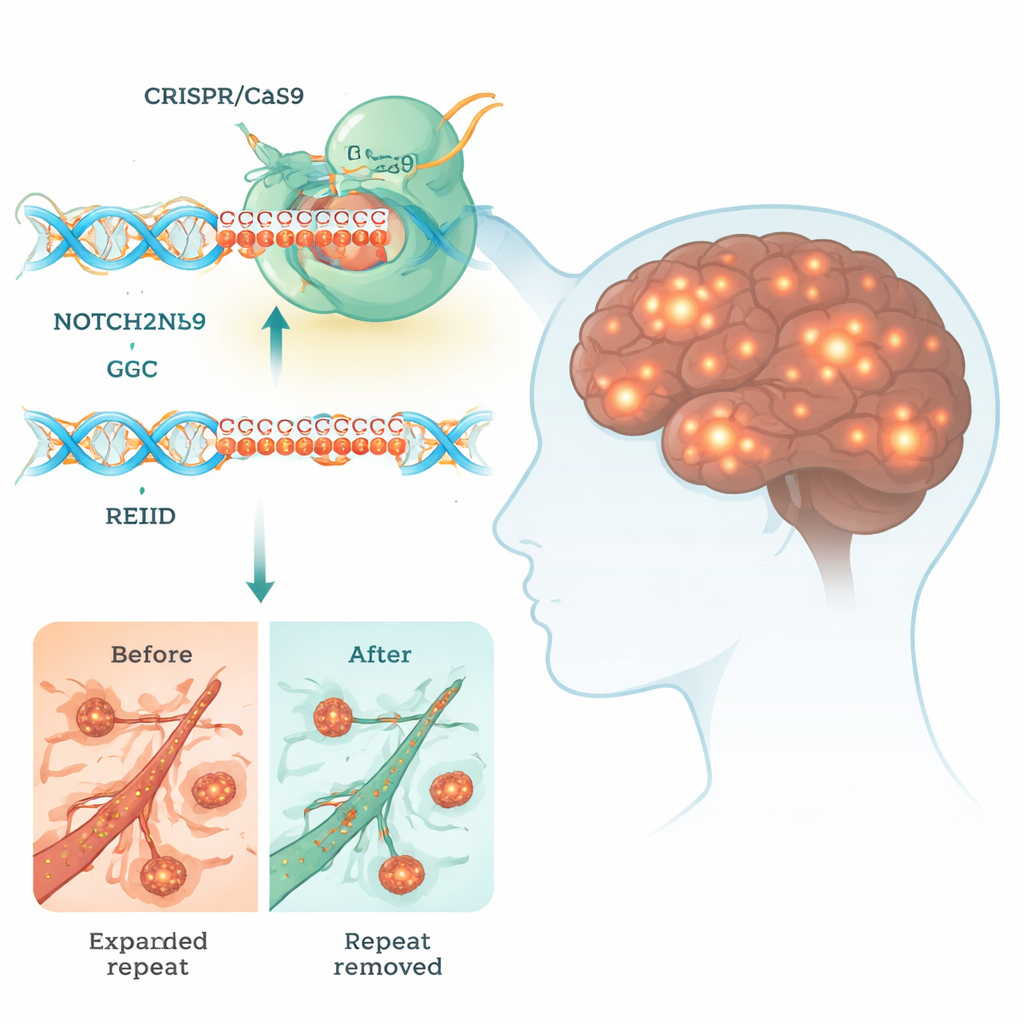
Een verborgen genetische dader
Veel erfelijke hersenaandoeningen worden veroorzaakt door korte DNA-sequenties die veel langer zijn geworden dan normaal. Bij NIID is het probleem een overmatige reeks van drieletter-eenheden, "GGC", in een gen dat NOTCH2NLC heet. Hoewel deze reeks in een regio ligt die niet direct codeert voor een klassiek eiwit, kan hij toch door het cellulaire machinerie worden afgelezen om abnormale polyglycine (polyG)-ketens te produceren. Deze kleverige ketens klonteren samen tot bolletjes in de kern van zenuwcellen en andere weefsels, en verstoren vitale processen zoals energieproductie, RNA-verwerking en het verkeer van moleculen tussen kern en cytoplasma.
De uitdaging van precieze genetische chirurgie
Het ontwerpen van een genbewerkingsbehandeling voor NIID is uitzonderlijk lastig omdat NOTCH2NLC meerdere bijna-identieke zustergenen heeft die belangrijk zijn voor de ontwikkeling van het menselijk brein. Als CRISPR de verkeerde knipt, kan het meer kwaad dan goed doen. De onderzoekers doorzochten daarom zorgvuldig het DNA rond de GGC-herhaling en vonden kleine sequentieverschillen die NOTCH2NLC onderscheiden van zijn verwanten. Vervolgens ontwierpen ze paren CRISPR-gids-RNA's die Cas9, de "moleculaire schaar", leiden om net voor en net na de uitgebreide herhaling te knippen. Deze duale-knipstrategie laat het herstelmechanisme van de cel het toxische segment verwijderen terwijl de rest van de genfamilie gespaard blijft.
Van cellen in een schaaltje naar patiënt-afgeleide neuronen
Het team testte hun CRISPR-ontwerp eerst in standaard menselijke cellen en in cellen die zo werden aangepast dat ze een grote NOTCH2NLC-herhaling droegen. In deze modellen knipte de editor efficiënt de herhaling eruit en daalden de niveaus van polyG-klonteringen met ruwweg de helft of meer. Daarna gingen ze verder met geïnduceerde pluripotente stamcellen (iPSC's) gemaakt van een patiënt met NIID en zetten deze cellen om in neurale voorlopercellen, een vroeg stadium van hersencellen. Met CRISPR verwijderden ze ofwel de uitgebreide herhaling, of vervingen ze die door een versie met normale lengte. Gedetailleerde DNA- en whole-genome-sequencing toonden aan dat het bewerken zeer nauwkeurig was, met weinig aanwijzingen voor ongewenste knipwonden, en de bewerkte cellen bleven zich normaal delen en rijpen. 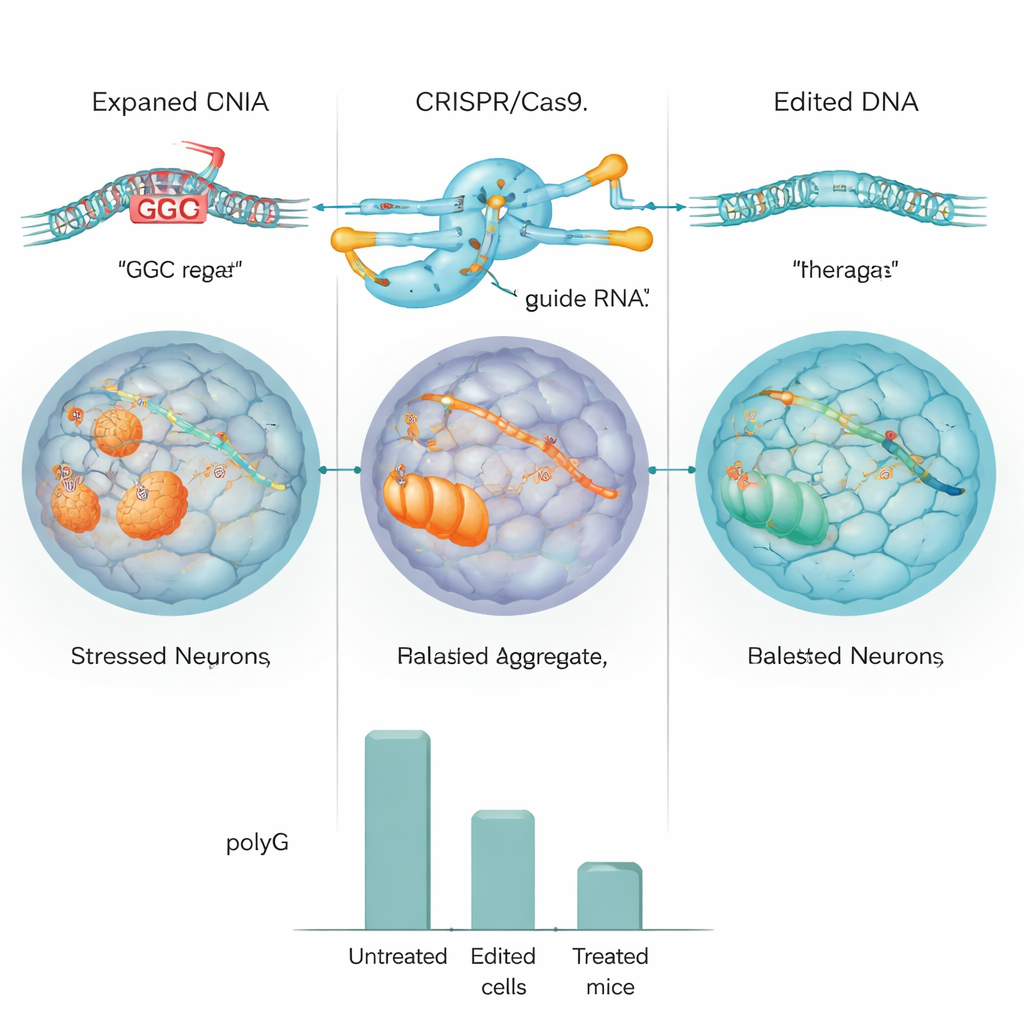
Herstel van brein en lichaam in een muismodel
Om te zien of deze aanpak daadwerkelijk de ziekte kon verbeteren, gebruikten de onderzoekers muizen die zo waren gemodelleerd dat ze de menselijke NOTCH2NLC-herhaling droegen en NIID-achtige kenmerken ontwikkelden, waaronder nucleaire inclusies, bewegingsproblemen en een verkorte levensduur. Ze verpakten het CRISPR-systeem in een gemodificeerd virus dat zich door de hersenen kan verspreiden na een eenvoudige injectie in de bloedbaan van pasgeboren muizen. Bij behandelde dieren werd de uitgebreide herhaling succesvol verwijderd in hersenweefsel. Als gevolg daarvan daalden de toxische polyG-niveaus scherp, verbeterden markers van zenuwcelgezondheid en verminderde abnormale activatie van ondersteunende hersencellen. Gedragstests toonden aan dat behandelde muizen meer bewogen, beter in balans waren en langer leefden dan hun onbehandelde nestgenoten. Vergelijkbare voordelen werden gezien in het hart, dat in dit model ook polyG ophoopt.
Wat dit zou kunnen betekenen voor toekomstige behandelingen
Voor leken is de kernboodschap dat NIID grotendeels lijkt te worden aangedreven door één specifieke te lange DNA-herhaling, en dat het precieze verwijderen van die herhaling veel ziektesignalen in cellen en muizen kan terugdraaien. Dit werk vertaalt zich nog niet naar een direct toepasbare menselijke therapie: onderzoekers moeten nog de langetermijnveiligheid verfijnen, de aflevermethoden verbeteren en testen in grotere, menselijker dieren uitvoeren. Maar de studie levert een sterke proof of concept dat zorgvuldig gericht genbewerken een toxische herhaling veilig kan uitschakelen terwijl nauw verwante genen gespaard blijven. Die strategie kan op termijn worden aangepast, niet alleen voor NIID, maar ook voor andere hersen- en spierziekten die worden veroorzaakt door soortgelijke herhalingsuitbreidingen.
Bronvermelding: Xie, N., Pan, Y., Tong, H. et al. Precise excision of expanded GGC repeats in NOTCH2NLC via CRISPR/Cas9 for treating neuronal intranuclear inclusion disease. Nat Commun 17, 1683 (2026). https://doi.org/10.1038/s41467-026-68385-5
Trefwoorden: CRISPR-genbewerking, neuronaal intranucleair inclusieziekte, herhalingsexpansie-aandoeningen, NOTCH2NLC, neurodegeneratie