Clear Sky Science · nl
Tmem110 reguleert de conformatie van TRPML1 om endolysosomale homeostase te behouden en lekkend mitochondriaal DNA en pathologische verwerking van zelf‑DNA te voorkomen
Waarom weggelopen DNA na letsel ertoe doet
Wanneer we ernstig trauma oplopen, zoals een zware klap tegen het hoofd, stopt de schade niet bij de plek van het letsel. Veel patiënten ontwikkelen een gevaarlijke reactie van het hele lichaam waarbij de longen, lever, nieren en andere organen beginnen uit te vallen. Deze studie toont hoe kleine structuren binnen cellen — lysosomen, mitochondriën en immuunsensoren — met elkaar communiceren om te bepalen of het lichaam het puin stilletjes opruimt of ontspoort in een zelfgerichte immuunaanval. Inzicht in dit verborgen opruimsysteem kan nieuwe mogelijkheden openen om orgaanfalen na trauma te voorkomen en auto-immuun- en ontstekingsziekten te behandelen.
Van hoofdletsel naar crisis van het hele lichaam
Traumatisch hersenletsel (TBI) kan een krachtige ontstekingsstorm veroorzaken die bekendstaat als multiple organ dysfunction syndrome (MODS), maar hoe schade in de hersenen zich verspreidt naar afgelegen organen was onduidelijk. De auteurs richten zich op monocyten en macrofagen, immuuncellen die door bloed en weefsels patrouilleren en fungeren als professionele afvalophalers. Na TBI sterven cellen op ongecontroleerde wijze en komen hele mitochondriën — kleine energiecentrales die hun eigen DNA bevatten — in de circulatie terecht. Dit mitochondriale DNA (mtDNA) lijkt verdacht veel op bacterieel DNA voor het immuunsysteem en kan, als het niet snel wordt verwijderd, sterke antivirale verdedigingsreacties activeren. Normaal nemen cellen deze zwervende mitochondriën op in zure compartimenten die lysosomen heten, waar enzymen het DNA afbreken voordat het in het cytosol lekt. 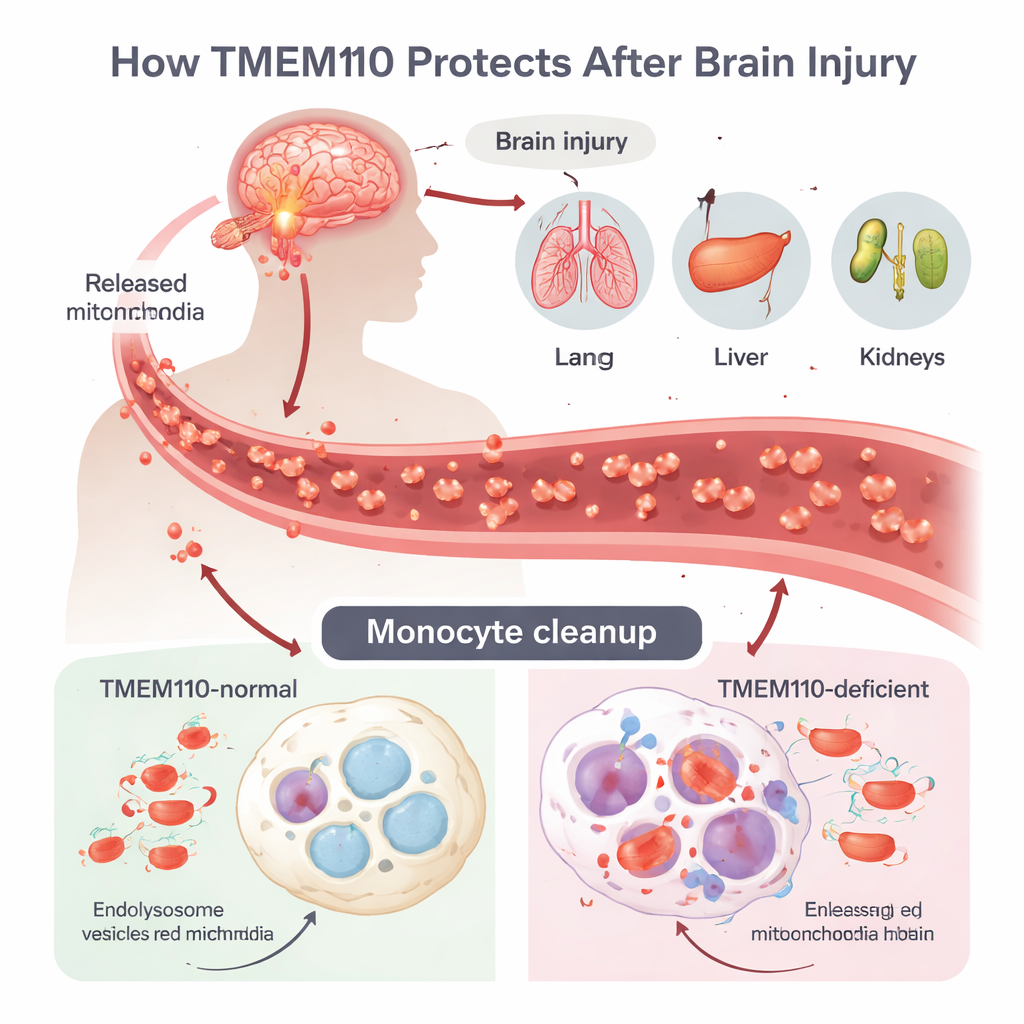
Een poortwachtereiwit dat lysosomen stabiel houdt
Het team identificeerde TMEM110, een eiwit dat het membraan van het endoplasmatisch reticulum (een belangrijk intracellulair membraannetwerk) doorkruist, als een cruciale poortwachter in dit proces. Met genetisch gemodificeerde muizen die TMEM110 alleen misten in monocyten en macrofagen, creëerden ze een gecontroleerd model van hersenletsel. In vergelijking met normale muizen ontwikkelden TMEM110‑deficiënte dieren veel hogere niveaus van type I interferonen — krachtige antivirale signaalmoleculen — in hun bloed en cerebrospinale vloeistof. Hun longen, lever, nieren en lymfeklieren toonden ernstiger schade en hun langetermijnoverleving na TBI was aanzienlijk slechter. Wanneer de onderzoekers de receptor voor type I interferonen blokkeerden, of het mutant beenmerg vervingen door normaal beenmerg, daalden orgaanschade en sterftepercentages, wat aantoont dat excessieve interferon‑signaalgeving door perifere monocyten een belangrijke drijver van MODS is in deze context.
Hoe foutieve ionenhuishouding DNA laat ontsnappen
Bij nadere bestudering van deze immuuncellen vonden de auteurs dat lysosomen zonder TMEM110 chemisch uit balans waren: ze waren minder zuur en overbelast met calcium. Onder deze omstandigheden verloor het enzym DNase II — dat normaal DNA in lysosomen afbreekt — zijn activiteit, werden lysosomale membranen fragiel en ontsnapte mtDNA naar het omliggende cytosol. Laboratoriumexperimenten met menselijke monocyten die gelabelde donormitochondriën insloten bevestigden dat, zonder TMEM110, meer mtDNA in het cytosol lekte en een piek in interferon‑geïnduceerde genen veroorzaakte. De studie toont aan dat TMEM110 werkt door een ander eiwit te regelen, het lysosomale ionkanaal TRPML1. Wanneer TMEM110 aanwezig is, maakt het fysiek contact met TRPML1 en verschuift het kanaal naar een “open” conformatie die kleine calcium‑release hotspots aan het lysosoomoppervlak creëert. Deze gecontroleerde uitstroom van calcium helpt de juiste zuurgraad te behouden, ondersteunt membraanherstel en houdt mtDNA gevangen en afgebroken binnenin. 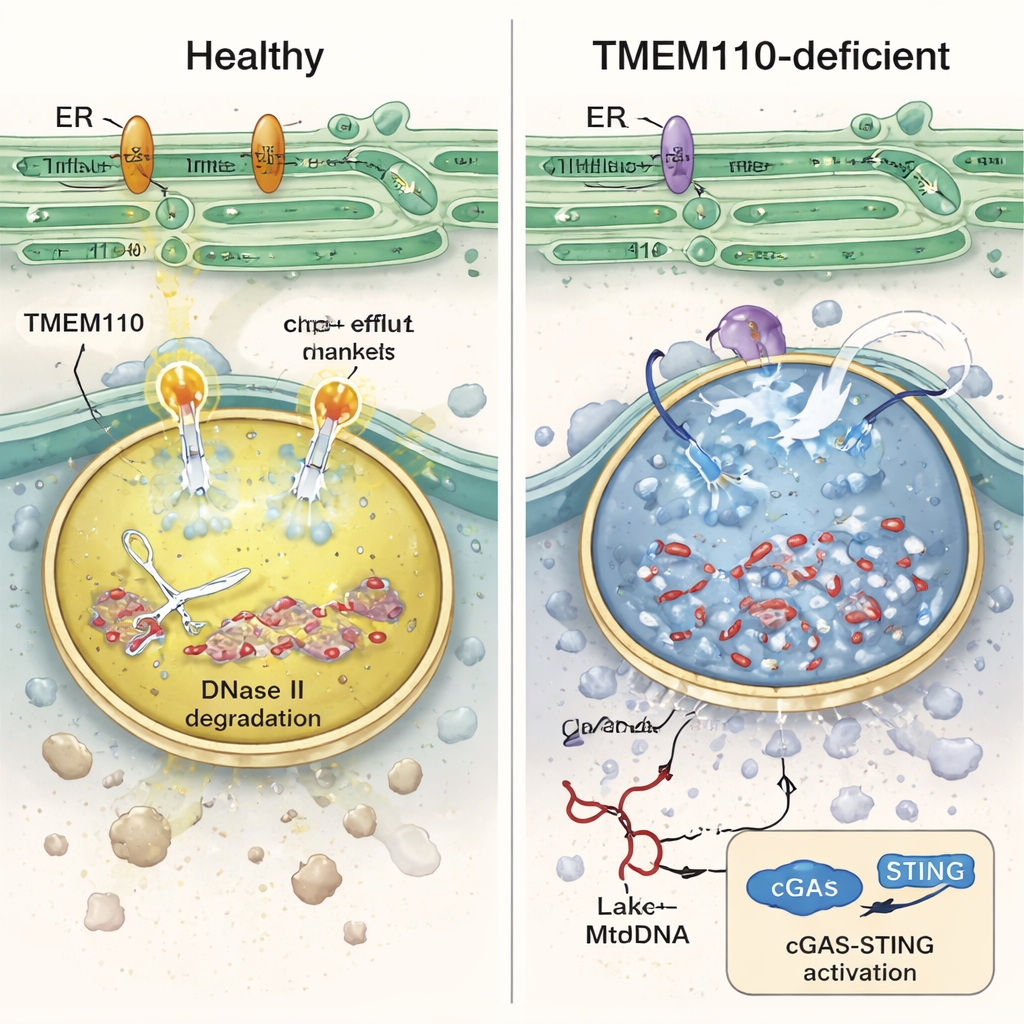
Een terugkoppelingslus met het DNA‑alarmsysteem van de cel
Zodra mtDNA in het cytosol lekt, wordt het herkend door de cGAS–STING‑route, het belangrijkste alarmeringssysteem van de cel voor vreemd DNA. Interessant genoeg bindt TMEM110 ook aan STING in rust en houdt het STING gevangen in het endoplasmatisch reticulum, waardoor onnodig alarm wordt voorkomen. Wanneer cytosolisch DNA zich ophoopt, wordt STING geactiveerd en verslapt het zijn greep op TMEM110. Dat onthult op zijn beurt een ander deel van TMEM110 dat TRPML1 aantrekt en het lysosomale calciumverlies versterkt, waardoor een terugkoppelingslus ontstaat: het waarnemen van zelf‑DNA activeert een mechanisme dat de DNA‑verwijdering verbetert. Ziektegerelateerde mutaties in STING die bij humane autoinflammatoire syndromen voorkomen verstoren deze overdracht, waardoor TMEM110 in een geremde toestand blijft zitten en bijdraagt aan chronische interferonactivatie. In muizen met zo’n STING‑mutatie leidde TBI tot ernstiger orgaanschade en hogere sterfte, maar het afleveren van een klein TMEM110‑fragment aan lysosomen met behulp van een mRNA–lipide‑nanodeeltje therapie herstelde gedeeltelijk de controle van mtDNA en verbeterde de overleving.
Aanwijzingen van patiënten en wegen naar nieuwe behandelingen
De auteurs onderzochten vervolgens een klinische cohorte van 143 mensen met trauma‑gerelateerd hersenletsel en MODS. Patiënten waarvan de monocyten vroeg na het letsel hogere TMEM110‑niveaus vertoonden, herstelden vaker de orgaanfunctie en overleefden. Degenen met lagere TMEM110‑waarden hadden meer circulerend mtDNA en gedecellulariseerde mitochondriën, sterkere interferonresponsen, hogere scores voor orgaanfalen en ruimere auto‑antilichaamprofielen, inclusief antilichamen tegen DNA en kernproteïnen. Deze patronen spiegelden de bevindingen bij muizen nauwkeurig en ondersteunen het idee dat TMEM110‑gestuurde controle van lysosomale stabiliteit en mtDNA‑verwerking een gedeeld mechanisme is bij menselijke ziekte.
Wat dit betekent voor patiënten met zwaar trauma
Deze studie suggereert in gewone bewoordingen dat ons immuunsysteem na een groot letsel voor een delicate keuze staat: stilletjes de vloed van zelf‑DNA afbreken die vrijkomt uit stervende cellen, of het interpreteren als een virale invasie en een allesomvattende aanval beginnen die onze eigen organen kan beschadigen. TMEM110, door een lysosomaal ionkanaal af te stemmen en samen te werken met de DNA‑sensor STING, helpt cellen de veiligere weg te kiezen. Wanneer dit systeem faalt — omdat TMEM110 ontbreekt, STING gemuteerd is of lysosomen worden overweldigd — ontsnapt mtDNA, blijft het alarm aanstaan en volgt multi‑orgaanbeschadiging. Het richten op deze TMEM110–TRPML1–STING‑as, bijvoorbeeld met lysosoomgerichte mRNA‑therapieën, zou een nieuwe manier kunnen bieden om orgaanfalen en auto‑immuunachtige complicaties na ernstig trauma te voorkomen of te behandelen.
Bronvermelding: Feng, Z., Pan, Y., Zhou, J. et al. Tmem110 regulates the conformation of TRPML1 to maintain endolysosomal homeostasis and prevent mitochondrial DNA leakage and pathological self-DNA processing. Nat Commun 17, 1678 (2026). https://doi.org/10.1038/s41467-026-68382-8
Trefwoorden: traumatisch hersenletsel, mitochondriaal DNA, lysosomen, type I interferon, cGAS-STING-route