Clear Sky Science · nl
Cryo-EM-structuur van het menselijke COP1-DET1 ubiquitine-ligasecomplex
Hoe cellen beslissen welke eiwitten ze vernietigen
In elke cel moeten duizenden eiwitten voortdurend op het juiste moment worden opgebouwd, omgevormd of afgebroken. Dit artikel onderzoekt een van de belangrijkste "kwaliteitscontrole"-machines van de cel, een moleculaire versnipperaar die bepaalt wanneer krachtige genregulatoren — gekoppeld aan kanker en ontwikkeling — moeten worden verwijderd. Door zijn driedimensionale structuur tot bijna atomair detail te onthullen, laten de auteurs zien hoe deze machine kan schakelen tussen een inactieve, gestapelde toestand en een actieve, substraatverwerkende vorm — inzicht dat uiteindelijk kan helpen bij het ontwerpen van medicijnen om de activiteit te verhogen of te remmen.
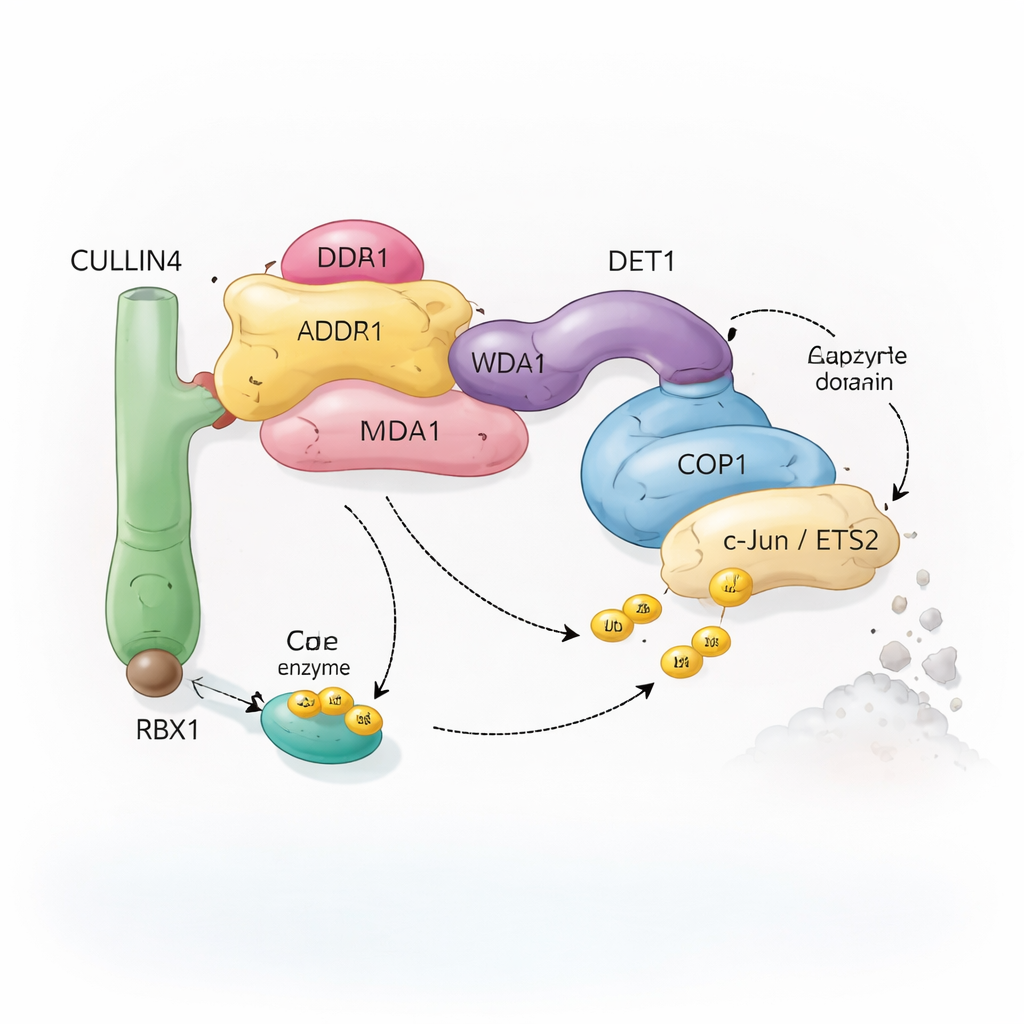
Een moleculair recyclingteam met veel onderdelen
Cellen vertrouwen op een systeem dat ubiquitinatie heet om eiwitten voor recycling te markeren. Kleine ubiquitinemoleculen werken als afneembare vlaggetjes die de cel vertellen of een eiwit moet worden aangepast, verplaatst of afgebroken. Speciale enzymcomplexen, bekend als ubiquitine-ligases, hechten deze vlaggetjes aan geselecteerde doelwitten. Het hier bestudeerde complex draait om COP1, een eiwit dat voorkomt van planten tot mensen en dat helpt belangrijke transcriptiefactoren te taggen—eiwitten die bepalen welke genen aan- of uitgezet worden. COP1 werkt niet alleen: het kan worden ingebouwd in een grotere assemblage die is opgebouwd rond een scaffold-eiwit genaamd CULLIN4, plus verschillende adaptor-eiwitten genaamd DDB1, DDA1 en DET1. Samen vormen deze onderdelen een flexibele "recyclingploeg" die specifieke transcriptiefactoren herkent, zoals c‑Jun en ETS2, van wie er veel betrokken zijn bij celgroei en kanker.
Het complex in 3D vastleggen
Om te begrijpen hoe deze ploeg werkt, gebruikten de onderzoekers single-particle cryo-elektronenmicroscopie, een techniek die met flitsgevroren eiwitten afbeeldt en hun vormen in hoge resolutie reconstrueert. Ze rekreëerden het menselijke COP1–DET1-systeem in gecultiveerde cellen, zuiverden de complexen en visualiseerden verschillende structurele toestanden. Eerst bepaalden ze de structuur van de DDB1–DDA1–DET1-module, die fungeert als centraal knooppunt. DET1 neemt een ongewone, deels flexibele vorm aan in plaats van een stijf schijfje, met een uitstekende "klauw" die partnerenzymen kan grijpen. Vervolgens, door COP1 en een klasse hulpenzymen die E2's worden genoemd toe te voegen, vingen ze grotere assemblages die laten zien hoe alle onderdelen samengaan, waarbij zowel compacte stapels als meer open dimerische (twee-COP1) ordeningen zichtbaar werden.
Een inactieve stapel en een actieve dimer
Een van de meest opvallende bevindingen is een gestapelde, filamentachtige structuur opgebouwd uit herhaalde lagen van het complex. In elke laag verweven acht COP1-moleculen zich via hun coiled-coil-segmenten en vormen zo een ruitvormige ring. Hun substraatherkenningsgebieden, de zogenaamde WD40-domeinen, wijzen allemaal in één richting en zijn deels afgeschermd door naburige lagen. Deze dichte verpakking vertegenwoordigt waarschijnlijk een "uit"-toestand waarin toegang voor doelwitten beperkt is. In tegenstelling daarmee zagen de onderzoekers, wanneer ze complexen onderzochten die samen met COP1-substraten zoals c‑Jun of ETS2 werden geconsumeerd, een andere, dimerische vorm: twee COP1-moleculen naast elkaar, met hun WD40-domeinen naar buiten gericht en beschikbaar om te binden aan de korte "VP"-motieven die in veel transcriptiefactoren voorkomen. Biochemische tests bevestigen dat alleen deze dimerische toestand efficiënt de bouw van lange ubiquitineketens op c‑Jun ondersteunt.
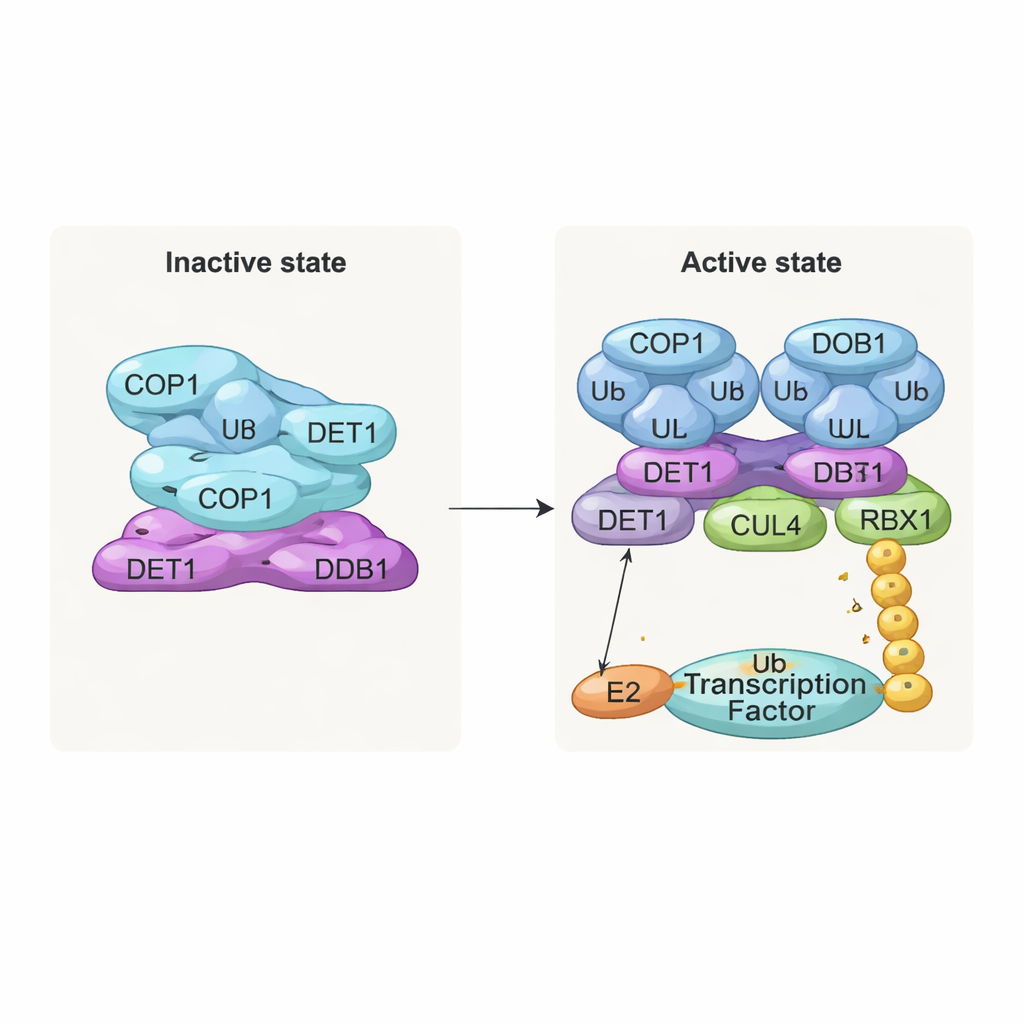
DET1 als flexibele brug en verkeersleider
DET1 komt naar voren als de sleutelorganisator die alle delen van de machine verbindt. Het N-terminus nestelt zich in DDB1 en verankert het complex aan het CULLIN4-scaffold, terwijl het klauwgebied zich om een familie E2-enzymen wikkelt die Ube2e worden genoemd. Gedetailleerde mutatie-experimenten tonen aan dat DET1, niet COP1, direct deze E2's vastgrijpt en ze dicht bij COP1’s catalytische RING-regio positioneert. In deze opstelling lijkt Ube2e te helpen bij het plaatsen van de allereerste ubiquitinetags op het substraat. Een tweede E2-enzym, Ube2d3, wordt vervolgens via de CULLIN4–RBX1-arm gerekruteerd om deze tags uit te breiden tot langere ketens die volledige afbraak signaleren. Met andere woorden, DET1 fungeert als een flexibele brug die één E2 aan COP1 presenteert, terwijl het grotere scaffold een tweede E2 binnenbrengt om het werk af te maken.
Waarom dit belangrijk is voor gezondheid en ziekte
Door deze structurele toestanden en hun activiteiten in kaart te brengen, verklaart de studie hoe dezelfde eiwitset kan wisselen tussen een inactieve, gestapelde vorm en een actieve dimer die transcriptiefactoren voor vernietiging markeert. Deze schakel is vooral belangrijk voor factoren zoals c‑Jun, die de celdeling aandrijven en sterk met kanker verbonden zijn wanneer ze verkeerd gereguleerd raken. Begrijpen hoe COP1 en DET1 samenwerken—hoe DET1’s klauw specifieke E2-enzymen selecteert, hoe COP1’s WD40-oppervlak VP-bevattende substraten herkent, en hoe de actieve dimer zich vormt—biedt een blauwdruk voor toekomstig onderzoek. Op de lange termijn zouden geneesmiddelen die de inactieve stapel stabiliseren of de actieve dimer bevoordelen onderzoekers nieuwe manieren kunnen geven om genregulatiepaden te beïnvloeden bij kanker en andere aandoeningen waarin eiwitafbraak ontspoort.
Bronvermelding: Wang, S., Teng, F., Stjepanovic, G. et al. Cryo-EM structure of the human COP1-DET1 ubiquitin ligase complex. Nat Commun 17, 543 (2026). https://doi.org/10.1038/s41467-026-68375-7
Trefwoorden: ubiquitine-ligase, COP1, eiwitafbraak, cryo-EM-structuur, c-Jun