Clear Sky Science · nl
INCENP en CDCA8 voorspellen respons en uitkomsten van neoadjuvante chemotherapie bij plaveiselcelcarcinoom van de slokdarm
Waarom dit onderzoek belangrijk is voor kankerpatiënten
Veel mensen met kanker van de slokdarm, borst of longen krijgen intensieve chemotherapie vóór een operatie om tumoren te verkleinen. Slechts ongeveer de helft van deze patiënten profiteert daar werkelijk van; voor de rest veroorzaken de middelen bijwerkingen zonder de kanker te stoppen. Deze studie stelt een eenvoudige maar cruciale vraag: kunnen we van tevoren voorspellen wie op chemotherapie zal reageren, en kunnen we de behandeling effectiever maken voor degenen die nu niet reageren?
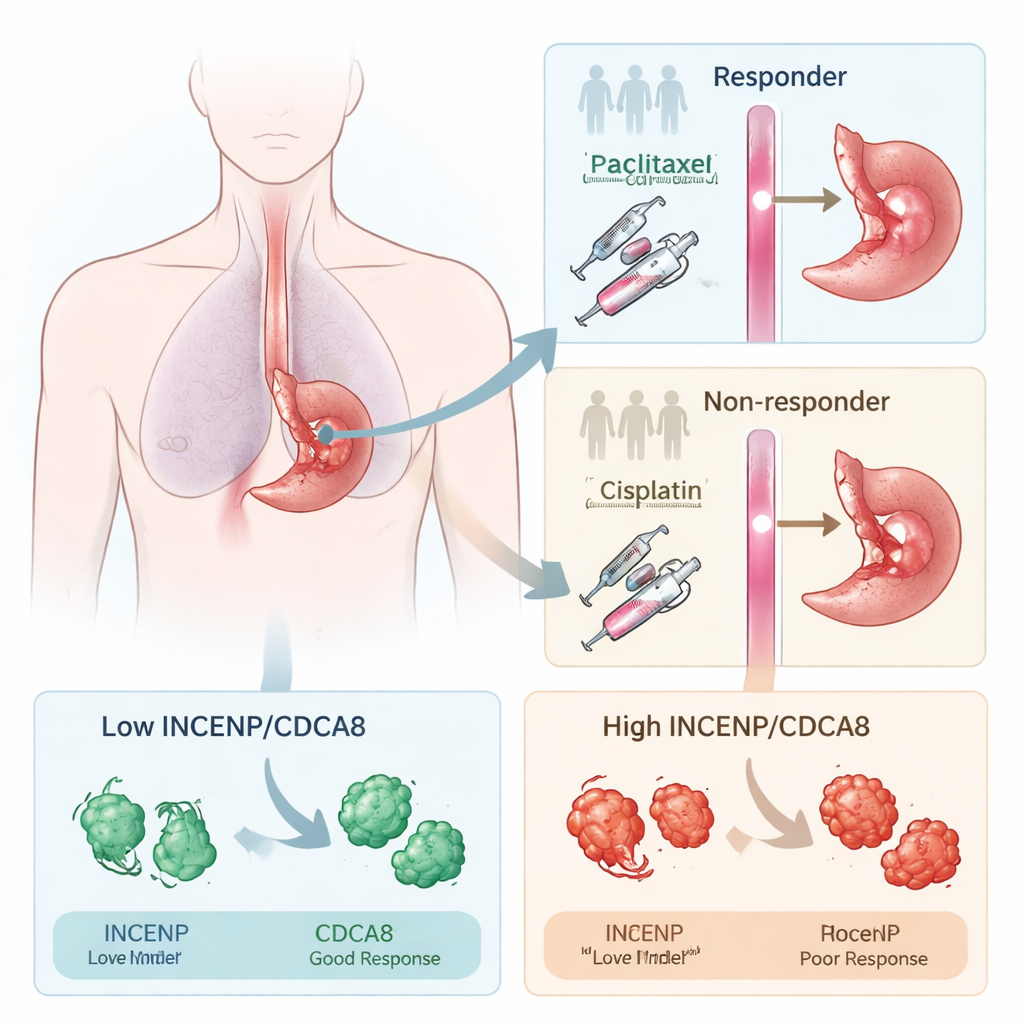
Wie reageert op de behandeling zichtbaar maken
De onderzoekers richtten zich op een standaard regime vóór operatie dat paclitaxel en cisplatine combineert, veelgebruikt bij verschillende kankersoorten. Eerst vergeleken ze bij patiënten met plaveiselcelcarcinoom van de slokdarm tumormonsters van mensen bij wie de kanker sterk krimpte na deze therapie (responders) met monsters van degenen wiens tumoren nauwelijks veranderden (non-responders). Door te onderzoeken welke genen hoger of lager werden afgelezen, vonden ze dat veel verschillen te maken hadden met hoe cellen delen — een proces dat chemotherapie juist wil verstoren. Twee eiwitten die helpen bij het scheiden van chromosomen tijdens celdeling, INCENP en CDCA8, vielen herhaaldelijk op omdat ze veel sterker aanwezig waren in tumoren die resistent waren tegen de behandeling.
Twee eiwitten die waarschuwen voor mogelijke resistentie
Om te testen of INCENP en CDCA8 slechts bijfiguren waren of actieve veroorzakers van resistentie, veranderde het team hun hoeveelheden in slokdarmkankercellen die in het laboratorium werden gekweekt. Wanneer ze één van beide eiwitten verlaagden, werden de kankercellen veel gevoeliger voor paclitaxel en cisplatine: ze vormden minder kolonies en er waren aanzienlijke lagere medicijndoses nodig om ze te doden. Wanneer ze de cellen dwongen extra INCENP of CDCA8 te produceren, gebeurde het omgekeerde: de middelen werden minder effectief. In muizen met geïmplanteerde menselijke slokdarmtumoren leidde het onderdrukken van deze eiwitten tot sterkere tumorkrimp door chemotherapie. Patiënten van wie de tumoren vóór behandeling hoge niveaus INCENP en CDCA8 bevatten, hadden ook een grotere kans op ziekteprogressie en kortere overleving, wat hun waarde als waarschuwingssignaal versterkt.
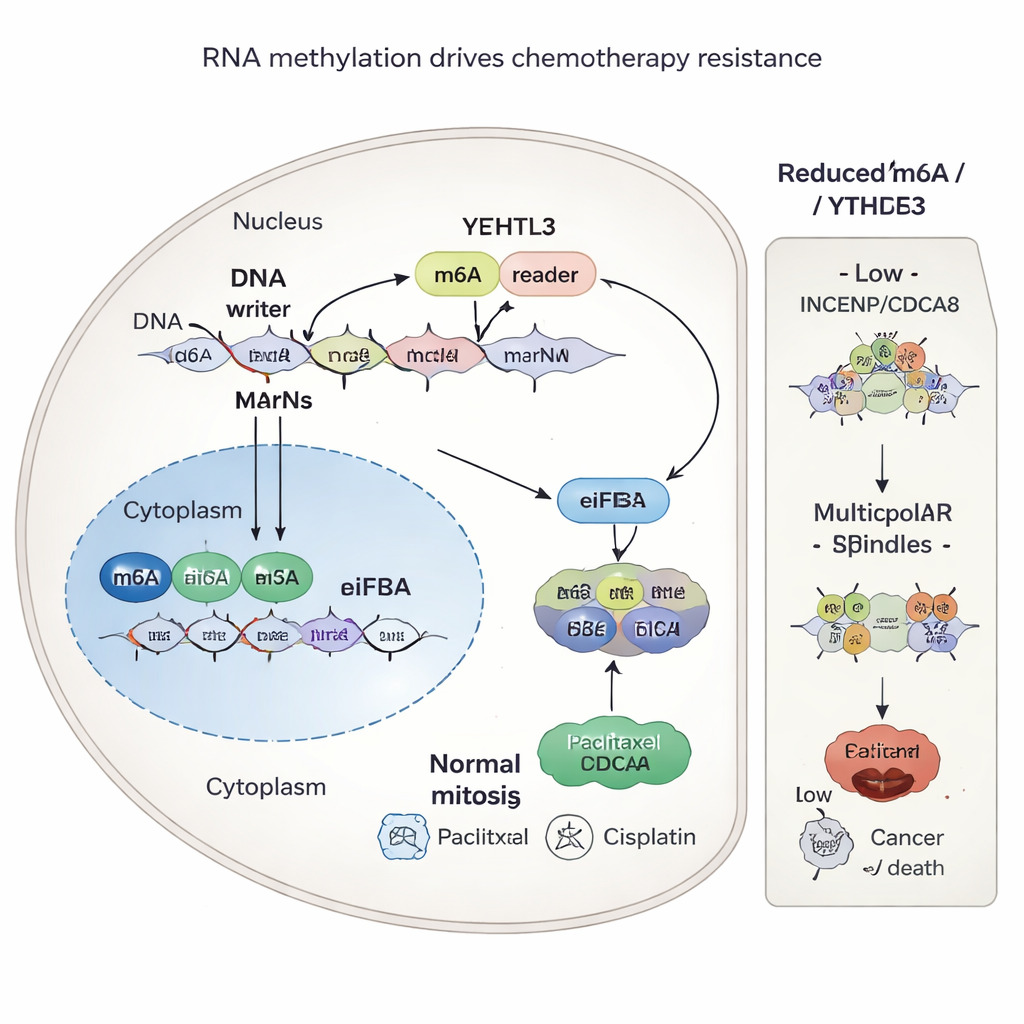
Een chemische markering op RNA die resistentie aanwakkert
De studie vroeg zich vervolgens af waarom INCENP en CDCA8 zo overvloedig aanwezig zijn in resistente tumoren. Het antwoord wees naar een subtiel chemisch merkje op RNA, m6A genoemd, dat fungeert als een fijninstelling voor hoe efficiënt genetische boodschappen in eiwitten worden omgezet. Een enzym genaamd METTL3 voegt deze m6A-markeringen toe op specifieke plaatsen in de RNA-blauwdrukken voor INCENP en CDCA8. Een ander eiwit, YTHDF3, herkent deze markeringen en helpt het eiwitproductiesysteem van de cel te rekruteren, waardoor de productie van de twee eiwitten toeneemt. Wanneer de wetenschappers METTL3 of YTHDF3 terugbrachten, of YTHDF3 blokkeerden met een klein molecuul genaamd Ebselen, gingen de m6A-markeringen verloren of werden ze genegeerd, daalden de eiwitniveaus van INCENP en CDCA8 en werden kankercellen gevoeliger voor chemotherapie.
Celdeling verstoren om chemotherapie te helpen
INCENP en CDCA8 zijn onderdeel van een groter complex, het chromosomal passenger complex, dat ervoor zorgt dat chromosomen gelijk verdeeld worden over dochtercellen. In resistente cellen helpen hoge niveaus van deze eiwitten om tijdens celdeling nette, bipolaire spoelen te behouden, waardoor de kanker de schade door paclitaxel en cisplatine kan overleven. Wanneer INCENP en CDCA8 onderdrukt zijn, vormen cellen vaak defecte, multipolaire spoelen. Deze chaos bij de chromosoomverdeling duwt kankercellen richting celdood en versterkt het dodelijke effect van chemotherapie. Cruciaal is dat het beschermende vermogen van INCENP en CDCA8 afhing van specifieke m6A-sites in hun RNA; het muteren van deze sites maakte de resistentie ongedaan.
Niet beperkt tot één kankertype
Aangezien paclitaxel plus cisplatine ook wordt gebruikt bij long- en borstkanker, onderzochten de onderzoekers biopten van patiënten met deze tumoren. In alle drie de kankersoorten waren mensen van wie de tumoren vóór therapie lage niveaus INCENP, CDCA8 en YTHDF3 hadden, veel waarschijnlijker om goed op de behandeling te reageren. Statistische analyses lieten zien dat het combineren van deze drie markers bijzonder veel kracht gaf om waarschijnlijke responders van non-responders te onderscheiden, wat wijst op een praktisch testpaneel dat bij meerdere kankers toepasbaar zou kunnen zijn.
Wat dit betekent voor patiënten en artsen
In eenvoudige bewoordingen identificeert dit werk een moleculair "vingerafdruk" die helpt verklaren waarom sommige tumoren krachtige chemotherapie negeren. Hoge niveaus van INCENP en CDCA8, aangedreven door een m6A-gebaseerd regelsysteem met METTL3 en YTHDF3, houden kankercellen georganiseerd delend zelfs onder medicijnaanval. Het meten van deze eiwitten in een biopsie kan artsen helpen voorspellen of paclitaxel plus cisplatine waarschijnlijk een patiënt zal helpen, en zo anderen besparen van een ineffectieve behandeling. Tegelijkertijd zouden middelen die deze route blokkeren gecombineerd kunnen worden met standaardchemotherapie om resistente tumoren door middel van dodelijke delingsfouten te laten instorten, wat mogelijk de overleving verbetert voor mensen met meerdere belangrijke kankers.
Bronvermelding: Wang, X., Wang, T., Wang, K. et al. INCENP and CDCA8 predict neoadjuvant chemotherapy response and outcomes in esophageal squamous cell carcinoma. Nat Commun 17, 1672 (2026). https://doi.org/10.1038/s41467-026-68371-x
Trefwoorden: neoadjuvante chemotherapie, plaveiselcelcarcinoom van de slokdarm, chemotherapie-resistentie, INCENP- en CDCA8-biomarkers, RNA m6A-methylering