Clear Sky Science · nl
K48-ubiquitine-afhankelijke proteasen hakken post-ER-eiwitten in stukken
Hoe cellen beslissen welke eiwitten ze vernietigen
Onze cellen verwijderen voortdurend versleten of beschadigde eiwitten, met name die ingebed zitten in membranen en fungeren als poorten en sensoren. Dit artikel laat zien dat cellen ubiquitine, een klein label, niet alleen als een algemeen “afval”-sticker gebruiken, maar als een code die membraaneiwitten precies vertelt hoe ze worden afgebroken. Inzicht in deze code helpt verklaren hoe cellen gezond blijven en kan toekomstige therapieën sturen die gericht ziekteveroorzakende eiwitten vernietigen.
Een cellulair streepjescode voor eiwitverwijdering
Cellen versieren ongewenste eiwitten met ketens van een klein eiwit genaamd ubiquitine. Deze ketens kunnen op verschillende manieren aan elkaar gekoppeld zijn, vergelijkbaar met kralen die door verschillende gaatjes gestringd zijn, en elk patroon kan een andere uitkomst signaleren. De auteurs concentreerden zich op membraaneiwitten die al het endoplasmatisch reticulum (ER) hebben verlaten en door compartimenten zoals het Golgi en endosomen reizen. Ze onderzochten of twee veelvoorkomende ketentypes, genoemd K48-gebonden en K63-gebonden ubiquitine, werkelijk uitwisselbare labels zijn of dat ze cargo naar verschillende vernietigingsroutes sturen.
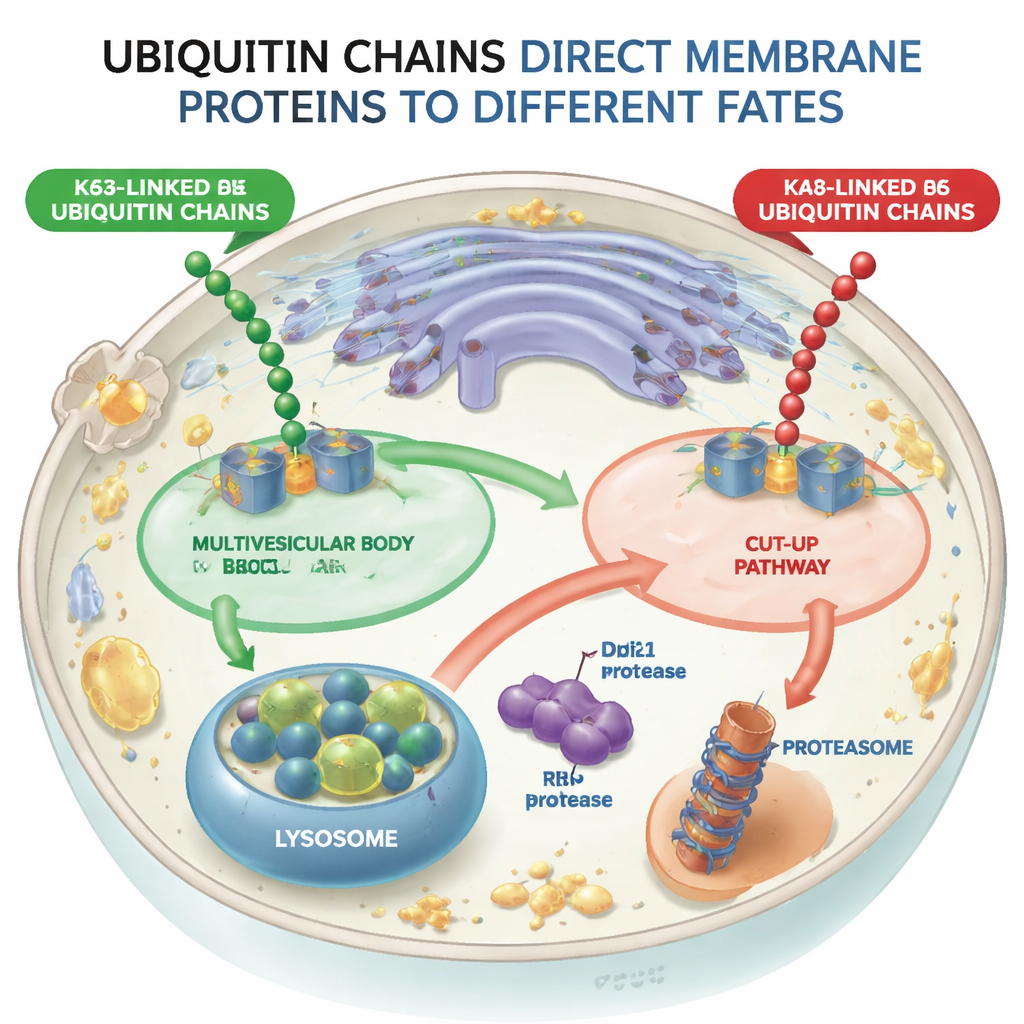
Twee uiteenlopende paden voor gelabelde eiwitten
Met gistcellen als model creëerden de onderzoekers moleculaire machines (ubiquitine-ligases) die ofwel K48-gebonden ofwel K63-gebonden ketens aan hetzelfde test-membraaneiwit, een sorteereceptor genaamd Vps10, konden koppelen. Wanneer Vps10 K63-gebonden ketens kreeg, werd het naar interne blaasjes in endosomen gestuurd — structuren bekend als multivesiculaire lichamen — die uiteindelijk versmelten met lysosomen, de verteringscompartimenten van de cel. In tegenstelling daarmee volgde Vps10 met K48-gebonden ketens niet deze multivesiculaire route. In plaats daarvan werd het op een geheel andere manier afgebroken, wat aantoont dat de cel onderscheid maakt tussen deze twee ketentypen en dat het multivesiculaire pad effectief K48-geëtiketteerde cargo afstoot.
Een “cut-up”-pad dat eiwitten in tweeën snijdt
Het team ontdekte dat K48-gebonden ketens een eiwit-scheurpad activeren dat ze CUT-UP noemen, een afkorting voor Cleavage of Ubiquitinated Targets by Ubiquitin-dependent Proteases. In plaats van het volledige eiwit in één keer uit het membraan te trekken, hakt CUT-UP het in stukken die vervolgens worden afgemaakt door bestaande cellulaire afbraaksystemen. Eén sleutelenzym, Ddi1, drijft in het cytosol en knipt het deel van het membraaneiwit af dat naar het cytoplasma gericht is. Dat fragment wordt vervolgens verteerd door het proteasoom, de belangrijkste eiwitversnipperaar van de cel. Tegelijkertijd zit een ander enzym, Rbd2, in het membraan zelf en snijdt het het deel van het eiwit dat naar de binnenkant van het compartiment is gericht, waardoor het vrijkomt in de ruimte die uiteindelijk naar het lysosoom leidt. Het blokkeren van Ddi1, Rbd2, het proteasoom en lysosomale enzymen samen was nodig om K48-gelabelde Vps10 volledig te beschermen tegen afbraak, wat bevestigt dat al deze componenten samenwerken in het CUT-UP-pad.
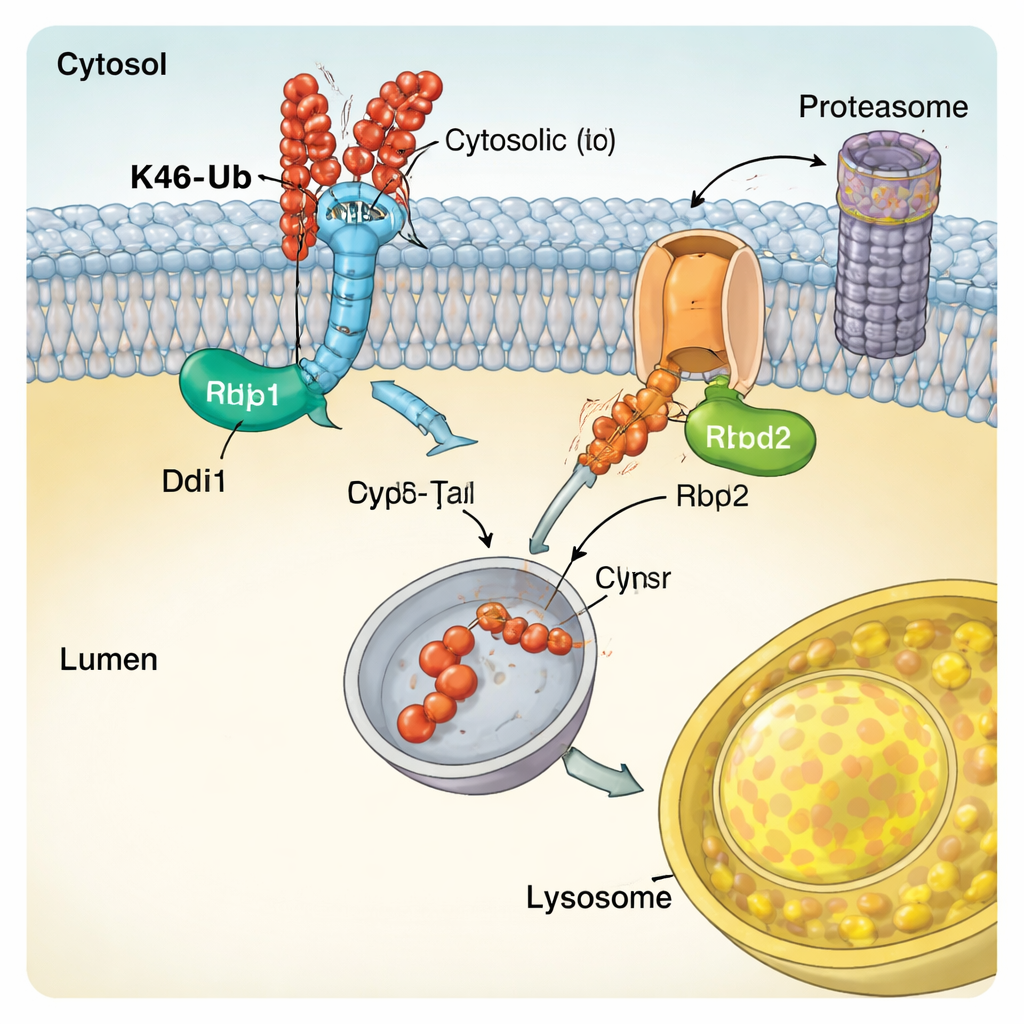
Gespecialiseerde enzymen die de ubiquitinecode lezen
Om te begrijpen hoe CUT-UP zijn doelwitten herkent, onderzochten de auteurs de moleculaire eigenschappen van Ddi1. Ze toonden aan dat Ddi1’s centrale catalytische kern niet alleen eiwitten knipt maar ook ubiquitine direct kan binden, en dat zijn activiteit wordt bijgesteld door extra regio’s die zich vasthechten aan ubiquitineketens. Ddi1 bleek een bijzondere afhankelijkheid van K48-gebonden ketens te hebben, wat overeenkomt met zijn rol in CUT-UP. Rbd2 daarentegen is een rhomboïde protease dat het membraan overspant. De studie vond dat het actieve centrum van Rbd2 essentieel is voor het knippen van de lumen-georiënteerde delen van Vps10 en dat het enzym door meerdere secretorische compartimenten reist, waardoor het op meerdere cellulaire locaties kan handelen. Vergelijkbare enzymen bestaan in menselijke cellen en zijn in verband gebracht met aandoeningen variërend van neurodegeneratie tot kanker, wat suggereert dat CUT-UP-achtige mechanismen waarschijnlijk breed van belang zijn.
Waarom dit belangrijk is voor gezondheid en therapie
Door aan te tonen dat verschillende ubiquitineketentypes hetzelfde membraaneiwit naar scherp verschillende loten sturen — ofwel multivesiculair-lichamen-sortering ofwel CUT-UP-gemedieerde versnippering — levert dit werk sterk bewijs dat cellen een echte “ubiquitinecode” gebruiken om eiwitverwijdering fijn af te stemmen. De ontdekking van CUT-UP verduidelijkt hoe hardnekkige membraaneiwitten stukje bij beetje ontmanteld kunnen worden en belicht Ddi1 en Rbd2 als sleutelspelers die deze code lezen en afdwingen. Voor niet-specialisten is de kernboodschap dat cellen eiwitten niet simpelweg als vuilnis markeren; ze specificeren hoe dat vuilnis wordt afgevoerd. Nu medicijnontwikkelaars instrumenten ontwerpen die schadelijke eiwitten met ubiquitine labelen om ze te verwijderen, zal begrip van paden zoals CUT-UP essentieel zijn om te voorspellen welke fragmenten gevormd worden en hoe dat het celgedrag kan beïnvloeden.
Bronvermelding: Minard, A.Y., Winistorfer, S., Yu, L. et al. K48-ubiquitin-dependent proteases cut-up post-ER proteins. Nat Commun 17, 1669 (2026). https://doi.org/10.1038/s41467-026-68367-7
Trefwoorden: ubiquitinecode, eiwitafbraak, membraaneiwitten, proteasoom, lysosoom