Clear Sky Science · nl
Het verlies van Fsr-quorum sensing bevordert biofilmvorming en verslechtert de uitkomsten bij enterokokke infectieuze endocarditis
Stille saboteurs op de hartkleppen
Infectieuze endocarditis is een levensbedreigende infectie van de hartkleppen en komt wereldwijd steeds vaker voor. Deze studie richt zich op een belangrijke dader, de darmbacterie Enterococcus faecalis, en onderzoekt waarom sommige infecties bijzonder moeilijk te behandelen zijn. Door te achterhalen hoe deze bacteriën met elkaar ‘praten’ en beschermende biofilms op hartkleppen vormen, laten de onderzoekers zien waarom bepaalde stammen ernstigere ziekte veroorzaken en tegen antibiotica bestand zijn, en waarom één bacterieel communicatiesysteem, genaamd Fsr, verrassend genoeg als een rem in plaats van een versneller van schade fungeert.
Hoe bacteriën forten in het hart bouwen
Hartkleppen weerstaan normaal gesproken een van de snelste bloedstromingen in het lichaam, maar als het klepoppervlak beschadigd is, kunnen bloedplaatjes en stollingsproteïnen een klein stolsel of vegetatie vormen. Dit stolsel wordt een landingsplaats voor bacteriën in de bloedbaan. Eenmaal vastgehecht vermenigvuldigen de bacteriën zich en weven ze zich in een biofilm — een slijmerige, gestructureerde gemeenschap die hen beschermt tegen immuuncellen en geneesmiddelen. Het team gebruikte microfluïdica-apparaten om bloedstroom in het lab na te bootsen, en een rattenmodel om endocarditis in levende dieren te recreëren, waardoor ze konden observeren hoe E. faecalis zich aanpast terwijl de infectie vordert van enkele verspreide cellen naar dikke, rijpe biofilms. 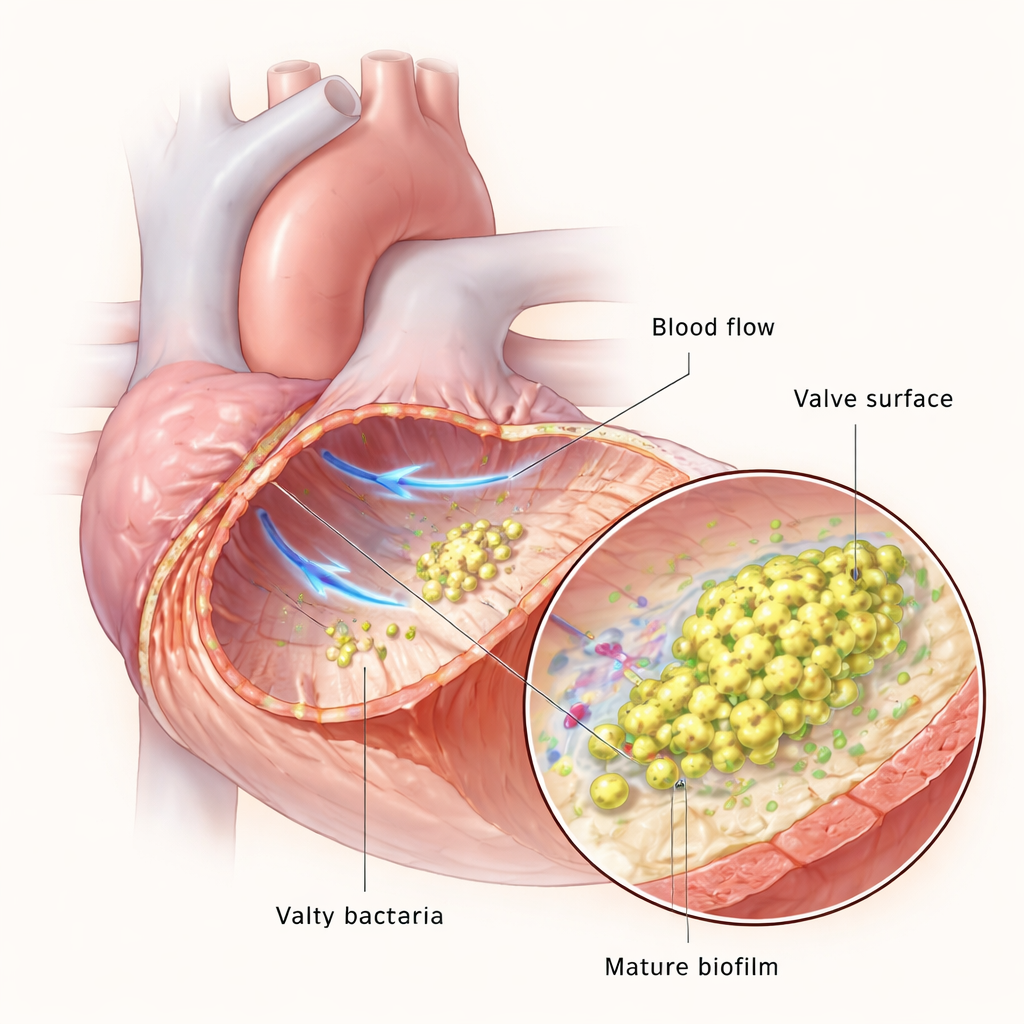
Wanneer snelle bloedstroom de bacteriële “klets” uitschakelt
Bacteriën coördineren hun gedrag vaak via quorum sensing, een chemisch ‘stemproces’ dat genen aan- of uitzet zodra er genoeg cellen aanwezig zijn. Fsr is het quorum sensing-systeem dat E. faecalis gebruikt. Verrassend genoeg ontdekten de onderzoekers dat sterke, stromende vloeistof de signaalmoleculen die nodig zijn om Fsr te activeren, daadwerkelijk wegspoelt. In een vroege infectiefase, wanneer bacteriën op het blootgestelde oppervlak van de vegetatie zitten en de volle kracht van de bloedstroom voelen, is Fsr grotendeels stil. Pas later, wanneer microkolonies groter worden en dieper in de vegetatie begraven raken — afgeschermd van de stroming — activeert Fsr. Dit betekent dat in het echte hart quorum sensing niet alleen wordt bepaald door het aantal bacteriën, maar ook door waar ze zich binnen de driedimensionale structuur bevinden.
Het uitschakelen van Fsr laat biofilms overgroeien
Om te testen wat Fsr precies doet voor de infectie, vergeleek het team normale bacteriën met mutanten die het volledige Fsr-systeem misten. In het begin koloniseerden beide versies de kleppen even goed. Maar na drie dagen hadden dieren geïnfecteerd met Fsr-deficiente stammen grotere vegetaties en veel meer bacteriën erin gepakt. Gedetailleerde beeldvorming toonde dat hun biofilms een groter deel van het stolsel bedekten en dat hun microkolonies groter waren. Het verlies van Fsr schakelde ook twee belangrijke uitgescheiden enzymen uit, GelE en SprE, die normaal helpen de biofilm te vormen en mogelijk overgroei beperken. Dieren geïnfecteerd met mutanten die alleen deze enzymen misten ontwikkelden ook omvangrijkere biofilms, zij het niet zo extreem als bij Fsr-null stammen, wat suggereert dat ook andere door Fsr gecontroleerde factoren een rol spelen. 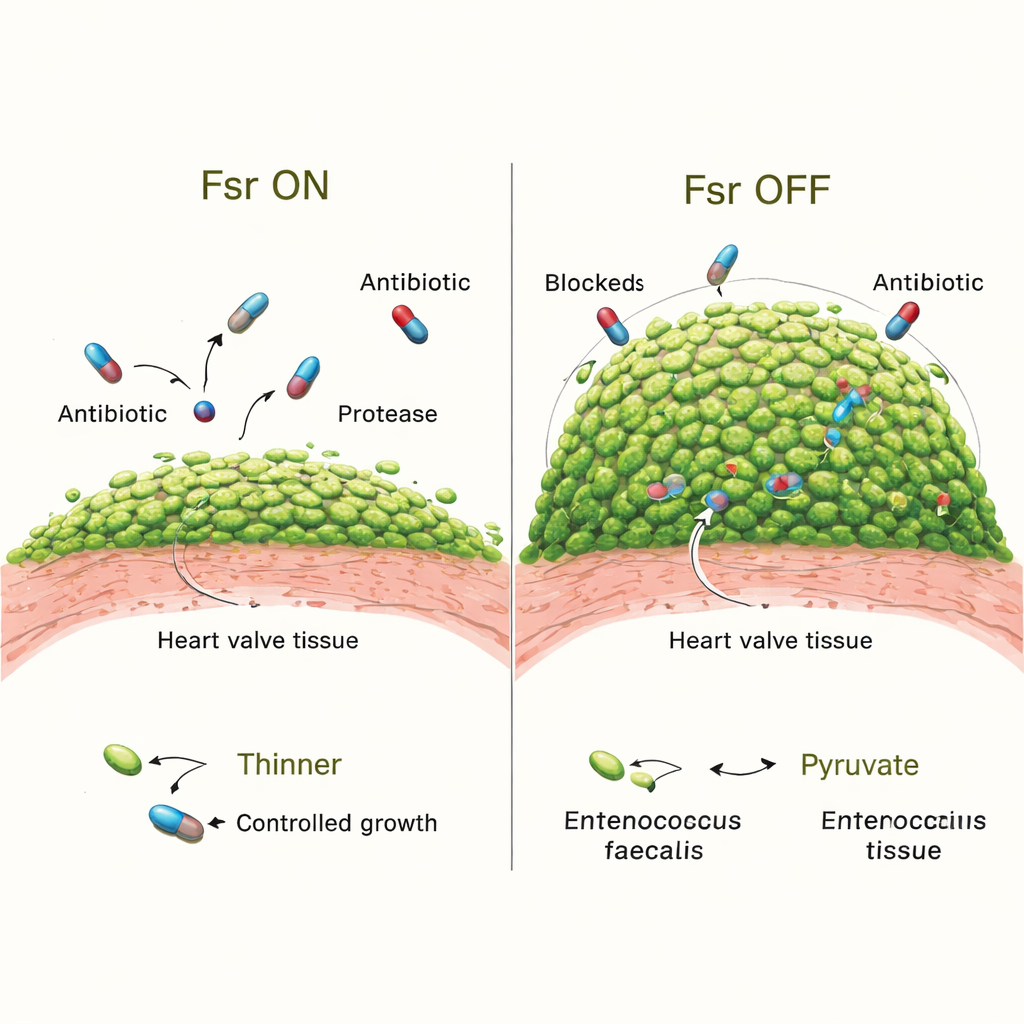
Metabole herprogrammering en een sterkere grip op antibiotica
Genexpressieprofielen van bacteriën binnen geïnfecteerde kleppen toonden aan dat Fsr meer regelt dan slechts een paar enzymen. Zonder Fsr veranderde de activiteit van honderden genen, vooral die betrokken bij suikeropname en energieproductie. Een genpaar, lrgA en lrgB, stak eruit: deze werden sterk aangezet in Fsr-deficiente bacteriën en hielpen de cellen beter gebruik te maken van pyruvaat, een klein energiehoudend molecuul dat in bloed aanwezig is. Toen de onderzoekers lrgAB samen met Fsr verwijderden, verdween de overmatige biofilmgroei, wat wijst op een sleutelrol voor deze metabole route bij het aandrijven van de overgroeide infectie. Opmerkelijk was dat Fsr-deficiente biofilms ook lastiger te behandelen waren. In ratten die het antibioticum gentamicine kregen, slonken infecties met normale bacteriën en verbeterden het aantal bloedplaatjes — een graadmeter voor ziektelast. Daarentegen reageerden Fsr-deficiente infecties nauwelijks, ook al waren de bacteriën in standaard laboratoriumtests niet resistenter tegen het middel.
Een mensspecifieke wending in ontsteking
De studie ontdekte ook een mogelijke manier waarop deze bacteriën bij mensen ontsteking kunnen aanwakkeren. Het enzym GelE kan de menselijke voorloper van het immuunsignaal IL-1β in een actieve vorm knippen die ontstekingsreacties opwekt. Intrigerend genoeg knipte GelE ratten-IL-1β anders, waarbij het eiwit werd afgebroken in plaats van geactiveerd, en de precieze ‘activerings’-knip ontbrak in rat- en muisweefsels. Dit soort soortspecifieke effect suggereert dat bij mensen GelE de ontsteking precies bij de rand van de biofilm kan richten, wat mogelijk weefselschade tijdens endocarditis verergert.
Van laboratorium naar kliniek: waarom het verlies van Fsr telt voor patiënten
Om na te gaan of deze experimentele bevindingen ook in de praktijk relevant zijn, analyseerden de onderzoekers E. faecalis-isolaten van 81 patiënten met infectieuze endocarditis in Zwitserland en de Verenigde Staten. Bijna de helft van de stammen misten van nature het Fsr-systeem. Patiënten geïnfecteerd met deze Fsr-negatieve stammen hadden langduriger bacteriëmie — meer dagen met detecteerbare bacteriën in het bloed — en hadden een grotere kans op een hoge-ernstcategorie die intensieve zorg, langdurige ziekenhuisopnames, ingrijpende hartprocedures of overlijden omvatte. Andere virulentiegenen konden dit patroon niet verklaren, wat direct wijst op verlies van Fsr als een belangrijke indicator van agressievere ziekte.
Waarom dit belangrijk is voor toekomstige behandelingen
Gezamenlijk zetten deze bevindingen een simpele opvatting op zijn kop: dat het blokkeren van bacteriële communicatie altijd infecties zal verzwakken. Bij E. faecalis-endocarditis remt het Fsr-systeem juist de uitbreiding van de biofilm en maakt het bacteriën gevoeliger voor antibiotica. Wanneer Fsr ontbreekt, vormen bacteriën dichtere biofilms, benutten ze bloednutriënten efficiënter en drijven ze hardnekkige, langdurige infecties aan. Voor patiënten betekent dit dat stammen zonder Fsr kunnen voorspellen dat de ziekte moeilijker te behandelen is, en dat therapieën die zonder onderscheid quorum sensing uitschakelen in deze context averechts kunnen werken. In plaats daarvan kunnen gerichte aanpakken van metabole routes zoals het gebruik van pyruvaat, of het monitoren van Fsr- en GelE-status als prognostische markers, betere manieren bieden om deze gevaarlijke hartinfecties te beheersen.
Bronvermelding: Antypas, H., Schmidtchen, V., Staiger, W.I. et al. Loss of Fsr quorum sensing promotes biofilm formation and worsens outcomes in enterococcal infective endocarditis. Nat Commun 17, 1668 (2026). https://doi.org/10.1038/s41467-026-68366-8
Trefwoorden: infectieuze endocarditis, bacteriële biofilms, quorum sensing, Enterococcus faecalis, antibiotische tolerantie