Clear Sky Science · nl
Gemanipuleerde VPg-saRNA bereikt kap-onafhankelijke, laag-immunogene en precieze codering van therapeutische eiwitten in vivo
De regels herschrijven voor RNA-geneesmiddelen
Vaccins gebaseerd op boodschapper-RNA (mRNA) droegen sterk bij aan het keren van de COVID-19-pandemie, maar vergelijkbare moleculen gebruiken om ontbrekende eiwitten bij chronische ziekten te vervangen of aan te vullen is veel moeilijker. Het lichaam breekt vreemd RNA vaak snel af en roept sterke immuunreacties op, en veel bestaande ontwerpen van zelf-amplificerend RNA (saRNA) maken fouten tijdens het kopiëren. Deze studie beschrijft een nieuw type saRNA—gebouwd uit onderdelen van menselijk norovirus—dat is ontworpen om langdurig te zijn, minder ontstekingsreacties te veroorzaken en uitzonderlijk nauwkeurig te zijn, waardoor de weg wordt geopend naar meer precieze en duurzame RNA-geneesmiddelen.
Een slimmer zelf-kopierend RNA
Conventionele mRNA-geneesmiddelen dragen één "recept" voor een eiwit en worden eenmaal door de cel afgelezen voordat ze worden afgebroken. Zelf-amplificerend RNA bevat extra virale machinerie die het mogelijk maakt dat het RNA zichzelf binnen cellen kopieert, waardoor de opbrengst uit een kleine dosis sterk toeneemt. De best bestudeerde saRNA-systemen komen van alphavirussen, maar die zijn omvangrijk, roepen sterke antivirale afweer op en kopiëren hun sequenties met relatief lage nauwkeurigheid. De auteurs keerden zich in plaats daarvan tot menselijk norovirus, een veelvoorkomende veroorzaker van buikgriep. Ze isoleerden een compact gedeelte van het norovirus-genoom en bouwden dit om als drager voor therapeutische genen. Centraal staat VPg, een klein viraal eiwit dat chemisch aan het voorste uiteinde van het RNA is verbonden. VPg vervangt de gebruikelijke "cap"-structuur op menselijke mRNAs en stelt het RNA in staat te worden vertaald door een andere set cel-factoren die minder gevoelig zijn voor bepaalde stresssignalen. 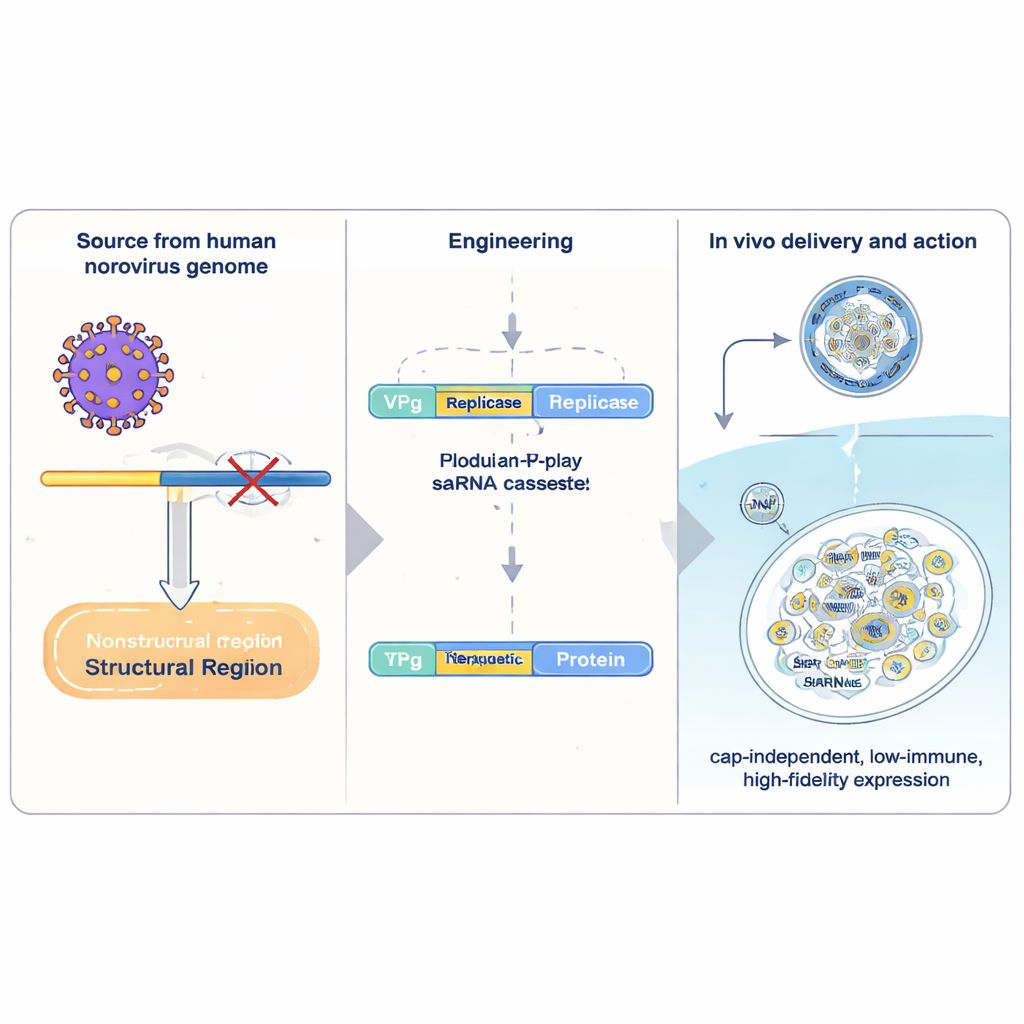
Hoge nauwkeurigheid zonder immuunopwinding
Voor eiwittherapieën is nauwkeurigheid van groot belang: zelfs kleine kopieerfouten kunnen het gedrag van een geneesmiddel veranderen of toxische bijproducten creëren. Het team toonde aan dat wanneer norovirus-VPg bindt aan het RNA-kopiërende enzym van het virus (een polymerase), het de snelheid waarmee verkeerde bouwstenen worden ingebouwd vertraagt, waardoor de foutfrequentie scherp daalt. Ze identificeerden specifieke aminozuren in VPg die contact maken met een sleutelcontrolegebied van de polymerase en toonden aan dat het verstoren van dit interface de kopieernauwkeurigheid vermindert. Tegelijkertijd creëren klassieke saRNA-ontwerpen grote hoeveelheden dubbelstrengs RNA, een moleculaire alarmbel die antivirale verdedigingen activeert en de eiwitproductie stillegt. Door de polymerase te herontwerpen zodat deze een specifieke VPg-gebonden startvorm bevoordeelt en door het genoom zo te herschikken dat alleen de therapeutische streng efficiënt wordt geproduceerd, verminderden de auteurs de vorming van dubbelstrengs RNA sterk. Ze stemden daarnaast een staartregio van het RNA af zodat VPg op de juiste plaats bevestigt, waardoor korte, onbedoelde fragmenten die tot stray peptiden zouden kunnen leiden, worden voorkomen.
Werkt waar standaard mRNA faalt
Het nieuwe VPg-gebaseerde saRNA werd vervolgens getest in veeleisende ziektetoepassingen waar gewone gecapte mRNA's moeite hebben. Bij kanker-geassocieerde cachexie—een wasting-syndroom waarbij spieren en vet verdwijnen—zijn belangrijke translatiefactoren die de standaard mRNA-cap herkennen uitgeschakeld, waardoor cap-afhankelijke mRNAs inefficiënt zijn. Omdat VPg een alternatieve toegang tot de translatiemachinerie van de cel gebruikt, bleef het de productie van het honger- en metabolismehormoon ghreline stimuleren in een muismodel van alvleesklierkanker. Maandelijkse injecties met lage doses hielpen spier- en vetmassa te behouden, verbeterden voedselinname en metabolisme en verlengden de overleving licht, zonder duidelijke toxiciteit of tekenen van chronische immuunactivatie.
Precisie-aanval op kanker en minder opgewonden auto-immuniteit
Om te testen of hoge fideliteit bij kopiëren echt belangrijk is, laadden de onderzoekers het VPg-vector met een complex oncolytisch construct, GSDMDENG, dat is ontworpen om gaten te slaan in mitochondriën van kankercellen en tumorspecifieke immuunresponsen te stimuleren. Wanneer hetzelfde construct op een conventioneel alphavirus-saRNA werd geplaatst, stapelden mutaties zich op na herhaalde kopieerrondes en verzwakten zo de selectieve kankerdodende en immuun-primende functies. In contrast behield het VPg-systeem de bedoelde sequentie, produceerde sterke doding van tumorcellen en veroorzaakte duurzame T-celresponsen die alvleesklierkanker in muismodellen vertraagden of voorkwamen. Ten slotte pasten ze VPg-saRNA toe op een andere uitdaging: chronische graft-versus-host-ziekte, waarbij immuuncellen de longen aanvallen na beenmergtransplantatie. Een VPg-saRNA dat geactiveerd proteïne C codeerde, verminderde schadelijke antistofvorming, voorkwam longlittekens en verbeterde de ademhaling bij muizen, terwijl een vergelijkbaar constructs op alphavirusbasis sterkere innate immuniteit opwekte en de uitkomsten verslechterde.
Waarom dit belangrijk is voor toekomstige RNA-geneesmiddelen
Samengevat schetst het werk een compacte, "plug-and-play" RNA-platform dat drie wenselijke eigenschappen combineert: het kopieert zichzelf nauwkeurig, is ontworpen om immuunalarmen te minimaliseren en omzeilt enkele van de knelpunten die standaard mRNA-translatie beperken. Omdat het therapeutische gen eenvoudig kan worden verwisseld in een vaste norovirus-gebaseerde ruggengraat, kunnen veel verschillende eiwitten—van hormonen tot stollingsregulatoren tot oncolytische middelen—op hetzelfde chassis worden getest. Hoewel er nog veel werk nodig is voor gebruik bij mensen, suggereert deze VPg-saRNA-benadering een weg naar RNA-geneesmiddelen die meer lijken op stabiele eiwitinfuzen: lage dosis, langduriger werkzaam en afgestemd om zelfs in zieke weefsels te functioneren waar gewone mRNA-boodschappen niet betrouwbaar kunnen worden afgelezen. 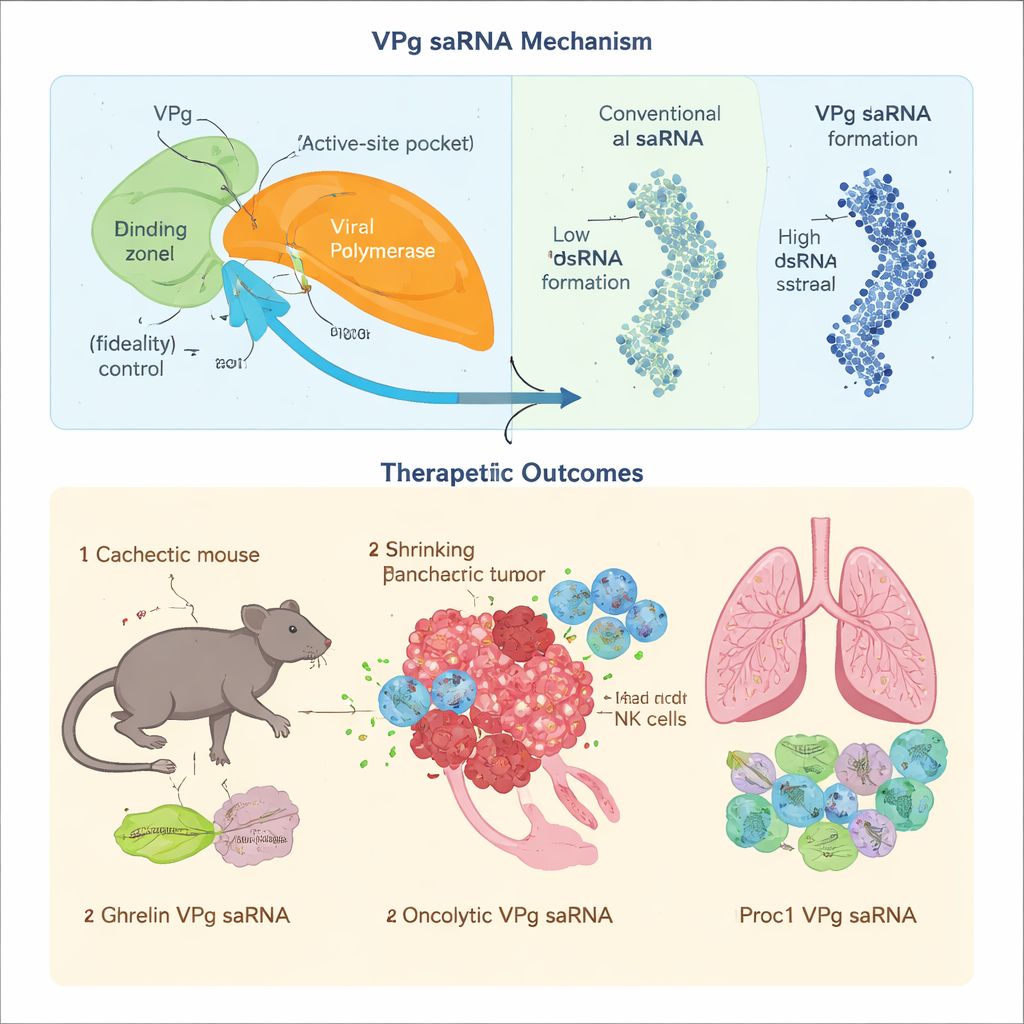
Bronvermelding: Feng, Z., Chu, L., Li, Q. et al. Engineered VPg saRNA achieves cap-independent, low-immunogenic and precise encoding of therapeutic proteins in vivo. Nat Commun 17, 1666 (2026). https://doi.org/10.1038/s41467-026-68364-w
Trefwoorden: zelf-amplificerend RNA, mRNA-therapeutica, norovirus VPg, kanker-cachexie, graft-versus-host ziekte