Clear Sky Science · nl
De rol van laag-complexe herhalingen in RNA–RNA-interacties en een deep-learningkader voor duplexvoorspelling
Plakkerige RNA-sequenties die het celgedrag vormen
In elke cel botsen RNA-moleculen voortdurend tegen elkaar en vormen vluchtige partnerschappen die helpen bepalen welke genen aanstaan, hoe eiwitten worden gemaakt en hoe cellen zich ontwikkelen. Deze studie toont aan dat veel van die RNA–RNA-ontmoetingen niet willekeurig zijn: ze worden aangestuurd door korte, eenvoudige, sterk repetitieve sequenties die werken als moleculaire klittenband. De onderzoekers bouwen ook een kunstmatige intelligentietool die kan aanwijzen waar zulke RNA-paren waarschijnlijk ontstaan, wat nieuwe wegen opent om te onderzoeken hoe cellen functioneren bij gezondheid en ziekte.
Eenvoudige herhalingen met krachtige effecten
RNA wordt vaak beschreven als een boodschapper die genetische informatie van DNA naar eiwitten draagt, maar het fungeert ook als een steiger, een regulator en een gids. Veel van die functies hangen af van het binden van twee RNA-strengen aan elkaar. Door gegevens uit meerdere grootschalige experimentele onderzoeken in menselijke en muiscellen te combineren, laten de auteurs zien dat de regio’s van RNA die daadwerkelijk deelnemen aan zulke koppelingen sterk verrijkt zijn in wat zij laag-complexe herhalingen noemen. Dit zijn reeksen opgebouwd uit korte motieven — zoals reeksen van G- en C-basen — die keer op keer worden herhaald. In plaats van genomisch “puin” blijken deze repetitieve delen juist uitstekende aanlegplaatsen te zijn waar één RNA zich aan veel anderen kan vasthechten, en zo dichte interactiehubs over het transcriptoom vormt. 
RNA-hubs voor ontwikkeling en regulatie
Toen het team onderzocht welke genen deze herhalingsrijke contactplaatsen dragen, verscheen een opvallend patroon: veel ervan coderen voor eiwitten die de ontwikkeling en celidentiteit sturen, zoals transcriptiefactoren. Zelfs in kankercellijnen die niet actief differentiëren, waren RNA’s die verbonden zijn met ontwikkelingsprogramma’s sterk betrokken bij contactvorming op basis van herhalingen. De auteurs zoemden ook in op specifieke lange niet-coderende RNA’s (lncRNA’s), RNA-moleculen die geen eiwitten coderen maar vaak wel reguleren. Bijvoorbeeld, doelen van het lncRNA TINCR en van een ander lncRNA dat belangrijk is voor de vorming van motorneuronen, Lhx1os, toonden beiden een overmaat aan complementaire herhalingen. In deze gevallen worden eenvoudige herhalingen op het lncRNA weerspiegeld door complementaire herhalingen in hun partner-RNA’s, wat stabiele paren mogelijk maakt die kunnen helpen de niveaus of de vertaling van sleutelgenen voor ontwikkeling fijn af te stemmen.
Waar eiwitten en bewerkingsenzymen meedoen
Deze door herhalingen gedreven RNA-contacten werken zelden alleen. De auteurs legden kaarten van eiwitbinding over hun interactiegegevens en vonden dat veel contactplaatsen met herhalingen ook worden herkend door RNA-bindende eiwitten die betrokken zijn bij translatiecontrole, RNA-afbraak en de vorming van cytoplasmatische granula zoals P-bodies en stressgranula. Eén eiwit in het bijzonder, STAU1, dat de vernietiging van zijn RNA-doelen kan triggeren, bindt vaak duplexen die gevormd worden via laag-complexe herhalingen. Het onderdrukken van STAU1 leidde tot hogere niveaus van RNA’s die bij deze duplexen betrokken zijn, vooral die met herhalingen, wat suggereert dat door herhalingen gemedieerde RNA-koppeling transcripties kan signaleren voor gecontroleerde afbraak. Dezelfde herhalingsrijke regio’s trekken ook RNA-bewerkingsenzymen aan zoals ADAR1, die specifieke basen binnen dubbelstrengs RNA chemisch modificeren, wat erop wijst dat laag-complexe herhalingen bewerkingsplaatsen helpen positioneren die het RNA-gedrag fijnregelen.
Een neuraal netwerk leren RNA-contacten te lezen
Standaard computermodellen proberen RNA–RNA-binding voornamelijk te voorspellen op basis van thermodynamische stabiliteit—hoeveel energie het kost om een duplex te vormen of te verbreken. Hoewel nuttig missen deze modellen vaak echte interacties die in cellen worden waargenomen, vooral tussen lange RNA’s. Om verder te gaan dan eenvoudige energieregels trainden de auteurs een deep-learningmodel genaamd RIME dat gebruikmaakt van ‘‘language model’’-achtige embeddings: numerieke representaties van RNA-sequenties die patronen coderen geleerd uit enorme verzamelingen nucleïnezuurgegevens. RIME krijgt paren van RNA-segmenten te zien en leert te classificeren of ze interageren, waarbij veel echte paringen uit psoralen-gebaseerde crosslinkingexperimenten als positieve voorbeelden dienen en zorgvuldig geconstrueerde niet-interagerende paren als negatieven. 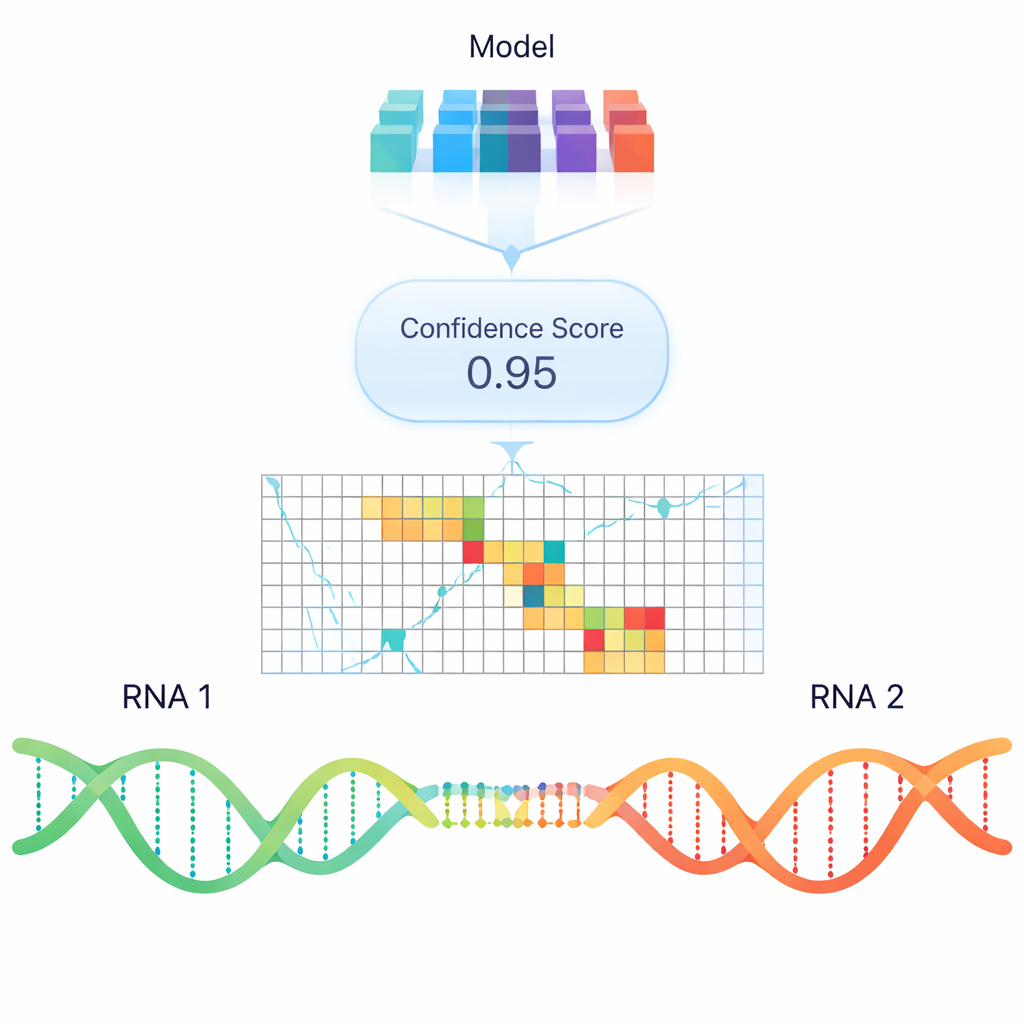
Slimmere voorspellingen en nieuwe biologische aanwijzingen
Bij vergelijking met toonaangevende thermodynamica-gebaseerde tools en een andere neurale-netwerkmethode presteert RIME consequent beter in het onderscheiden van echte RNA–RNA-contacten van lokvogels, vooral voor experimentele interacties met hoge betrouwbaarheid. Het voorspelt niet alleen of twee RNA’s zullen paren, maar richt zich vaak ook op de exacte regio’s die betrokken zijn, en leert vanzelf dat laag-complexe herhalingen sterke voorspellers van contact zijn. Opmerkelijk genoeg werkt hetzelfde model, getraind alleen op interacties tussen verschillende RNA’s, ook goed voor het voorspellen van interne baseparing binnen één enkel RNA-molecuul, in overeenstemming met zowel structurele experimenten als klassieke vouwalgoritmen. Voor niet-coderende regulatoren zoals TINCR, NORAD en SMaRT herontdekt RIME met succes bekende functionele interactieplaatsen en suggereert het aanvullende kandidaatregio’s.
Waarom dit ertoe doet
Voor een niet-specialistische lezer is de kernboodschap dat korte, repetitieve reeksen in RNA—die vroeger gemakkelijk als nuttig ruis konden worden afgedaan—fungeren als centrale verbindingspunten in het RNA-netwerk van de cel. Ze brengen RNA’s bijeen, nodigen regulatorische eiwitten en bewerkingsenzymen uit en worden veel gebruikt in paden die bepalen hoe cellen zich ontwikkelen en reageren op stress. Het nieuwe RIME-model geeft onderzoekers een krachtig middel om genomen te scannen op deze RNA–RNA-partnerschappen, inclusief die welke misgaan bij neurologische en andere ziekten geassocieerd met repetitie-expansies. In wezen laat dit werk zien dat het begrijpen—en voorspellen—hoe eenvoudige RNA-herhalingen aan elkaar kleven verborgen lagen van genregulatie kan onthullen.
Bronvermelding: Setti, A., Bini, G., Pellegrini, F. et al. The role of low-complexity repeats in RNA–RNA interactions and a deep learning framework for duplex prediction. Nat Commun 17, 1637 (2026). https://doi.org/10.1038/s41467-026-68356-w
Trefwoorden: RNA–RNA-interacties, laag-complexe herhalingen, lange niet-coderende RNA, deep learning, genregulatie