Clear Sky Science · nl
Transcriptomische handtekening-geleide uitroeiing van intermediaire alveolaire epitheelcellen verbetert longfibrose bij muizen
Waarom littekenvorming in de longen ertoe doet
Longfibrose is een ernstige longaandoening waarbij de fijne luchtzakjes geleidelijk veranderen in stijf littekenweefsel, waardoor elke ademhaling zwaar aanvoelt. Artsen weten dat deze littekenvorming begint wanneer normale herstelprocessen ontsporen, maar het was onduidelijk welke specifieke cellen daarvoor verantwoordelijk zijn en hoe ze verwijderd kunnen worden zonder gezond longweefsel te beschadigen. Deze studie onderzoekt een nieuwe manier om de moleculaire boodschappen binnen longcellen te "lezen", die informatie te gebruiken om schadelijke overgangscellen te identificeren en ze selectief uit te schakelen om littekenvorming bij muizen te verminderen.
Cellen betrapt tijdens fout herstel
Na longletsel delen speciale surfactant-producerende cellen, de type II-cellen, zich normaal en rijpen vervolgens uit tot dunne type I-cellen die de luchtzakjes bekleden en zuurstof naar het bloed laten passeren. Bij fibrose blijven veel van deze cellen vastzitten in een tussentoestand in plaats van deze transitie te voltooien. Eerdere single-cell RNA-sequencingstudies vonden deze intermediaire cellen zowel bij muizen als bij mensen, maar het was niet duidelijk of ze slechts voorbijgangers waren of belangrijke drijvers van de ziekte. De onderzoekers richtten zich op een muizentransitioneel celtype dat Krt8+ alveolaire differentiatie-intermediates heet, en hun menselijke tegenhangers die bekendstaan als aberrante basaloïde cellen, die in grote aantallen voorkomen in verkleefde longen.
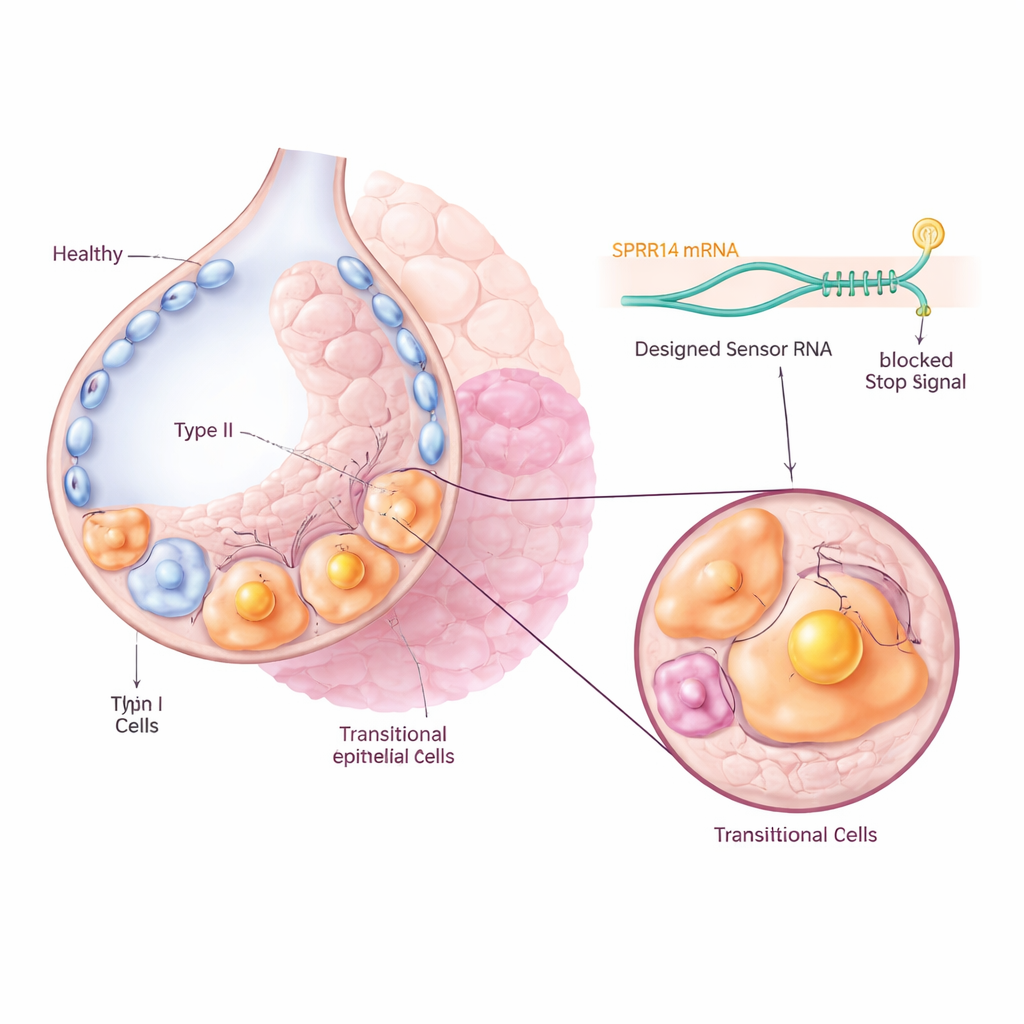
Een unieke moleculaire naamkaart vinden
Om deze probleemcellen aan te pakken zonder hun gezonde buren te raken, doorzocht het team eerst grote genexpressiedatasets op een merker die sterk en specifiek aanstond in de transitionele populatie. Ze identificeerden een molecuul genaamd SPRR1A als een opvallende "naamkaart": het was sterk verrijkt in Krt8+ intermediaire cellen in fibrotische muizenlongen en in KRT5-/KRT17+ aberrante basaloïde cellen van patiënten met idiopathische longfibrose, maar grotendeels afwezig in normale longcellen. Microscopen van zowel muis- als menslongweefsel bevestigden dat SPRR1A vooral verscheen in beschadigde, gereconstrueerde regio's en niet in gezonde luchtzakjes, wat suggereert dat het als een precies houvast kan dienen om de daders te herkennen.
Cellen programmeren met een RNA-sensor
De onderzoekers gebruikten vervolgens een recent ontwikkelde technologie genaamd CellREADR, die functioneert als een intern moleculair sensor. Ze ontwierpen korte RNA-sequenties die kunnen baseparen met SPRR1A-RNA binnen een cel. Wanneer de sensor SPRR1A detecteert, activeert hij de productie van een gekoppeld "effector"-eiwit, zoals een fluorescente marker of een receptor die de cel gevoelig maakt voor een medicijn. Bij muizen werden virussen gebruikt om deze sensor–effectorconstructen naar longcellen te brengen. Alleen cellen die actief SPRR1A produceerden schakelden het fluorescente signaal in, waardoor het team de transitionele cellen direct uit fibrotische longen kon volgen en isoleren. Single-cell sequencing toonde aan dat de gelabelde cellen sterk overeenkwamen met het bekende transitionele gendrukpatroon, wat bevestigde dat de RNA-sensor nauwkeurig de beoogde populatie doelwitte.
Schadelijke intermediaten uitschakelen
Vervolgens werd de effector gewijzigd van een onschuldig fluorescerend eiwit naar de difterie-toxine-receptor, zodat SPRR1A-positieve cellen selectief gedood konden worden door difterie-toxine toe te dienen. Door de behandeling te timen met de piek van de overgangscellen na chemisch longletsel, konden de auteurs ongeveer een derde van deze populatie verwijderen. Deze gerichte uitputting leidde tot opvallend minder longlittekenvorming: er was minder collageenophoping, lagere niveaus van fibrotische eiwitten en meer normaal ogende luchtzakstructuren. Gedetailleerde analyses toonden dat de meeste SPRR1A-positieve cellen tekenen droegen van een gestreste, verouderingsachtige toestand, met een kleine subset die in staat was tot sterke proliferatie, wat suggereert dat deze intermediaten zowel niet goed herstellen als het fibrotische proces in stand houden.
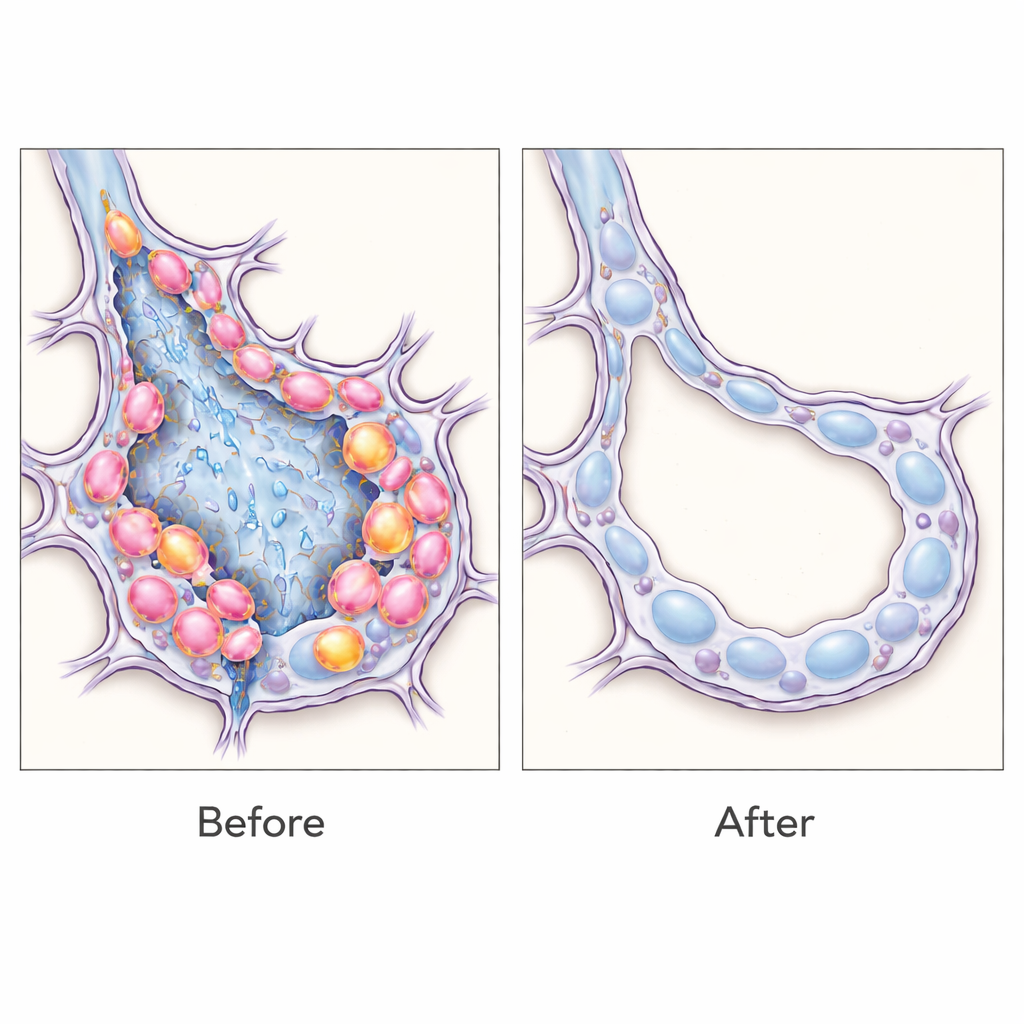
Wat dit betekent voor toekomstige behandelingen
Deze bevindingen pleiten ervoor dat transitionele epitheelcellen niet alleen markeringen zijn maar actieve drijvers van longfibrose, en dat het selectief verwijderen ervan de balans in muizen kan kantelen naar een gezondere longarchitectuur. Breder laat het werk een flexibele strategie zien: door cel-specifieke RNA-handtekeningen te "lezen", kunnen onderzoekers nauw omschreven cellulaire populaties labelen, bestuderen en zelfs elimineren in levend weefsel zonder telkens speciale diermodellen te hoeven maken. Hoewel er nog veel werk nodig is voordat zulke RNA-sensorische hulpmiddelen veilig voor mensen aangepast kunnen worden, opent deze benadering een weg naar precisietherapieën die precies die celtypes richten die het herstel verstoren bij chronische longlittekening en mogelijk andere fibrotische aandoeningen.
Bronvermelding: Peng, F., Jiang, Cs., Zheng, Z. et al. Transcriptomic signature-guided depletion of intermediate alveolar epithelial cells ameliorates pulmonary fibrosis in mice. Nat Commun 17, 1636 (2026). https://doi.org/10.1038/s41467-026-68354-y
Trefwoorden: longfibrose, alveolaire epitheelcellen, single-cell RNA sequencing, RNA-detectietechnologie, cellulaire veroudering