Clear Sky Science · nl
Single-nucleus-atlas van de centrale amygdala onthult chromatine- en gentranscriptiedynamiek bij alcoholverslaving
Waarom dit onderzoek van belang is voor het dagelijks leven
Alcoholverslaving (alcohol use disorder, AUD) treft miljoenen mensen en hun families, maar we weten nog verrassend weinig over wat langdurig zwaar drinken op celniveau met het menselijk brein doet. Deze studie zoomt in op één klein maar cruciaal gebied — de centrale amygdala, een knooppunt voor angst, stress en motivatie — om in kaart te brengen hoe alcohol hersencellen en hun genetische regelsystemen hervormt. Door geavanceerde "single-cell"-sequencing te combineren met genetisch onderzoek naar verslavingsrisico, beginnen de auteurs te verklaren waarom sommige mensen kwetsbaarder zijn voor AUD en hoe alcohol blijvende moleculaire littekens in de hersenen achterlaat.
Nauw kijken naar een klein hersenknooppunt
De centrale amygdala is een belangrijk uitgangsstation in het emotie- en stressnetwerk van de hersenen en staat sterk in verband met het verminderen van angst, craving en dwangmatig alcoholgebruik. In dit werk analyseerden onderzoekers ongeveer 175.000 individuele celkernen afkomstig van de centrale amygdala van 50 mensen — 22 met een voorgeschiedenis van alcoholverslaving en 28 zonder AUD. Met een technologie die zowel genactiviteit (RNA) als chromatine‑toegankelijkheid (hoe "open" of "gesloten" DNA is) in dezelfde cel leest, bouwden ze een gedetailleerde atlas van alle belangrijke hersenceltypen in dit gebied, inclusief verschillende soorten neuronen en ondersteunende cellen zoals astrocyten en microglia. Ze vonden dat remmende (inhiberende) neuronen — die hersenactiviteit dempen of vormgeven — bijzonder talrijk zijn in de centrale amygdala en schijnbaar specifiek zijn aangetast bij mensen met AUD. 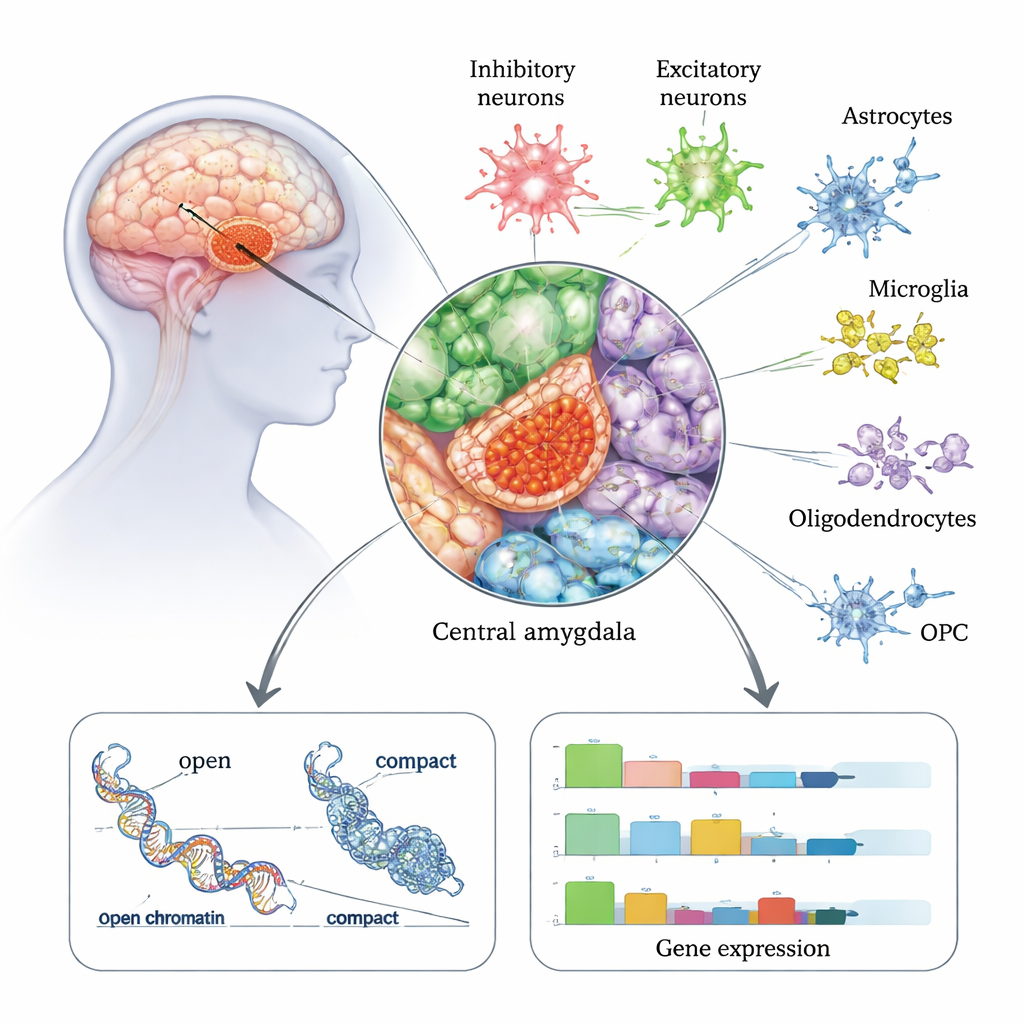
Welke cellen en genen veranderen bij alcoholverslaving?
Het team vergeleek systematisch genactiviteit tussen mensen met en zonder AUD, per celtype. Ze ontdekten meer dan 1.800 genen waarvan de activiteit in specifieke celpopulaties was veranderd, met de grootste verschuivingen in inhiberende neuronen, gevolgd door exciterende neuronen en astrocyten. Eén subtype inhiberende neuron, gemarkeerd door het peptide proenkephalin (PENK), vertoonde bijzonder sterke veranderingen. Veel van de aangedane genen zijn betrokken bij communicatie tussen hersencellen, met name de balans tussen het exciterende glutamaat en het inhiberende GABA. Bijvoorbeeld het gen GABRA2, dat helpt bij de opbouw van een belangrijk type GABA-receptor, was verhoogd in bepaalde inhiberende neuronen, terwijl GRM8, een glutamaatreceptor, en NCAM1, een celadhesiemolecuul belangrijk voor synapsen, in tegengestelde richtingen veranderden tussen neuron-subtypes. Deze patronen suggereren dat de fijnregeling van excitatie en inhibitie in de centrale amygdala verstoord is bij AUD.
De schakelaars van het brein: chromatine en regelende elementen
Genen werken niet in isolatie; ze worden gereguleerd door DNA-stukken die functioneren als schakelaars en dimmers. Door naar chromatine te kijken — de manier waarop DNA is verpakt — identificeerden de onderzoekers meer dan een half miljoen kandidaat-regelgebieden en koppelden die op celtype‑specifieke wijze aan nabijgelegen genen. Bijna de helft van deze elementen was uniek voor één celtype, wat benadrukt hoe gespecialiseerd verschillende hersencellen zijn. Veel regelgebieden die veranderden bij AUD waren verbonden met genen die betrokken zijn bij calciumhuishouding en glutamaat‑signaalgeving, zoals CALN1, een calciumbindend gen dat sterk actief is in neuronen. In inhiberende neuronen toonde CALN1 zowel verhoogde expressie als dichte clusters van regelende lussen, wat impliceert dat alcoholblootstelling de lokale DNA‑architectuur die dit gen controleert herschikt. 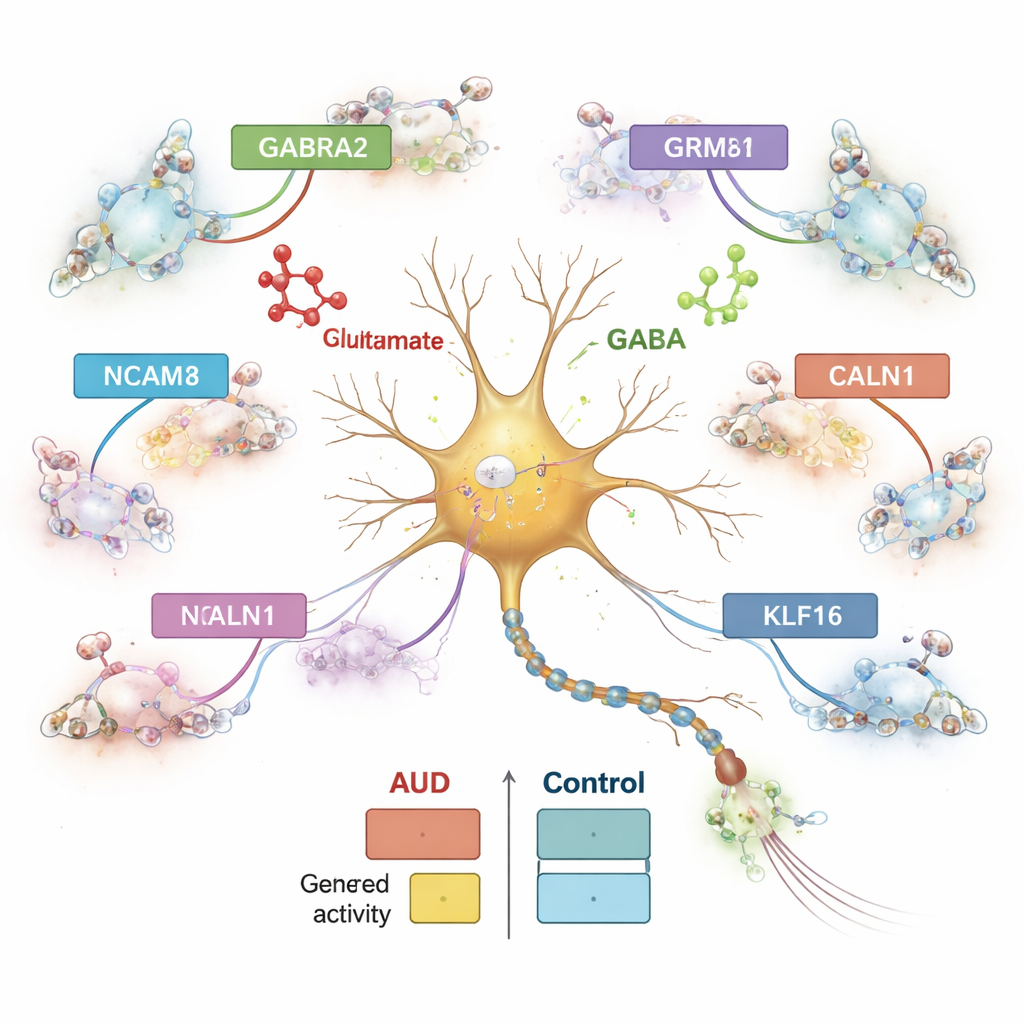
Van risicogenen naar echte hersenveranderingen
Genetische studies hebben vele DNA‑varianten geïdentificeerd die het risico op alcoholproblemen verhogen, maar waar en hoe ze in de hersenen werken was onduidelijk. Door hun single‑cell-kaarten te overleggen met grootschalige genome‑wide associatiestudies van problematisch alcoholgebruik vonden de auteurs dat risicogenen onevenredig actief en gedysreguleerd zijn in neuronen van de centrale amygdala, vooral in inhiberende neuronen. Ze identificeerden meer dan 200 waarschijnlijke causale risicovarianten die binnen regelgebieden liggen die open zijn in specifieke celtypen. Sommige vielen in of nabij genen die al aan verslaving gekoppeld zijn, zoals CACNA1C en DRD2, die helpen bij het regelen van neuronale prikkelbaarheid en dopaminesignalering. Andere, waaronder SEMA6D en NF1, verschenen als nieuwe kandidaten. Het team identificeerde ook een familie transcriptiefactoren genaamd Kruppel‑achtige factoren (met name KLF16) die brede veranderingen in calcium‑ en glutamaatgerelateerde genen lijkt te coördineren, en ze bevestigden delen van dit regelnetwerk in een muismodel van acute alcoholexpositie.
Wat dit betekent voor het begrijpen en behandelen van AUD
Kort gezegd toont deze studie aan dat alcoholverslaving niet slechts een diffuse hersenstoornis is, maar een hoogst georganiseerde verstoring geconcentreerd in bepaalde celtypen en moleculaire routes binnen een kritisch emotioneel knooppunt. Inhiberende neuronen van de centrale amygdala, samen met astrocyten en andere ondersteunende cellen, tonen gecoördineerde veranderingen in genactiviteit en in de DNA‑schakelaars die deze genen aansturen — vooral in systemen die glutamaat, GABA en calcium signalen reguleren. Door deze cellulaire veranderingen te koppelen aan genetische risicovarianten biedt het werk een routekaart die erfelijke kwetsbaarheid verbindt met concrete moleculaire gebeurtenissen in de hersenen. In de loop van de tijd kunnen dergelijke celspecifieke kaarten de ontwikkeling van meer precieze behandelingen begeleiden die de balans tussen excitatie en inhibitie herstellen, in plaats van breed op het hele brein in te grijpen.
Bronvermelding: Lee, C.Y., Hwang, A., McRiley, D. et al. Central amygdala single-nucleus atlas reveals chromatin and gene transcription dynamics in human alcohol use disorder. Nat Commun 17, 1634 (2026). https://doi.org/10.1038/s41467-026-68351-1
Trefwoorden: alcoholverslaving, centrale amygdala, single-cell genomica, inhiberende neuronen, genregulatie