Clear Sky Science · nl
Van TDP-43/RNA-complexvorming naar ziektegerelateerde TDP-43-aggregatie via een structurele en cellulaire aanpak
Waarom dit herseneiwit ertoe doet
Neurodegeneratieve aandoeningen zoals amyotrofische laterale sclerose (ALS) en frontotemporale dementie kenmerken zich vaak door opeenhopingen van verkeerd gevouwen eiwitten in zenuwcellen. Een van de meest voorkomende daders is een eiwit genaamd TDP-43, dat normaal helpt bij de verwerking van RNA — de werkbare kopie van onze genen. Deze studie stelt een cruciale vraag: wat doet TDP-43 in gezonde cellen, en wat gaat er mis waardoor een nuttige RNA-helper verandert in een toxisch, aggregaatvormend eiwit?
Hoe TDP-43 werkt in gezonde zenuwcellen
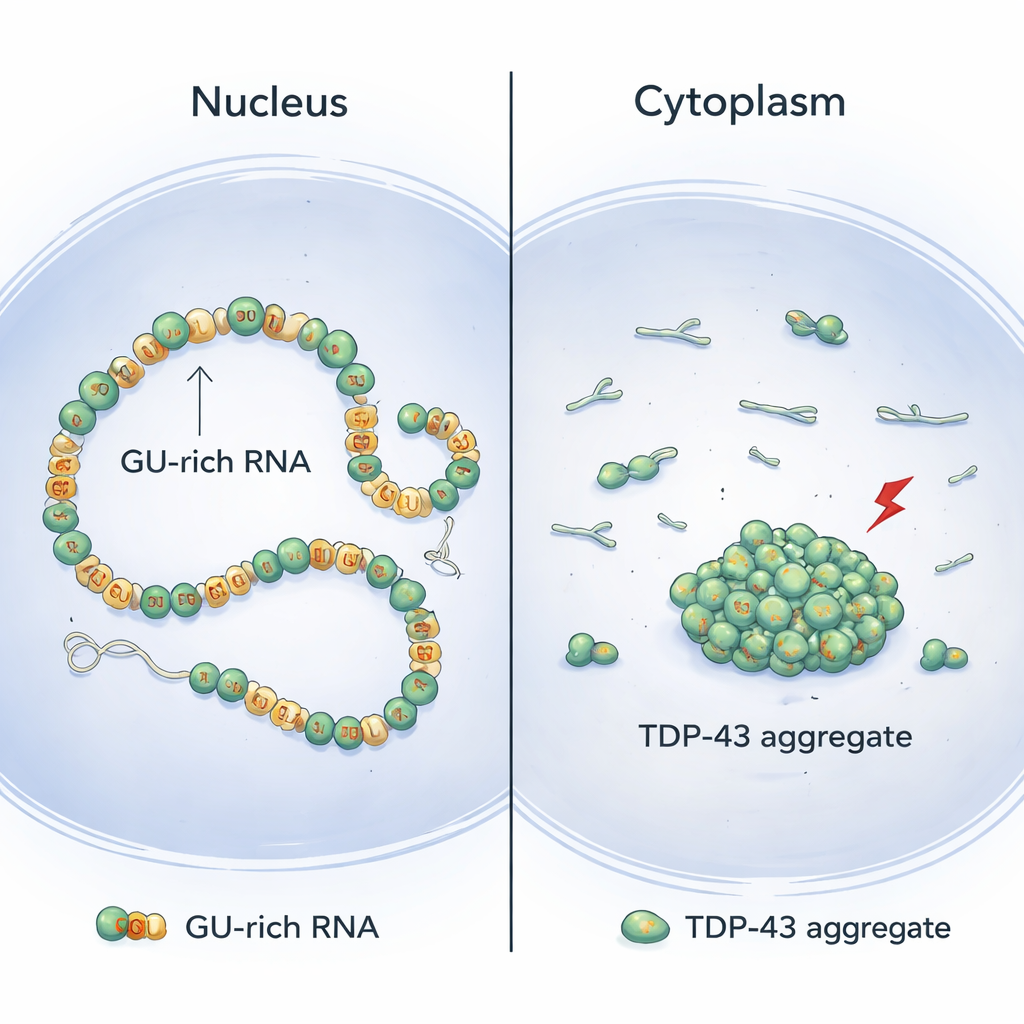
TDP-43 bevindt zich meestal in de celkern, waar het bindt aan lange stuken RNA die rijk zijn aan herhaalde “GU”-bouwstenen. Met een combinatie van structurele biologie en celexperimenten tonen de auteurs aan dat TDP-43-moleculen zich cooperatief opstellen langs deze GU-rijke regio’s en zo gladde, continue ketens op het RNA vormen. In deze rangschikking blijft het voorste deel van het eiwit — het N-terminaal domein — fysiek gescheiden tussen naburige moleculen. Daardoor blijven deze N-terminaalkussentjes beschikbaar om over langere afstanden verbindingen te maken met verafgelegen GU-rijke delen van hetzelfde RNA, waardoor lange introns (de niet-coderende stukken binnen genen) zachtjes worden gelusd en gecompacteerd zonder te klonteren.
Een ingebouwde touwtrekwedstrijd binnen het eiwit
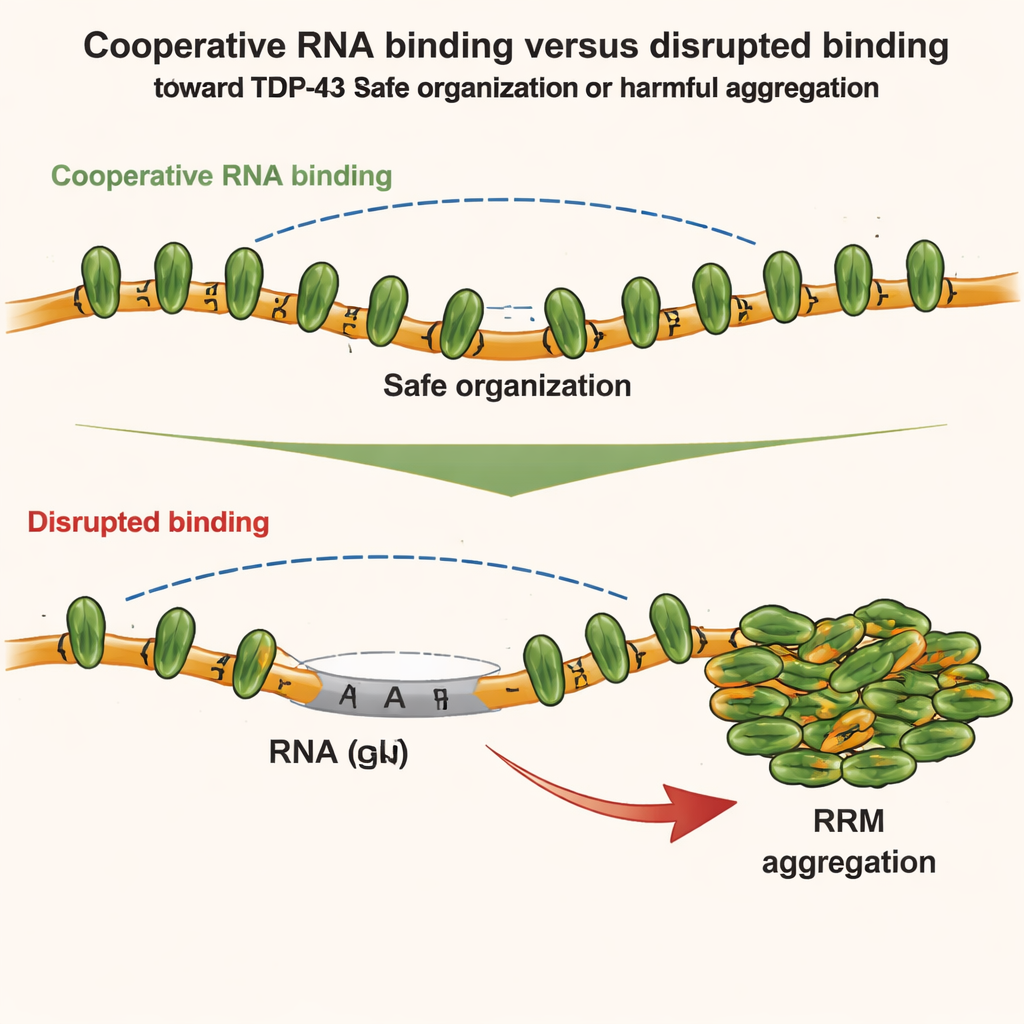
Het team onderzocht daarna hoe verschillende delen van TDP-43 met elkaar concurreren of samenwerken. Ze richtten zich op twee regio’s: het N-terminaal domein, dat aan andere N-terminale domeinen kan hechten, en de centrale RNA-bindende modules, die cooperatieve binding langs GU-rijk RNA aansturen. Met gevoelige technieken zoals NMR-spectroscopie, calorimetrie en small-angle X-ray scattering ontdekten ze dat wanneer TDP-43 cooperatief aan RNA bindt, de geometrie van de keten de directe N-terminaal-tot-N-terminaal contacten tussen aangrenzende moleculen juist verzwakt. Met andere woorden: sterke cooperatieve RNA-binding houdt lokale N-terminaalinteracties in toom. Maar wanneer deze cooperativiteit wordt verbroken — bijvoorbeeld door niet-GU-stukken in het RNA in te voegen of door TDP-43 te muteren — komen N-terminaalregio’s van naburige eiwitten dichter bij elkaar en kunnen ze nu aan elkaar vastklikken.
Van nuttige compactie tot schadelijke klontering
Deze structurele inzichten werden getest in levende cellen. De auteurs gebruikten geconstrueerde celsystemen om te volgen hoe verschillende TDP-43-mutanten zich mengen of scheiden binnen kunstmatige, RNA-rijke compartimenten. Ze vonden dat zowel cooperatieve RNA-binding als N-terminaalinteracties helpen bij het organiseren van TDP-43 in hogere-orde assemblages, maar op verschillende manieren. Cooperatieve binding rekt eiwitten uit langs GU-rijk RNA, terwijl N-terminaalcontacten verre clusters aan elkaar verbinden. Onder milde oxidatieve stress verandert het beeld echter. Een chemische stressor (arseniet) veroorzaakt specifieke chemische veranderingen — acetylatie — op de centrale RNA-bindende motieven, waardoor deze neigen samen te kleven. Als de cooperatieve binding aan RNA intact is, blijft TDP-43 grotendeels oplosbaar. Als de cooperativiteit verzwakt is, functioneren N-terminaallinks tussen nabijgelegen TDP-43-moleculen als een steiger die de geacetyleerde kern samenbrengt en zo onomkeerbare aggregatie bevordert.
Waarom TDP-43 meer in het cytoplasma klontert
Het model dat uit dit werk naar voren komt, helpt verklaren waarom TDP-43-aggregaten vaak in het cytoplasma van zieke neuronen worden aangetroffen in plaats van in de kern. In de kern zijn lange introns met vele GU-herhalingen gebruikelijk, wat continue, cooperatieve binding bevordert die risicovolle N-terminaalcontacten tussen buren laag houdt en veilige langafstandslussenvorming toestaat. In het cytoplasma daarentegen bevatten rijpe RNA’s veel minder GU-rijke stukken. Dit maakt TDP-43-binding meer patchy en minder cooperatief, waardoor de kans toeneemt dat naburige N-terminaaldomeinen interactie met elkaar aangaan en het toneel vormen voor aggregatie zodra stress-geïnduceerde chemische veranderingen optreden. Ter ondersteuning van dit beeld verminderde het kunstmatig toevoegen van extra GU-rijke introns in de kern de TDP-43-aggregatie onder stress.
Wat dit betekent voor toekomstige therapieën
Kort gezegd schetst de studie TDP-43 als een eiwit in evenwicht tussen nuttige RNA-organisatie en schadelijke klontering, waarbij cooperatieve binding aan GU-rijk RNA fungeert als een veiligheidsmechanisme. Wanneer dat vangnet faalt — door gewijzigde RNA-sequenties, eiwitmutaties of cellulaire stress — kunnen dezelfde domeinen die normaal lange RNA-segmenten compacteren, in plaats daarvan de vorming van toxische aggregaten aansturen. Voor niet-specialisten is de belangrijkste conclusie dat het behouden van het juiste soort interacties tussen TDP-43 en RNA een veelbelovende strategie kan zijn om het eiwitklonteren gezien bij ALS en verwante hersenziekten te voorkomen of te vertragen.
Bronvermelding: Feng, Y., Joshi, V., Pankivskyi, S. et al. From TDP-43/RNA complex formation to disease-linked TDP-43 aggregation through a structural and cellular approach. Nat Commun 17, 1631 (2026). https://doi.org/10.1038/s41467-026-68346-y
Trefwoorden: TDP-43-aggregatie, RNA-bindende eiwitten, ALS, eiwit–RNA-interacties, neurodegeneratie