Clear Sky Science · nl
Atomair precieze ligand-engineering van goudnanodeeltjes via interfaciale massatransfer
Waarom piepkleine gouddeeltjes belangrijk zijn voor de gezondheid
Medische beeldvorming maakt steeds vaker gebruik van nanodeeltjes — uiterst kleine deeltjes die een paar duizend keer kleiner zijn dan een mensenhaar — om organen en tumoren diep in het lichaam zichtbaar te maken. Deze studie laat zien hoe wetenschappers nu de buitenste coating van ultrasmalle gouddeeltjes bijna atoom voor atoom kunnen verfijnen, zodat dezelfde lichtgevende kern naar verschillende organen gestuurd kan worden, met name van de lever en milt naar de nieren. Dergelijke controle kan helpen bij het ontwerpen van veiligere contrastmiddelen en medicijndragers die precies daar komen waar artsen ze willen en het lichaam schoner verlaten.
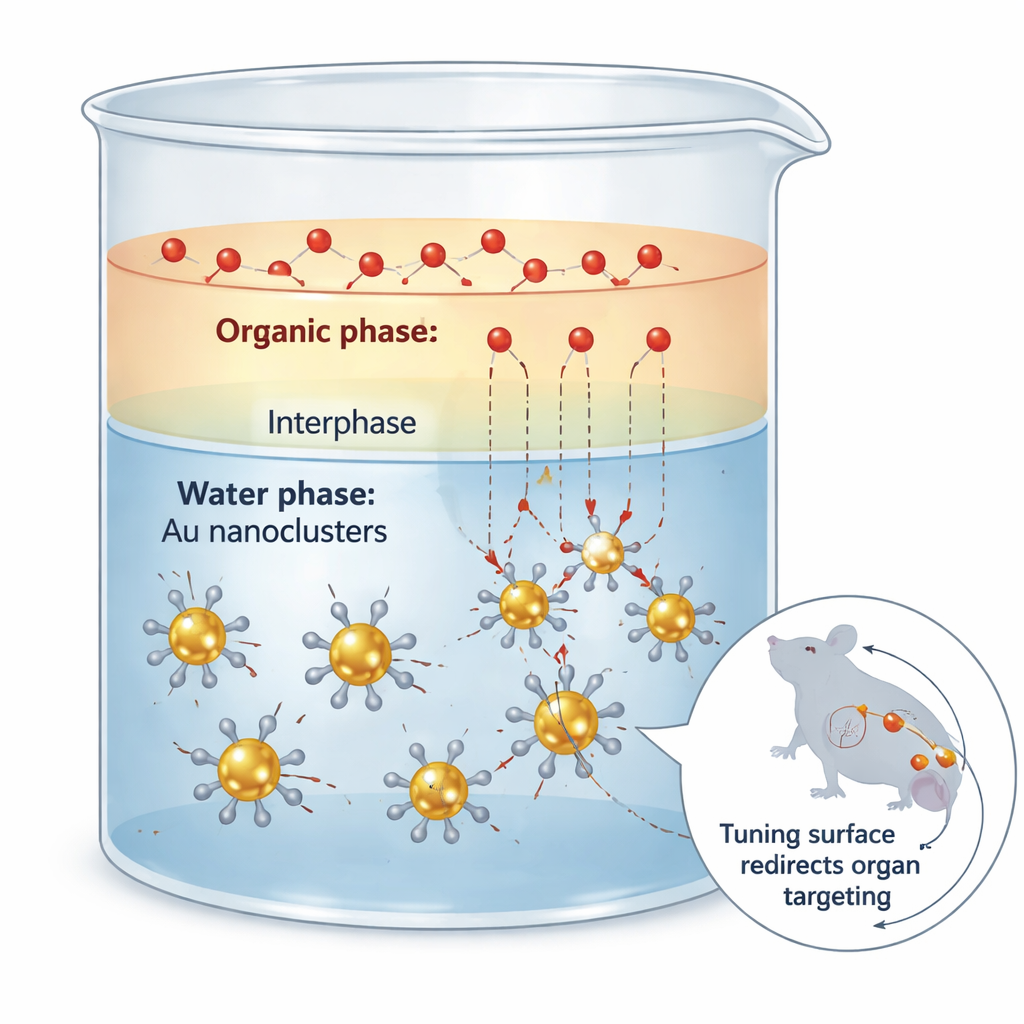
De uitdaging van het aankleden van piepkleine goudklusters
Goudnanoklusters zijn ultrasmalle gouddeeltjes die zich meer gedragen als grote moleculen dan als metalen korrels. Ze kunnen licht uitzenden in het near-infrared II-venster, wat diep in weefsel doordringt en scherpe beelden met weinig achtergrond geeft. Bijna alles aan hoe deze klusters zich in het lichaam gedragen — waar ze heen gaan, hoe lang ze circuleren en hoe ze worden uitgescheiden — hangt echter niet van het goud zelf af, maar van de organische liganden, of de "schil"-moleculen, die aan hun oppervlak gebonden zijn. Traditionele manieren om deze schil te veranderen werken vaak als grove chirurgie: de reactie gaat te snel, de coating wordt ongelijkmatig en de goudkern kan gedeeltelijk aangetast worden, waardoor zowel de structuur als de optische eigenschappen kapot gaan.
Het verkeer tussen twee vloeistoffen vertragen
De onderzoekers pakten dit probleem aan door een eenvoudig fysisch idee te benutten: massa-overdrachtsweerstand bij de grens tussen twee vloeistoffen die niet volledig mengen. Ze plaatsten de goudklusters in water en de inkomende zwavelhoudende liganden in een organisch oplosmiddel zoals ethylacetaat. In het dunne gebied waar de twee vloeistoffen deels mengen, diffunderen de liganden langzaam naar de klusters en wisselen ze met de oorspronkelijke schil. Zorgvuldige kinetische metingen toonden aan dat het ongewenste "etsen" van de goudkern extreem gevoelig is voor de concentratie van vrije ligand, terwijl de gewenste uitwisseling veel minder gevoelig is. Door de twee-fasenopstelling te gebruiken om de vrije liganden op een laag maar continu aangevuld niveau te houden, onderdrukte het team het etsen ongeveer zestigvoudig terwijl ze het grootste deel van het nuttige uitwisselingssnelheid behielden.
Een nauwkeurige moleculaire gereedschapsset bouwen
Met deze interfaciale methode konden de auteurs oppervlakliganden op een modelgoudkluster, Au25, op zeer gecontroleerde wijze vervangen. Ze begonnen met klusters beschermd door een negatief geladen sulfonzuur-ligand en wisselden die om voor allerlei nieuwe thiolliganden met carboxylzuren, aminen, hydroxylgroepen, nitrogroepen en hydrofobe aromatische ringen. Massaspectrometrie toonde schone, goed gedefinieerde mengsels aan, zoals Au25-klusters met specifieke aantallen van elk type ligand, in plaats van brede, rommelige distributies. De methode werkte ook voor andere klustergroottes en ligandfamilies, wat suggereert dat het een algemene strategie is om robuuste, op maat gemaakte goudnanoklusters te maken voor verschillende toepassingen.
Nanodeeltjes van lever naar nieren sturen
De meest opvallende test van deze precisie kwam uit in vivo beeldvormingsexperimenten in muizen. Door geleidelijk een positief geladen ligand, p-aminothiophenol, in de anders negatief geladen schil te introduceren, creëerde het team een reeks klusters waarvan de totale oppervlaktespanning verschuift van sterk negatief naar bijna zwitterionisch (in evenwicht gebrachte positieve en negatieve groepen). Alle versies gloeiden vergelijkbaar in laboratoriumtests, maar hun biodistributie in muizen verschilde dramatisch. Volledig negatieve klusters stapelden zich voornamelijk op in lever en milt. Naarmate meer positieve liganden werden toegevoegd, nam het signaal in deze organen af en nam het in de nieren en blaas toe, wat wijst op verbeterde renale klaring. Toen in plaats van de amine een neutrale hydroxyl-ligand werd gebruikt, trad deze verschuiving niet op, wat de bijzondere rol van positieve ladingen bij het omleiden van de deeltjes onderstreept.
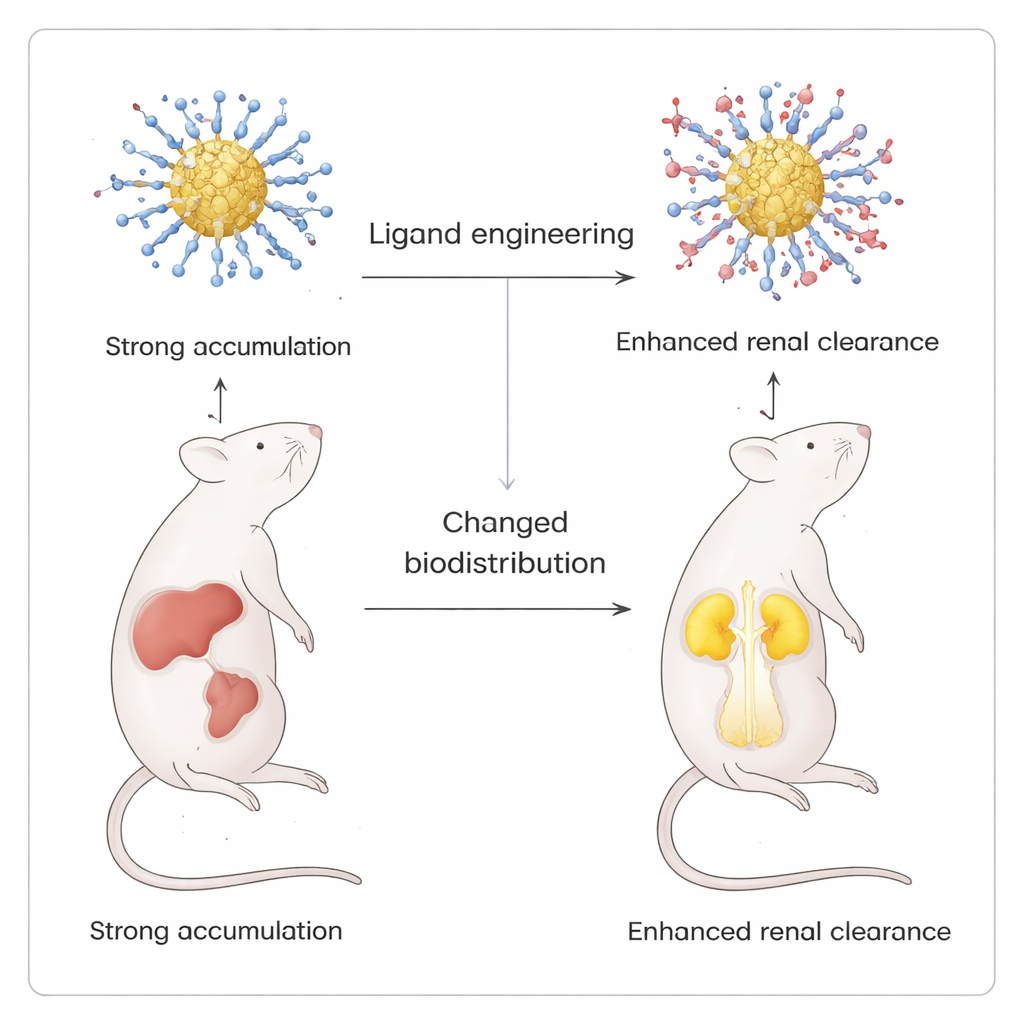
Wat dit betekent voor toekomstige medicijnen
Voor niet-specialisten is de belangrijkste conclusie dat wetenschappers een manier hebben gevonden om lichtgevende goudnanoklusters te "omkleden" met moleculaire coatings die bijna één molecuul per keer kunnen worden afgestemd, zonder het deeltje daaronder te beschadigen. Door een zachte tweevloeistofopzet te gebruiken, kunnen ze zowel de chemie als het uiteindelijke lot van deze deeltjes in het lichaam beheersen. Dit niveau van controle maakt het mogelijk om contrastmiddelen en potentiële medicijndragers te ontwerpen die specifieke organen laten oplichten en daarna via de nieren vertrekken in plaats van in de lever en milt achter te blijven, wat de weg vrijmaakt voor veiligere en beter voorspelbare nanogeneeskunde.
Bronvermelding: Zhang, B., Xiao, F., Song, X. et al. Atomically precise ligand engineering of gold nanoparticles via interphase mass transfer. Nat Commun 17, 1630 (2026). https://doi.org/10.1038/s41467-026-68345-z
Trefwoorden: goudnanoklusters, ligand-engineering, bio-imaging, nanogeneeskunde, biodistributie