Clear Sky Science · nl
DOT1L-activiteit beperkt de snelheid van transcriptie-elongatie en bevordert RNAPII-pauzering om mutagenese door AID te faciliteren
Hoe onze immuuncellen riskante DNA-bewerkingen fijnregelen
Ons immuunsysteem maakt krachtige antilichamen door doelbewust het eigen DNA te muteren, een riskante strategie die soms kanker kan aanwakkeren. Deze studie stelt een bedrieglijk eenvoudige vraag met grote implicaties: wat bepaalt waar en hoe efficiënt deze opzettelijke mutaties optreden? Het antwoord draait om een eiwit genaamd DOT1L, dat de leestempo van genen in B-cellen aanpast en daarmee helpt de mutatiemachine op de juiste plekken te richten.
Mutatie inschakelen om antilichamen te verscherpen
Wanneer B-cellen een infectie tegenkomen, verbeteren ze hun antilichamen op twee manieren. Ze brengen kleine wijzigingen in het bindingsgebied van het antilichaam aan om beter aan ziekteverwekkers te binden, en ze wisselen de staart (isotype) van het antilichaam om de immuunrespons te veranderen. Beide upgrades beginnen met een enzym dat AID heet, dat het DNA in actief afgelezen genen knipt en aanpast. Hoewel AID cruciaal is voor goede immuniteit, kan het ook andere genen raken, waardoor gevaarlijke breuken ontstaan die bloedkankers bevorderen. Eerder werk liet zien dat AID de voorkeur geeft aan sterk afgelezen genen en genen die gereguleerd worden door krachtige DNA-schakelaars genaamd super-enhancers, maar dat verklaarde nog niet volledig waarom slechts een selecte subset van genen echt kwetsbaar is.
Een chromatinemerk dat AID-gevoelige genen markeert
De auteurs concentreerden zich op eiwitten die dicht bij AID in de kern zitten. Met een proximiteits-labelingstechniek in menselijke cellen vonden ze dat AID in de buurt van DOT1L clustert, een enzym dat een specifieke plek op de histoon-eiwitten waarop DNA is gewikkeld, markeert. Deze markering — een chemische tag op histon H3 op positie K79 — komt veel voor op actieve genen. In muis-B-cellen dragen genen die AID vaak muteert — inclusief antilichaamgenen en kankergygerelateerde off-targets — bijzonder hoge niveaus van deze door DOT1L gemaakte merken. Toen de onderzoekers DOT1L uitschakelden in B-cellijnen of zijn activiteit blokkeerden met een geneesmiddel, daalde het ‘class switching’ van antilichamen, net als AID-gedreven DNA-breuken en kankervormende fusies tussen antilichaamgenen en het groeigen cMyc. Belangrijk is dat de katalytische functie van DOT1L, en niet alleen de aanwezigheid ervan, benodigd was: mutante versies die de histoonmarkering niet meer konden aanbrengen faalden in het herstellen van normale antibody switching.
De genlezer vertragen om AID tijd te geven
Op het eerste gezicht is dit verwarrend omdat DOT1L geassocieerd is met actieve genen, terwijl het verwijderen ervan genen niet simpelweg uitzet. Met een methode die nieuwgemaakte RNA-moleculen vastlegt, ontdekte het team dat B-cellen zonder DOT1L juist meer nascent-transcripten produceerden over veel DOT1L-gemarkeerde genen — hoewel er iets minder van het belangrijkste gen-lezende enzym, RNA-polymerase II, op die genen aanwezig was. Door deze nascent-RNA-metingen te combineren met kaarten van polymerasebezetting concludeerden ze dat DOT1L-markeringen onder normale omstandigheden fungeren als zachte verkeersdrempels. Ze vertragen de polymerase terwijl deze langs het gen beweegt en verlengen korte pauzes nabij het begin en binnen het genlichaam van DOT1L-gemarkeerde genen. Zonder DOT1L vliegt de polymerase sneller en zijn de pauzes korter. Omdat AID korte vensters nodig heeft waarin DNA blootligt en de polymerase blijft hangen, vermindert deze versnelling paradoxaal genoeg AID’s vermogen zich vast te hechten en zijn werk te doen, zelfs als de totale transcriptie toeneemt.
Het loskoppelen van genactiviteit en mutatierisico
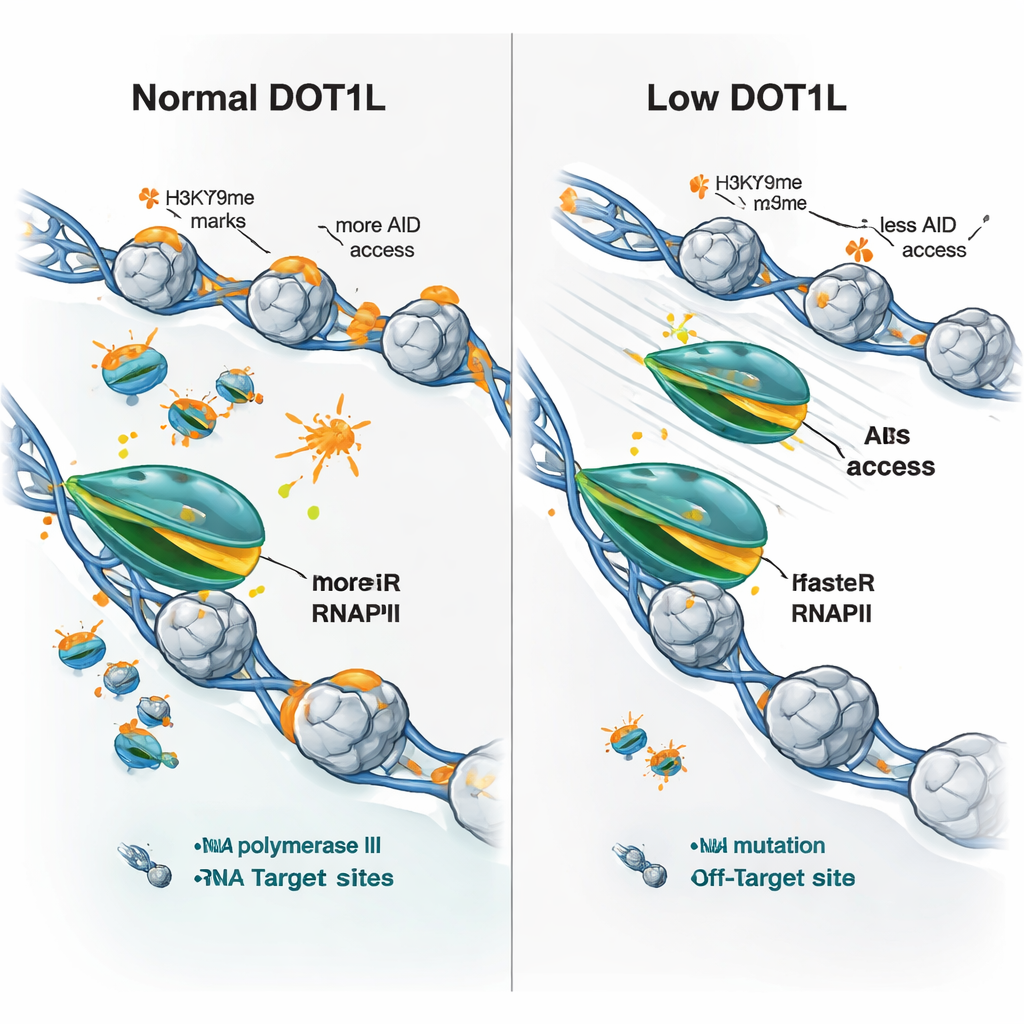
De onderzoekers vroegen zich vervolgens af of deze snelheidsveranderingen het gemengde patroon van genexpressie bij verlies van DOT1L konden verklaren — sommige genen gaan omhoog, andere omlaag. Ze vonden dat vrijwel alle DOT1L-gemarkeerde genen één gemeenschappelijke eigenschap hadden in knockoutcellen: snellere elongatie door RNA-polymerase II. Maar de uitkomst hing af van de begintoestand. Langzame, zwak tot expressie gebrachte genen neigden ertoe meer RNA te produceren wanneer de polymerase sneller werd, terwijl zeer actieve, lange genen met al snelle polymerasen soms minder produceerden, waarschijnlijk omdat te snelle doorgang efficiënte verwerking of voltooiing verstoort. Cruciaal is dat bij zowel antilichaamgenen als klassieke AID-off-targets het verlies van DOT1L leidde tot snellere polymerasebeweging, minder aanwijzingen voor polymerase ‘vastlopen’ en aanzienlijk verminderde AID-bezetting, zelfs wanneer die genen zelf niet minder actief waren.
Waarom dit belangrijk is voor immuniteit en kanker
Gezamenlijk schetst het werk DOT1L als een subtiele verkeersregelaar voor het machinerie dat genen leest in B-cellen. Door specifieke histoonmerken aan te brengen, vertraagt DOT1L RNA-polymerase II licht en verlengt het de pauzes, waardoor een transcriptie-omgeving ontstaat waarin AID productief antilichaamgenen kan benaderen — en helaas ook een beperkte set andere kwetsbare genen — om mutaties in te brengen. Wanneer DOT1L ontbreekt of geïnhibeerd wordt, scheurt de polymerase erdoorheen en blijft AID met minder kansen om te handelen, wat de diversificatie van antilichamen vermindert en tegelijkertijd het risico op bepaalde schadelijke herschikkingen verlaagt. Dit mechanistische inzicht verklaart waarom verlies van DOT1L zowel genexpressie kan verhogen als verlagen, en verbindt de fijne controle van transcriptiesnelheid rechtstreeks met waar ons immuunsysteem durft zijn eigen DNA te herschrijven.
Bronvermelding: Subramani, P.G., Seija, N., Ridani, J. et al. DOT1L activity limits transcription elongation velocity and favors RNAPII pausing to facilitate mutagenesis by AID. Nat Commun 17, 1623 (2026). https://doi.org/10.1038/s41467-026-68332-4
Trefwoorden: antilichaamdiversificatie, AID-enzym, DOT1L, gentranscriptie, B-cellen